Clear Sky Science · pl
Oś kaspaza‑1–EGR4 reguluje repolaryzację makrofagów w komórkach ostrej białaczki szpikowej
Przywracanie równowagi komórek walczących z rakiem
Ostra białaczka szpikowa (AML) to agresywny nowotwór krwi, który nie tylko rozwija się bez kontroli — także dyskretnie przebudowuje układ odpornościowy, by sprzyjać wzrostowi guza. W tym badaniu ujawniono, jak komórki białaczkowe potrafią nakłonić pobliskie komórki odpornościowe zwane makrofagami do przyjęcia trybu wspierającego guz, oraz zidentyfikowano molekularny „przełącznik”, który może zostać odwrócony, by przywrócić tym komórkom stan zwalczający nowotwór. Zrozumienie tego przełącznika może otworzyć nowe drogi do zwiększenia skuteczności istniejących terapii immunologicznych.
Przyjazne i nieprzyjazne pomocniki odpornościowe
Makrofagi to białe krwinki, które normalnie bronią organizmu i usuwają uszkodzone tkanki. W wielu nowotworach, w tym w AML, mogą zostać „przeedukowane” do roli opiekuńczej, chroniącej komórki guza zamiast je atakować. Makrofagi związane z guzem zwykle przyjmują stan podobny do M2, który łagodzi zapalenie i wspiera przeżycie komórek nowotworowych, podczas gdy stan M1 jest bardziej agresywny i wrogi wobec guza. Autorzy skupili się na tym, jak komórki białaczki wpływają na tę równowagę, badając, które sygnały wydobywające się z samych komórek nowotworowych nakłaniają makrofagi do zostania albo szkodliwymi wspomagaczami, albo pomocnymi bojownikami.
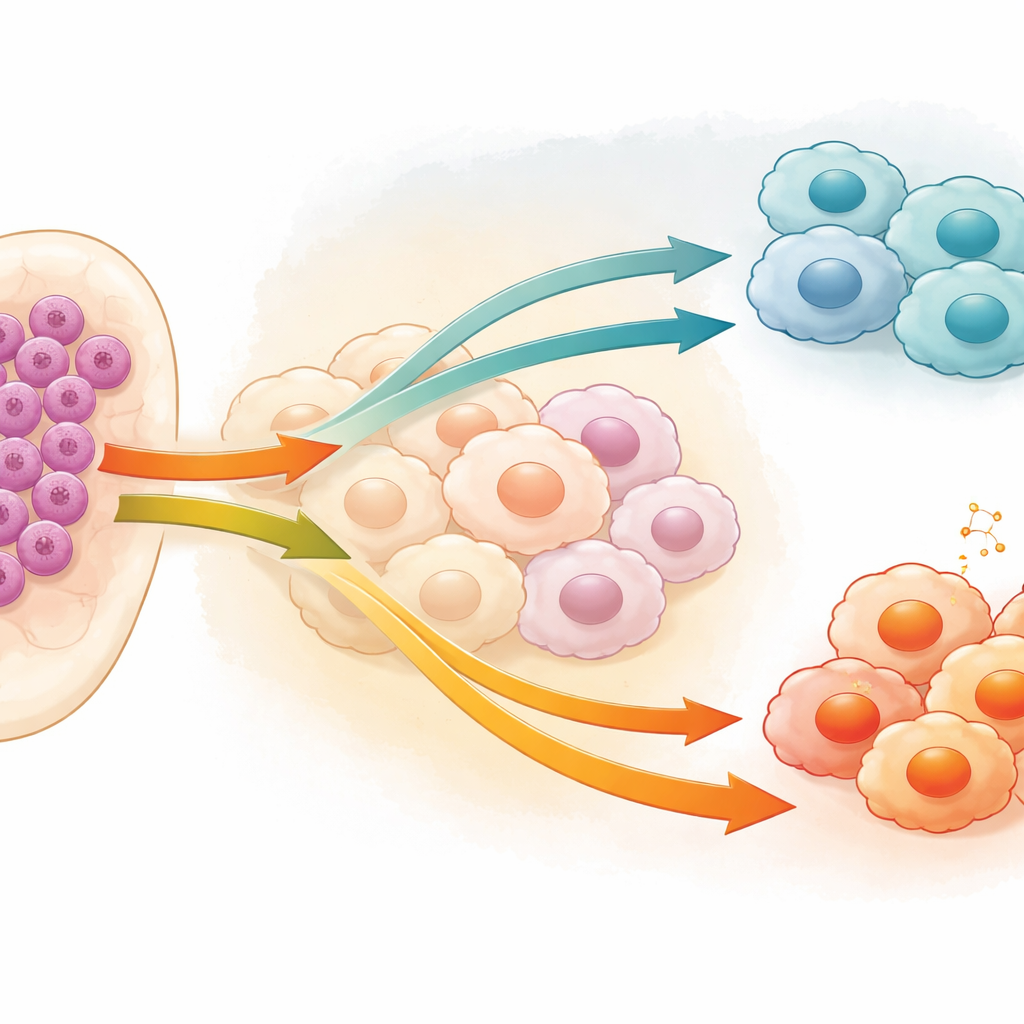
Ukryta ścieżka sygnalizacyjna w komórkach białaczki
Zespół skupił się na białku zwanym kaspazą‑1 (CASP1), najbardziej znanym z roli w zapalnym typie śmierci komórki, choć jego zachowanie w raku bywa złożone i niekiedy sprzeczne. Stwierdzili, że komórki AML często mają wysokie poziomy CASP1, a ten wzrost wiąże się z większą obecnością makrofagów wspierających guz o fenotypie M2. Używając dwóch ludzkich linii komórek AML, zmniejszyli aktywność CASP1 i zebrali koktajl związków uwalnianych przez zmodyfikowane komórki białaczkowe do otoczenia. Gdy przygotowany w ten sposób czynnik zastosowano do hodowanych w laboratorium makrofagów, wykazywały one mniej cech M2 i więcej charakterystyk związanych ze stanem M1, walczącym z guzem. Ta zmiana była widoczna na poziomie genów, markerów białkowych na powierzchni komórek oraz w ogólnym składzie populacji komórkowych.
Odkrycie kluczowego hamulca: EGR4
Aby zrozumieć, jak CASP1 w komórkach białaczki może tak silnie wpływać na makrofagi na zewnątrz, badacze zbadali globalną aktywność genów po obniżeniu poziomu CASP1. Odkryli, że poziomy czynnika transkrypcyjnego zwanego EGR4 gwałtownie wzrastały po wyciszeniu CASP1. Dalsze testy potwierdziły, że EGR4 działa jak molekularny hamulec zdolności komórki białaczkowej do nakierowywania makrofagów na stan M2. Gdy naukowcy celowo ponownie obniżyli EGR4 w komórkach pozbawionych CASP1, wcześniejsza korzystna zmiana w zachowaniu makrofagów częściowo zniknęła. Wskazywało to, że EGR4 jest kluczowym elementem pośredniczącym, przez który CASP1 wywiera swoje efekty na mikrośrodowisko guza.
Jak jedna ścieżka przechyla równowagę
Zagłębiając się dalej, badanie powiązało parę CASP1–EGR4 z innym dobrze znanym szlakiem sygnałowym, drogą IL‑10/STAT3, która silnie sprzyja makrofagom o fenotypie M2 wspierającym guz. Gdy CASP1 został obniżony w komórkach białaczki, sygnały zwykle aktywujące ten szlak w pobliskich makrofagach uległy przytłumieniu, w szczególności przeciwzapalna cząsteczka IL‑10 i jej partner, ufosforylowany STAT3. Obniżenie EGR4 cofnęło w dużej mierze to przytłumienie, ponownie podkreślając jego centralną rolę. U myszy wszczepionych ludzkimi komórkami AML blokada CASP1 nie tylko spowolniła wzrost guza, lecz także przebudowała mikrośrodowisko guza: makrofagi oddaliły się od cech M2, znaczniki podziału komórkowego spadły, a poziomy EGR4 wzrosły — wszystko zgodne z mniej przyjaznym niszą dla komórek białaczkowych.
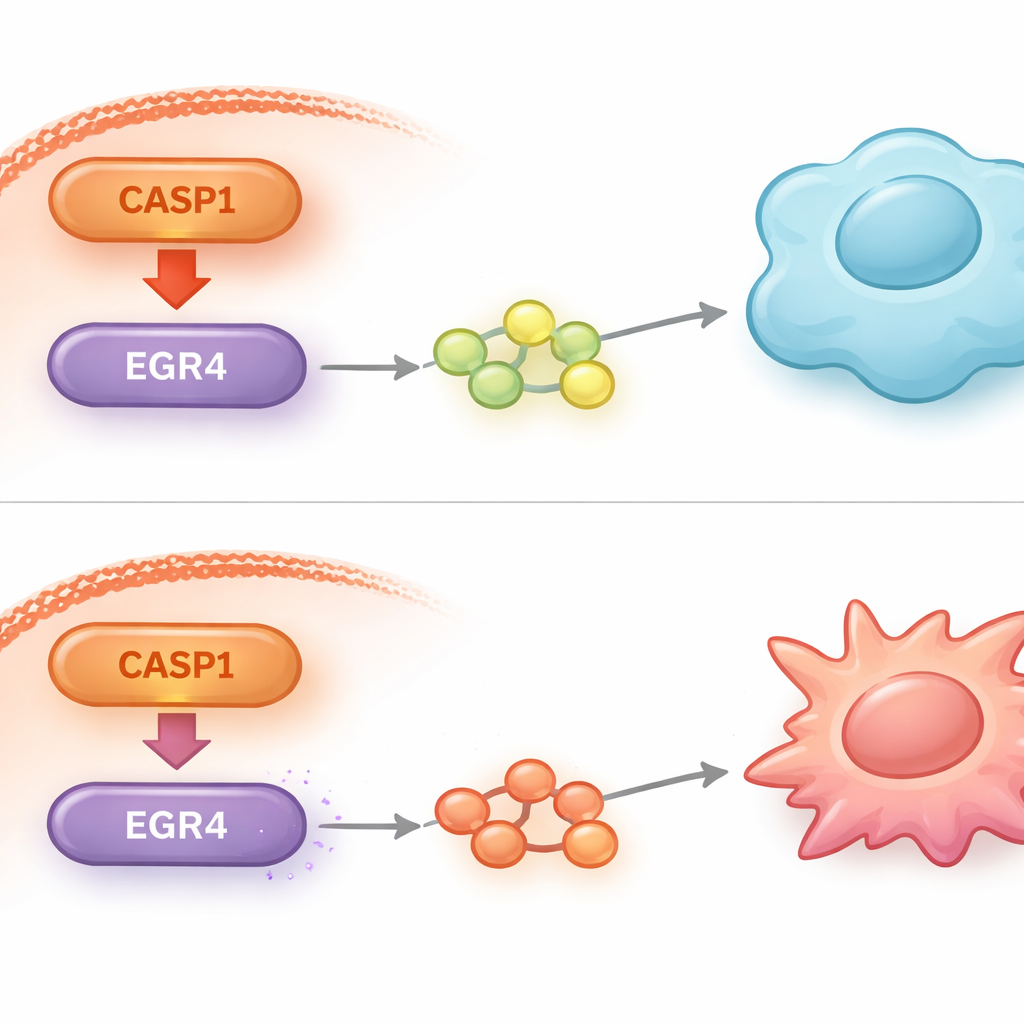
Co to może znaczyć dla przyszłego leczenia
Dla osoby niebędącej specjalistą główny wniosek jest taki, że komórki białaczki nie działają samodzielnie; aktywnie „szkolą” pobliskie komórki odpornościowe, aby je chroniły. Praca ta identyfikuje konkretny łańcuch dowodzenia — CASP1 kontroluje EGR4, który z kolei kształtuje sygnały skłaniające makrofagi do roli sprzyjającej guzowi. Przerwanie tego łańcucha sprawia, że otoczenie guza staje się mniej wspierające i spowalnia rozwój raka u zwierząt. Ponieważ istnieją już leki hamujące CASP1, testowane u ludzi w innych schorzeniach, szlak CASP1–EGR4 oferuje obiecujący nowy kierunek terapii mających na celu przebudzenie własnych mechanizmów immunologicznych organizmu przeciw AML.
Cytowanie: Qian, Y., Chen, Y., Feng, ZX. et al. The Caspase-1-EGR4 axis regulates macrophage repolarization in acute myeloid leukemia cells. Sci Rep 16, 11319 (2026). https://doi.org/10.1038/s41598-026-41381-x
Słowa kluczowe: ostra białaczka szpikowa, mikrośrodowisko guza, polaryzacja makrofagów, kaspaza‑1, szlak sygnałowy STAT3