Clear Sky Science · de
Die Caspase-1–EGR4-Achse reguliert die Re‑Polarisation von Makrophagen in akuten myeloischen Leukämiezellen
Die körpereigenen krebsbekämpfenden Zellen neu ausbalancieren
Akute myeloische Leukämie (AML) ist eine aggressive Blutkrebserkrankung, die nicht nur unkontrolliert wächst, sondern auch das Immunsystem so umgestaltet, dass der Tumor besser gedeihen kann. Diese Studie deckt auf, wie Leukämiezellen benachbarte Immunzellen, sogenannte Makrophagen, in einen tumorfördernden Zustand drängen können, und identifiziert einen molekularen „Schalter“, mit dem sich diese Zellen wieder in einen tumorbekämpfenden Zustand zurückversetzen lassen. Das Verständnis dieses Schalters könnte neue Wege eröffnen, bereits bestehende immunbasierte Therapien wirksamer zu machen.
Freundliche und unfreundliche Immunhelfer
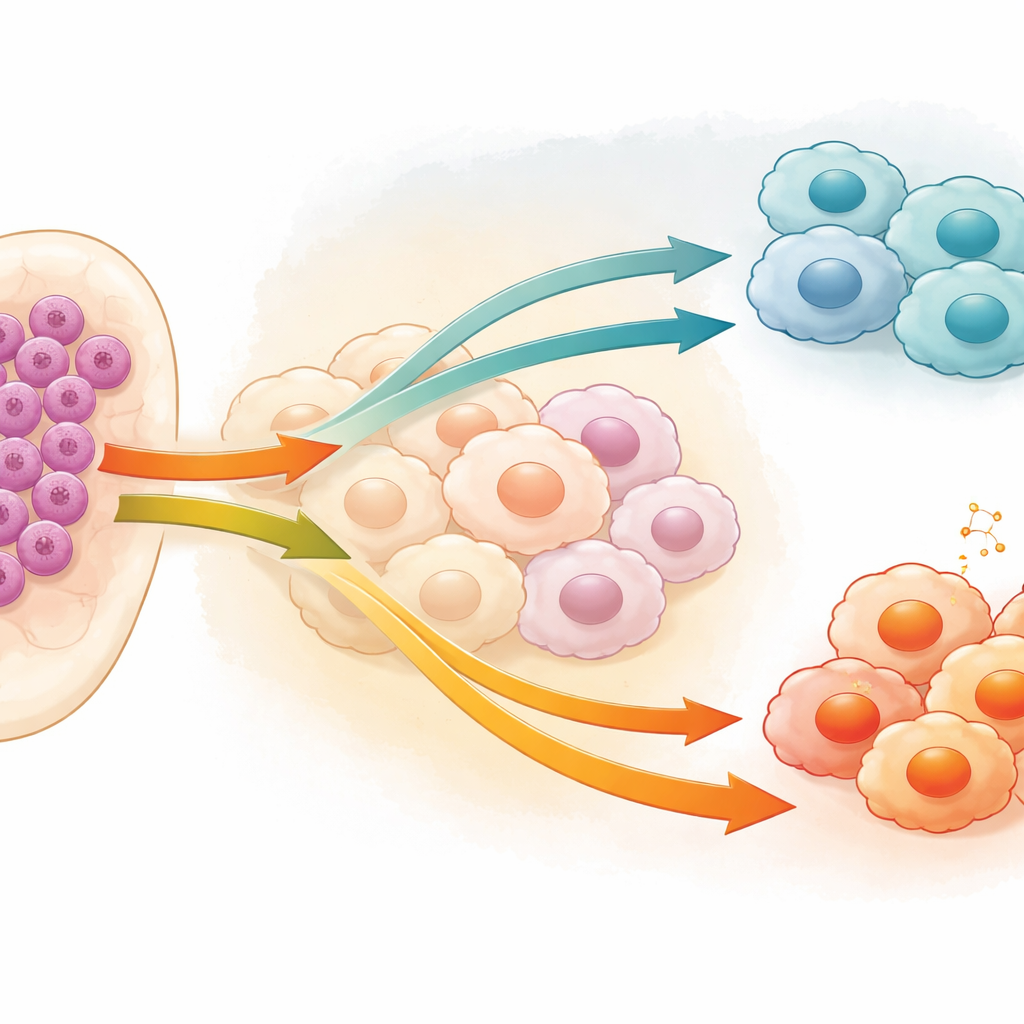
Makrophagen sind weiße Blutkörperchen, die normalerweise bei der Abwehr des Körpers und der Beseitigung beschädigten Gewebes helfen. In vielen Krebsarten, einschließlich AML, können sie „umprogrammiert“ werden und eine fürsorgliche Rolle übernehmen, die Tumorzellen schützt statt angreift. Diese tumorumgebungsassoziierten Makrophagen neigen dazu, einen M2‑ähnlichen Zustand anzunehmen, der Entzündungen dämpft und das Überleben von Krebszellen unterstützt, während der M1‑Zustand aggressiver ist und Tumoren feindlich gegenübersteht. Die Autorinnen und Autoren konzentrierten sich darauf, wie Leukämiezellen dieses Gleichgewicht beeinflussen und welche Signale von den Krebszellen selbst Makrophagen veranlassen, entweder schädliche Helfer oder hilfreiche Kämpfer zu werden.
Eine verborgene Signalkaskade innerhalb von Leukämiezellen
Das Team richtete den Fokus auf ein Protein namens Caspase‑1 (CASP1), das vor allem für seine Rolle beim entzündlichen Zelltod bekannt ist, dessen Verhalten im Krebs aber komplex und teils widersprüchlich ist. Sie fanden heraus, dass AML‑Zellen häufig hohe CASP1‑Spiegel aufweisen und dass dieser Anstieg mit einer vermehrten Präsenz tumorfördernder M2‑Makrophagen einhergeht. Anhand zweier humaner AML‑Zelllinien reduzierten sie die CASP1‑Aktivität und sammelten den Cocktail aus Molekülen, den diese veränderten Leukämiezellen in ihre Umgebung abgaben. Wurde dieses konditionierte Medium auf im Labor kultivierte Makrophagen aufgebracht, zeigten die Makrophagen weniger M2‑Merkmale und mehr Eigenschaften, die mit dem M1, dem tumorbekämpfenden Zustand, assoziiert sind. Diese Verschiebung trat auf Genebene, in Oberflächenproteinkennzeichen und im allgemeinen Muster der Zellpopulationen zutage.
Entdeckung einer wichtigen Bremse: EGR4
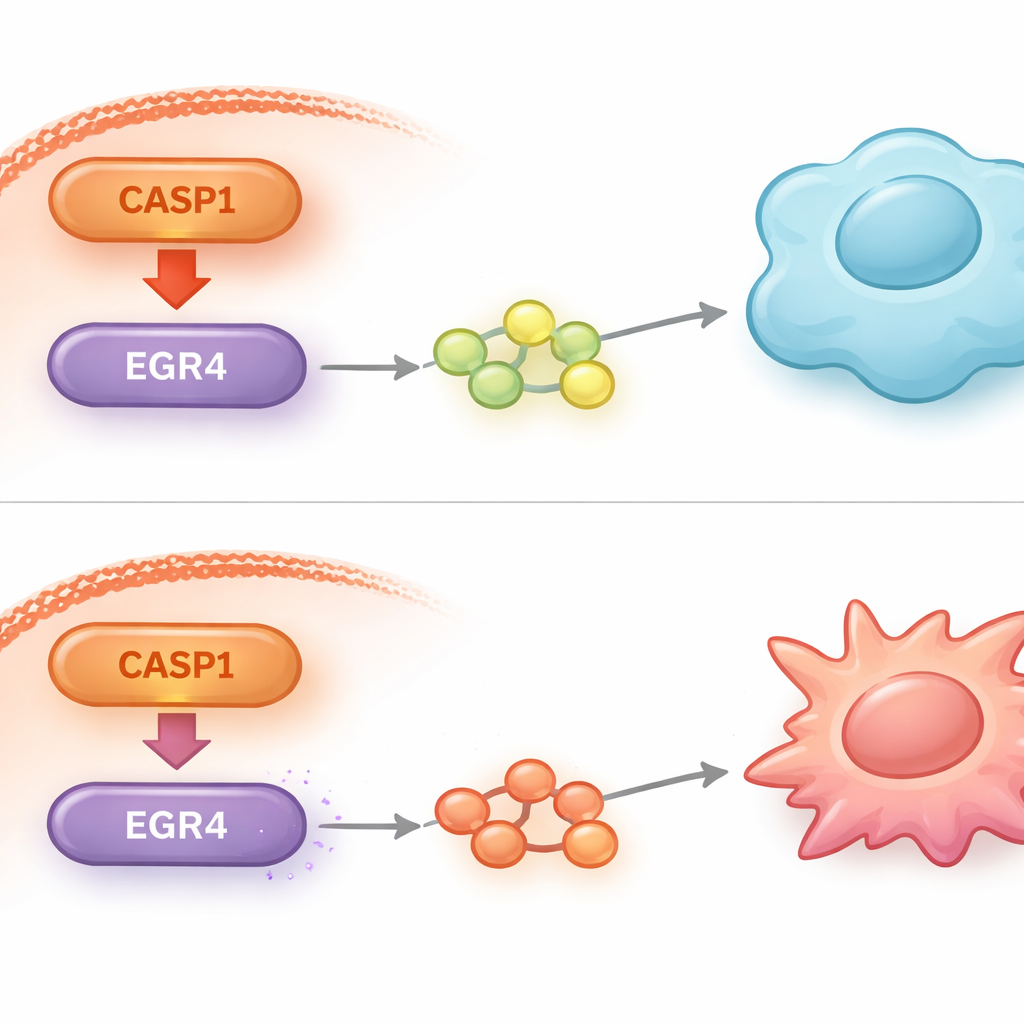
Um zu verstehen, wie CASP1 in Leukämiezellen außerhalb befindliche Makrophagen so stark beeinflussen kann, untersuchten die Forschenden die globale Genaktivität nachdem CASP1 reduziert worden war. Sie entdeckten, dass die Spiegel eines Transkriptionsfaktors namens EGR4 stark anstiegen, wenn CASP1 herunterreguliert wurde. Weitere Tests bestätigten, dass EGR4 wie eine molekulare Bremse auf die Fähigkeit der Leukämiezelle wirkt, Makrophagen in den M2‑Zustand zu treiben. Wenn die Wissenschaftlerinnen und Wissenschaftler EGR4 in CASP1‑defizienten Zellen gezielt wieder senkten, ging die zuvor beobachtete vorteilhafte Verschiebung im Makrophagenverhalten teilweise verloren. Das deutet darauf hin, dass EGR4 ein entscheidender nachgeschalteter Akteur ist, über den CASP1 seine Effekte auf die Tumorumgebung ausübt.
Wie ein einziger Signalweg das Gleichgewicht kippt
Bei tieferer Untersuchung verband die Studie das CASP1–EGR4‑Paar mit einer weiteren bekannten Signalkaskade, dem IL‑10/STAT3‑Weg, der stark M2‑ähnliche, tumorfördernde Makrophagen begünstigt. Wenn CASP1 in Leukämiezellen reduziert wurde, waren die Signale, die normalerweise diesen Weg in benachbarten Makrophagen aktivieren, abgeschwächt, insbesondere das anti‑entzündliche Molekül IL‑10 und dessen Partner, phosphoryliertes STAT3. Die Erniedrigung von EGR4 hob einen Großteil dieser Abschwächung wieder auf und unterstrich erneut seine zentrale Rolle. In Mäusen, die mit humanen AML‑Zellen transplantiert wurden, verlangsamte die Hemmung von CASP1 nicht nur das Tumorwachstum, sondern remodellierte auch die Tumormikroumgebung: Makrophagen entfernten sich von M2‑Eigenschaften, Marker der Zellteilung gingen zurück und EGR4‑Spiegel stiegen, alles Hinweise auf eine weniger einladende Nische für Leukämiezellen.
Was das für künftige Behandlungen bedeuten könnte
Für Nicht‑Spezialisten lautet die wichtigste Erkenntnis, dass die Leukämiezellen nicht isoliert handeln; sie trainieren aktiv benachbarte Immunzellen, sie zu beschützen. Diese Arbeit identifiziert eine klare Befehlskette — CASP1 steuert EGR4, das wiederum Signale formt, die Makrophagen in eine tumorfördernde Rolle drängen. Das Durchbrechen dieser Kette macht die Tumorumgebung weniger unterstützend und verlangsamt das Krebswachstum in Tiermodellen. Da es bereits Wirkstoffe gibt, die CASP1 hemmen und die bereits beim Menschen für andere Erkrankungen getestet wurden, bietet der CASP1–EGR4‑Weg einen vielversprechenden neuen Ansatz für Therapien, die darauf abzielen, die körpereigenen Immunabwehrkräfte gegen AML wiederzubeleben.
Zitation: Qian, Y., Chen, Y., Feng, ZX. et al. The Caspase-1-EGR4 axis regulates macrophage repolarization in acute myeloid leukemia cells. Sci Rep 16, 11319 (2026). https://doi.org/10.1038/s41598-026-41381-x
Schlüsselwörter: akute myeloische Leukämie, tumormikroumgebung, Makrophagenpolarisation, caspase-1, STAT3-Signalgebung