Clear Sky Science · fr
L’axe Caspase-1–EGR4 régule la repolarisation des macrophages dans les cellules de leucémie myéloïde aiguë
Rééquilibrer les cellules anti‑cancer de l’organisme
La leucémie myéloïde aiguë (LMA) est un cancer du sang agressif qui ne se contente pas de proliférer de manière incontrôlée : il reconfigure silencieusement le système immunitaire pour favoriser la survie de la tumeur. Cette étude révèle comment les cellules leucémiques peuvent pousser des cellules immunitaires voisines, appelées macrophages, vers un état qui soutient la tumeur, et identifie un « interrupteur » moléculaire susceptible d’être actionné pour ramener ces mêmes macrophages à un état combattant la tumeur. Mieux comprendre cet interrupteur pourrait ouvrir de nouvelles voies pour améliorer l’efficacité des traitements immunomodulateurs existants.
Alliés immunitaires bienveillants et hostiles
Les macrophages sont des globules blancs qui, en conditions normales, défendent l’organisme et nettoient les tissus endommagés. Dans de nombreux cancers, y compris la LMA, ils peuvent être « rééduqués » en un rôle nourricier qui protège les cellules tumorales au lieu de les attaquer. Ces macrophages associés aux tumeurs tendent à adopter un profil de type M2, qui calme l’inflammation et favorise la survie des cellules cancéreuses, tandis que l’état M1 est plus agressif et hostile aux tumeurs. Les auteurs se sont intéressés à la façon dont les cellules leucémiques influencent cet équilibre, en se demandant quels signaux émis par les cellules cancéreuses elles‑mêmes poussent les macrophages à devenir soit des aides nuisibles, soit des combattants utiles.
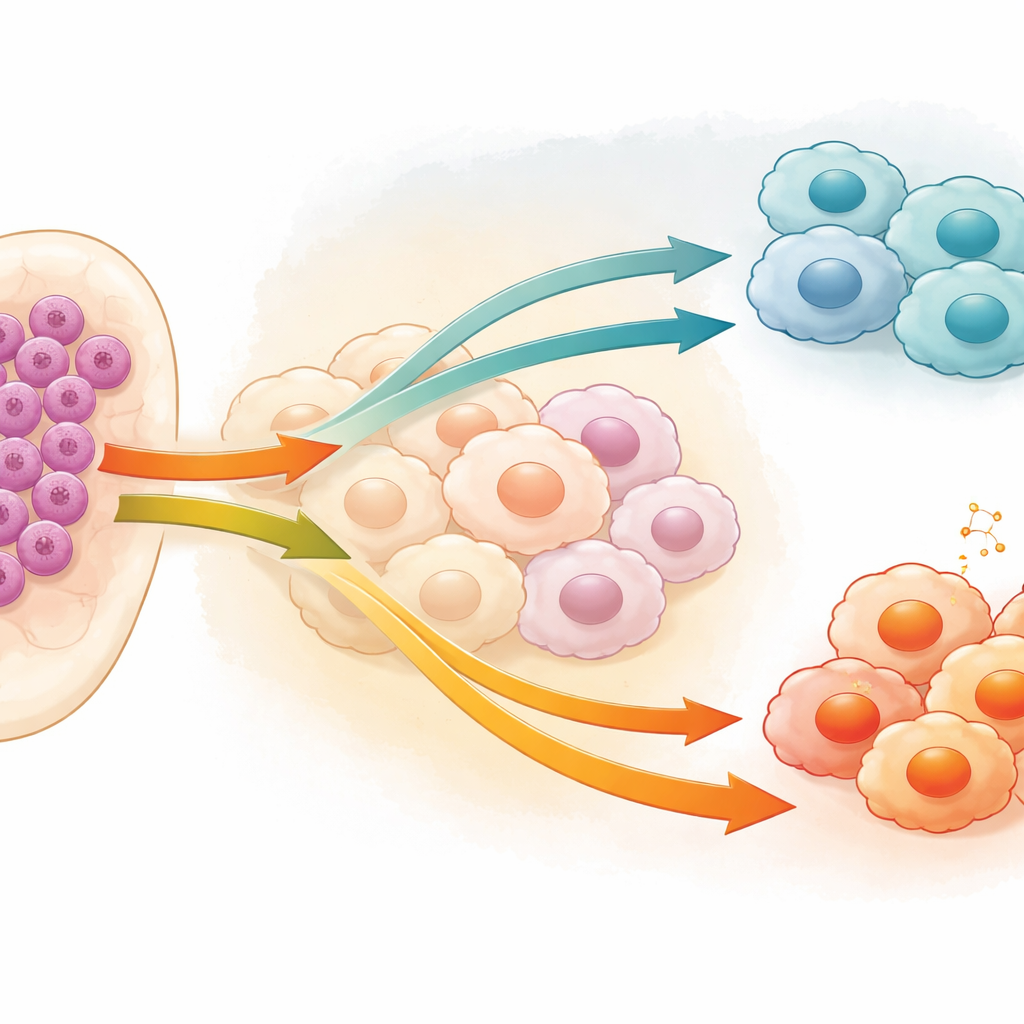
Une route de signalisation cachée au sein des cellules leucémiques
L’équipe s’est focalisée sur une protéine appelée caspase‑1 (CASP1), surtout connue pour son rôle dans la mort cellulaire inflammatoire, mais dont le comportement dans le cancer est complexe et parfois contradictoire. Ils ont constaté que les cellules de LMA présentent souvent des niveaux élevés de CASP1, et que cette augmentation est associée à une plus grande présence de macrophages de type M2 qui soutiennent la tumeur. En utilisant deux lignées cellulaires humaines de LMA, ils ont réduit l’activité de CASP1 et recueilli le cocktail de molécules libérées par ces cellules leucémiques modifiées. Lorsqu’un milieu conditionné par ces cellules était appliqué à des macrophages cultivés en laboratoire, ces derniers présentaient moins de traits M2 et davantage de caractéristiques associées à l’état M1, combattant la tumeur. Ce basculement se manifestait au niveau de l’expression génique, des marqueurs protéiques de surface et de la répartition globale des populations cellulaires.
Découverte d’un frein clé : EGR4
Pour comprendre comment CASP1 à l’intérieur des cellules leucémiques pouvait influencer à ce point les macrophages externes, les chercheurs ont examiné l’activité génique globale après réduction de CASP1. Ils ont découvert que les niveaux d’un facteur de transcription nommé EGR4 augmentaient fortement lorsque CASP1 était atténué. Des tests supplémentaires ont confirmé qu’EGR4 agit comme un frein moléculaire sur la capacité des cellules leucémiques à orienter les macrophages vers l’état M2. Lorsque les scientifiques ont volontairement diminué à nouveau EGR4 dans des cellules déficientes en CASP1, le changement bénéfique observé précédemment dans le comportement des macrophages a été partiellement annulé. Cela indique qu’EGR4 est un acteur en aval crucial par lequel CASP1 exerce ses effets sur le microenvironnement tumoral.
Comment une voie bascule l’équilibre
En approfondissant, l’étude a relié le couple CASP1–EGR4 à une autre voie de signalisation bien connue, la voie IL‑10/STAT3, qui favorise fortement les macrophages de type M2 et l’environnement tumoral. Lorsque CASP1 était réduit dans les cellules leucémiques, les signaux qui activent normalement cette voie chez les macrophages voisins étaient atténués, en particulier la molécule anti‑inflammatoire IL‑10 et son partenaire, STAT3 phosphorylé. La diminution d’EGR4 annulait en grande partie cette atténuation, soulignant à nouveau son rôle central. Chez des souris implantées avec des cellules humaines de LMA, le blocage de CASP1 n’a pas seulement ralenti la croissance tumorale mais a aussi remodelé le microenvironnement tumoral : les macrophages ont perdu des caractéristiques M2, les marqueurs de prolifération ont diminué et les niveaux d’EGR4 ont augmenté, cohérent avec une niche moins favorable aux cellules leucémiques.
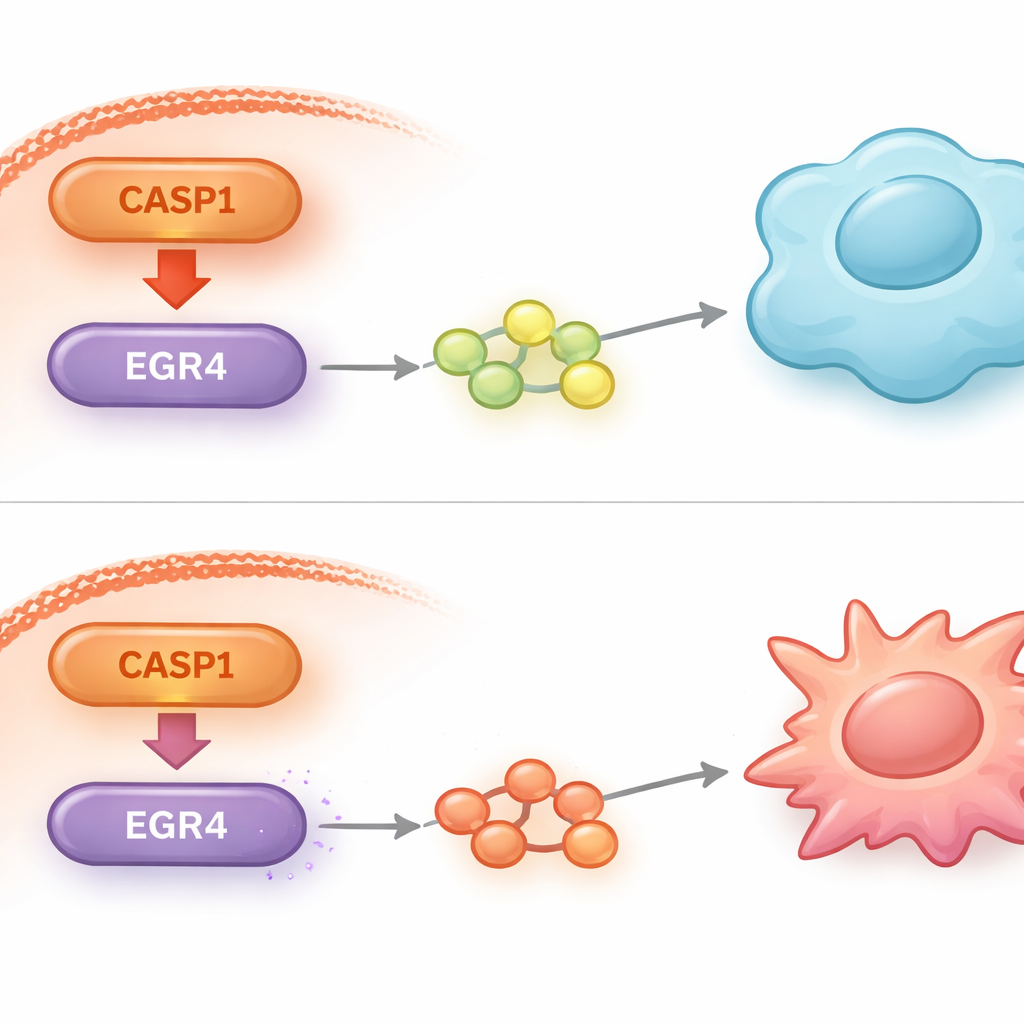
Ce que cela pourrait signifier pour les traitements futurs
Pour un non‑spécialiste, la conclusion principale est que les cellules leucémiques n’agissent pas seules ; elles entraînent activement les cellules immunitaires voisines à les protéger. Ce travail identifie une chaîne de commandement spécifique : CASP1 contrôle EGR4, qui à son tour module des signaux poussant les macrophages vers un rôle favorable à la tumeur. Rompre cette chaîne rend le microenvironnement tumoral moins accueillant et ralentit la croissance du cancer chez l’animal. Parce que des médicaments inhibant CASP1 existent déjà et ont été testés chez l’humain pour d’autres pathologies, la voie CASP1–EGR4 offre un angle prometteur pour des thérapies visant à réveiller les défenses immunitaires de l’organisme contre la LMA.
Citation: Qian, Y., Chen, Y., Feng, ZX. et al. The Caspase-1-EGR4 axis regulates macrophage repolarization in acute myeloid leukemia cells. Sci Rep 16, 11319 (2026). https://doi.org/10.1038/s41598-026-41381-x
Mots-clés: leucémie myéloïde aiguë, microenvironnement tumoral, polarisation des macrophages, caspase-1, signalisation STAT3