Clear Sky Science · nl
De Caspase-1–EGR4-as reguleert herpolarisatie van macrofagen in acute myeloïde leukemiecellen
Het herstel van het evenwicht van de kankebestrijdende cellen van het lichaam
Acute myeloïde leukemie (AML) is een agressieve bloedkanker die niet alleen ongecontroleerd groeit, maar ook stilletjes het immuunsysteem herprogrammeert zodat de tumor kan gedijen. Deze studie onthult hoe leukemiecellen nabije immuuncellen, zogenaamde macrofagen, in een tumor-ondersteunende modus duwen, en identificeert een moleculaire "schakelaar" die mogelijk kan worden omgezet om diezelfde cellen terug te brengen in een tumorbestrijdende staat. Inzicht in deze schakelaar kan nieuwe wegen openen om bestaande immuungerichte behandelingen effectiever te maken.
Vriendelijke en onvriendelijke immuunhulpen
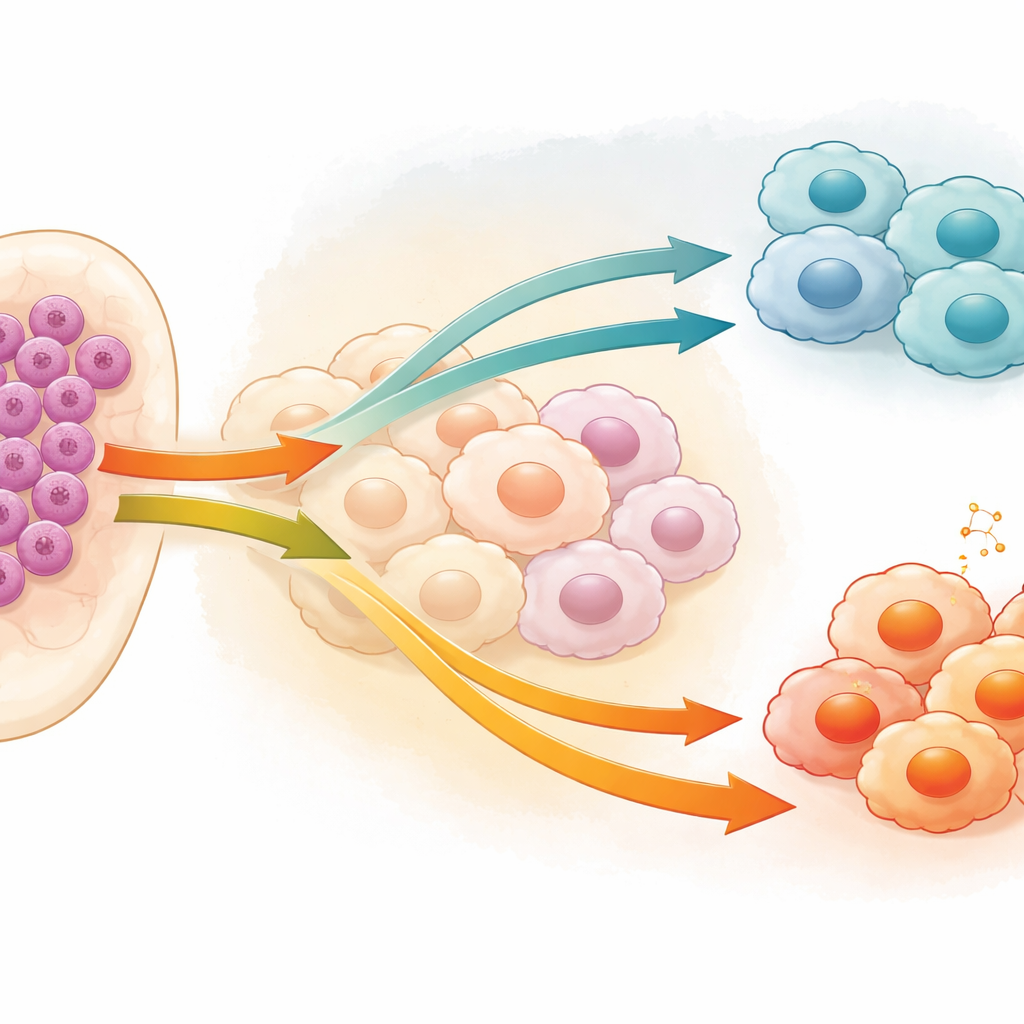
Macrofagen zijn witte bloedcellen die normaal het lichaam verdedigen en beschadigd weefsel opruimen. In veel vormen van kanker, waaronder AML, kunnen ze worden "heropgevoed" naar een verzorgende rol die tumorcellen beschermt in plaats van aanvalt. Deze tumorgeassocieerde macrofagen neigen naar een M2-achtig stadium, dat ontsteking dempt en het overleven van kankercellen ondersteunt, terwijl de M1-toestand agressiever is en vijandig staat tegenover tumoren. De auteurs concentreerden zich op hoe leukemiecellen dit evenwicht beïnvloeden en stelden de vraag welke signalen afkomstig van de kankecellen zelf macrofagen instrueren om schadelijke helpers of juist nuttige strijders te worden.
Een verborgen signaalroute binnen leukemiecellen
Het team richtte zich op een eiwit genaamd caspase-1 (CASP1), vooral bekend om zijn rol bij inflammatoir celdood, maar waarvan het gedrag in kanker complex en soms tegenstrijdig is. Ze vonden dat AML-cellen vaak hoge niveaus van CASP1 hebben, en dat deze toename samenhangt met een grotere aanwezigheid van tumor-ondersteunende M2-macrofagen. Met twee menselijke AML-celijnen verminderden ze de CASP1-activiteit en verzamelden de cocktail van moleculen die deze gewijzigde leukemiecellen in hun omgeving afscheidden. Wanneer dit geconditioneerde medium op in het laboratorium gekweekte macrofagen werd toegepast, vertoonden de macrofagen minder M2-eigenschappen en meer kenmerken die samenhangen met de M1, tumorbestrijdende staat. Deze verschuiving kwam tot uiting op genniveau, in eiwitmarkers op het celoppervlak en in het algemene patroon van celpopulaties.
Het ontdekken van een belangrijke rem: EGR4
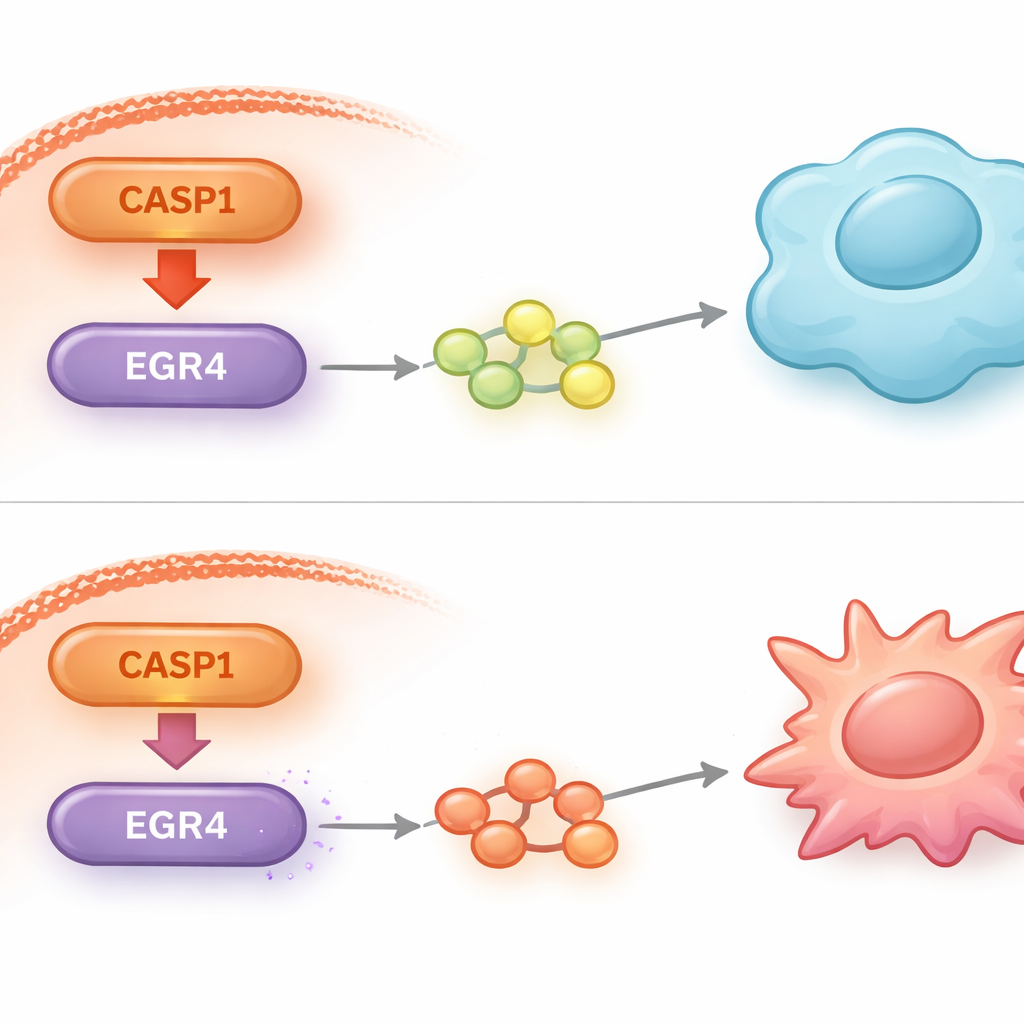
Om te begrijpen hoe CASP1 binnenin leukemiecellen zo sterk macrofagen van buitenaf kon beïnvloeden, onderzochten de onderzoekers de globale genactiviteit nadat CASP1 was verminderd. Ze ontdekten dat de niveaus van een transcriptiefactor genaamd EGR4 sterk stegen toen CASP1 werd gereduceerd. Verdere tests bevestigden dat EGR4 fungeert als een moleculaire rem op het vermogen van de leukemiecellen om macrofagen in de M2-toestand te drijven. Toen de wetenschappers EGR4 opzettelijk weer verlaagden in CASP1-deficiënte cellen, verdween het eerder waargenomen gunstige effect op het macrofaangedrag gedeeltelijk. Dit gaf aan dat EGR4 een cruciale downstream-speler is waardoor CASP1 zijn effecten op de tumoromgeving uitoefent.
Hoe één pad het evenwicht doet kantelen
Diepergravend koppelde de studie het CASP1–EGR4-paar aan een ander bekend signaalpad, het IL-10/STAT3-pad, dat sterk M2-achtige, tumor-ondersteunende macrofagen bevordert. Toen CASP1 in leukemiecellen werd verminderd, werden de signalen die dit pad normaal activeren in nabije macrofagen gedempt, met name het anti-inflammatoire molecuul IL-10 en zijn partner, gefosforyleerd STAT3. Het verlagen van EGR4 maakte veel van deze demping weer ongedaan, wat opnieuw de centrale rol van EGR4 benadrukte. In muismodellen waarin menselijke AML-cellen waren ingebracht, vertraagde remming van CASP1 niet alleen de tumorgroei maar hervormde ook de tumormicro-omgeving: macrofagen bewogen weg van M2-eigenschappen, markeringen van celdeling daalden en EGR4-niveaus stegen, allemaal consistent met een minder gastvrije niche voor leukemiecellen.
Wat dit kan betekenen voor toekomstige behandelingen
Voor niet-specialisten is de belangrijkste conclusie dat de leukemiecellen niet alleen opereren; ze trainen actief nabije immuuncellen om hen te beschermen. Dit werk identificeert een specifieke commandoketen — CASP1 die EGR4 regelt, die op zijn beurt signalen vormgeeft die macrofagen naar een tumorvriendelijke rol duwen. Het doorbreken van deze keten maakt de omgeving van de tumor minder ondersteunend en vertraagt de kankergroei in diermodellen. Omdat geneesmiddelen die CASP1 remmen al bestaan en bij mensen voor andere aandoeningen zijn getest, biedt dit CASP1–EGR4-pad een veelbelovende nieuwe invalshoek voor therapieën gericht op het heractiveren van de eigen immuunverdediging van het lichaam tegen AML.
Bronvermelding: Qian, Y., Chen, Y., Feng, ZX. et al. The Caspase-1-EGR4 axis regulates macrophage repolarization in acute myeloid leukemia cells. Sci Rep 16, 11319 (2026). https://doi.org/10.1038/s41598-026-41381-x
Trefwoorden: acute myeloïde leukemie, tumormicro-omgeving, macrofagenpolarisatie, caspase-1, STAT3-signaaltransductie