Clear Sky Science · es
El eje Caspasa‑1‑EGR4 regula la repolarización de macrófagos en células de leucemia mieloide aguda
Reequilibrar las células que combaten el cáncer en el organismo
La leucemia mieloide aguda (LMA) es un cáncer sanguíneo agresivo que no solo crece sin control, sino que también remodela silenciosamente el sistema inmunitario para que el tumor prospere. Este estudio revela cómo las células leucémicas pueden inducir a las células inmunitarias cercanas, llamadas macrófagos, a adoptar un modo que apoya al tumor, e identifica un «interruptor» molecular que podría accionarse para devolver a esas mismas células a un estado que combata el tumor. Comprender este interruptor podría abrir nuevas vías para aumentar la eficacia de los tratamientos inmunitarios existentes.
Ayudantes inmunitarios: amistosos y hostiles
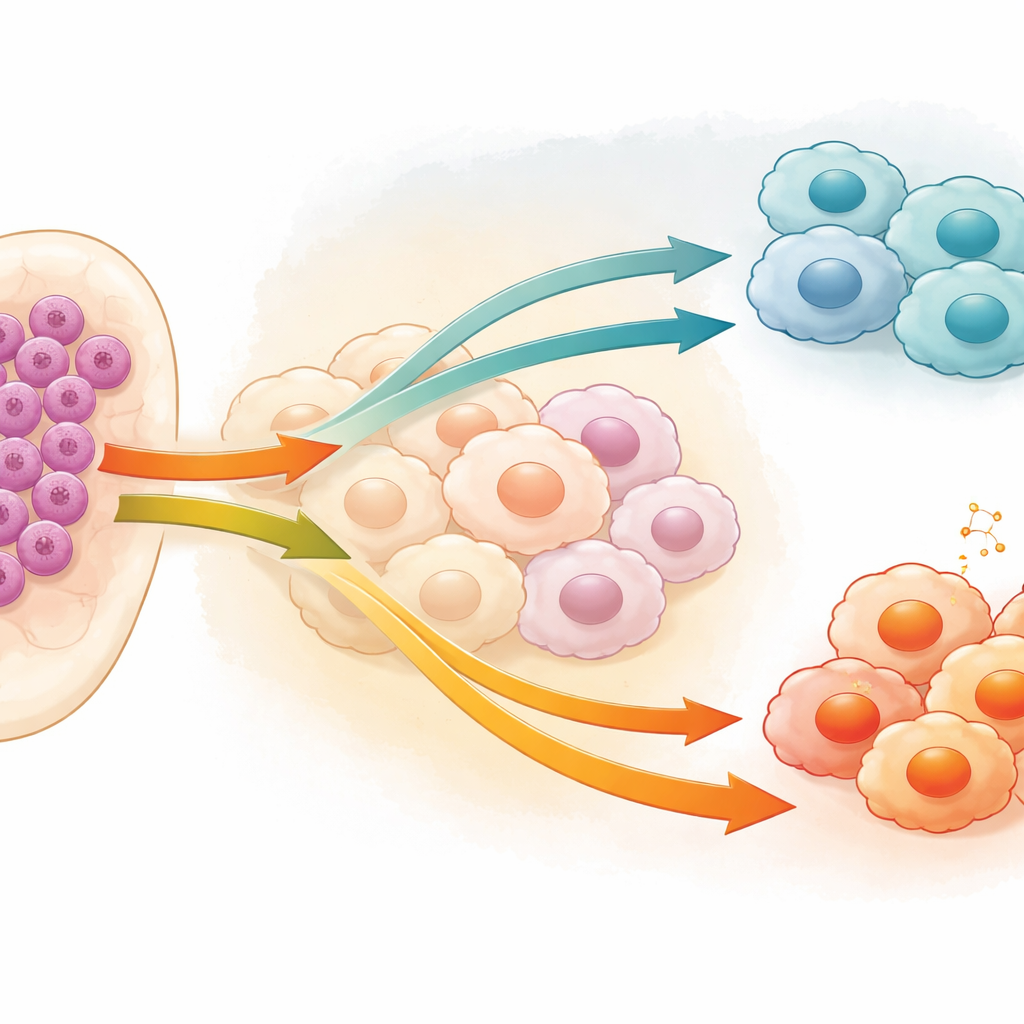
Los macrófagos son glóbulos blancos que normalmente ayudan a defender el organismo y a limpiar tejido dañado. En muchos cánceres, incluida la LMA, pueden «reeducarse» para desempeñar un papel protector que resguarda a las células tumorales en lugar de atacarlas. Estos macrófagos asociados a tumores tienden a adoptar un estado de tipo M2, que reduce la inflamación y favorece la supervivencia de las células cancerosas, mientras que el estado M1 es más agresivo y hostil para los tumores. Los autores se centraron en cómo las células leucémicas influyen en este equilibrio, preguntándose qué señales procedentes de las propias células cancerosas indican a los macrófagos que se conviertan en colaboradores nocivos o en luchadores útiles.
Una vía de señalización oculta dentro de las células leucémicas
El equipo se centró en una proteína llamada caspasa‑1 (CASP1), conocida sobre todo por su papel en la muerte celular inflamatoria, aunque su comportamiento en el cáncer es complejo y a veces contradictorio. Encontraron que las células de LMA suelen presentar niveles altos de CASP1, y que este aumento se vincula a una mayor presencia de macrófagos M2 que apoyan el tumor. Usando dos líneas celulares humanas de LMA, redujeron la actividad de CASP1 y recogieron el cóctel de moléculas que estas células leucémicas alteradas liberaban a su entorno. Cuando este medio condicionado se aplicó a macrófagos cultivados en el laboratorio, los macrófagos mostraron menos rasgos M2 y más características asociadas al estado M1, que combate el tumor. Este cambio se observó a nivel genético, en marcadores proteicos de la superficie celular y en el patrón global de las poblaciones celulares.
Descubriendo un freno clave: EGR4
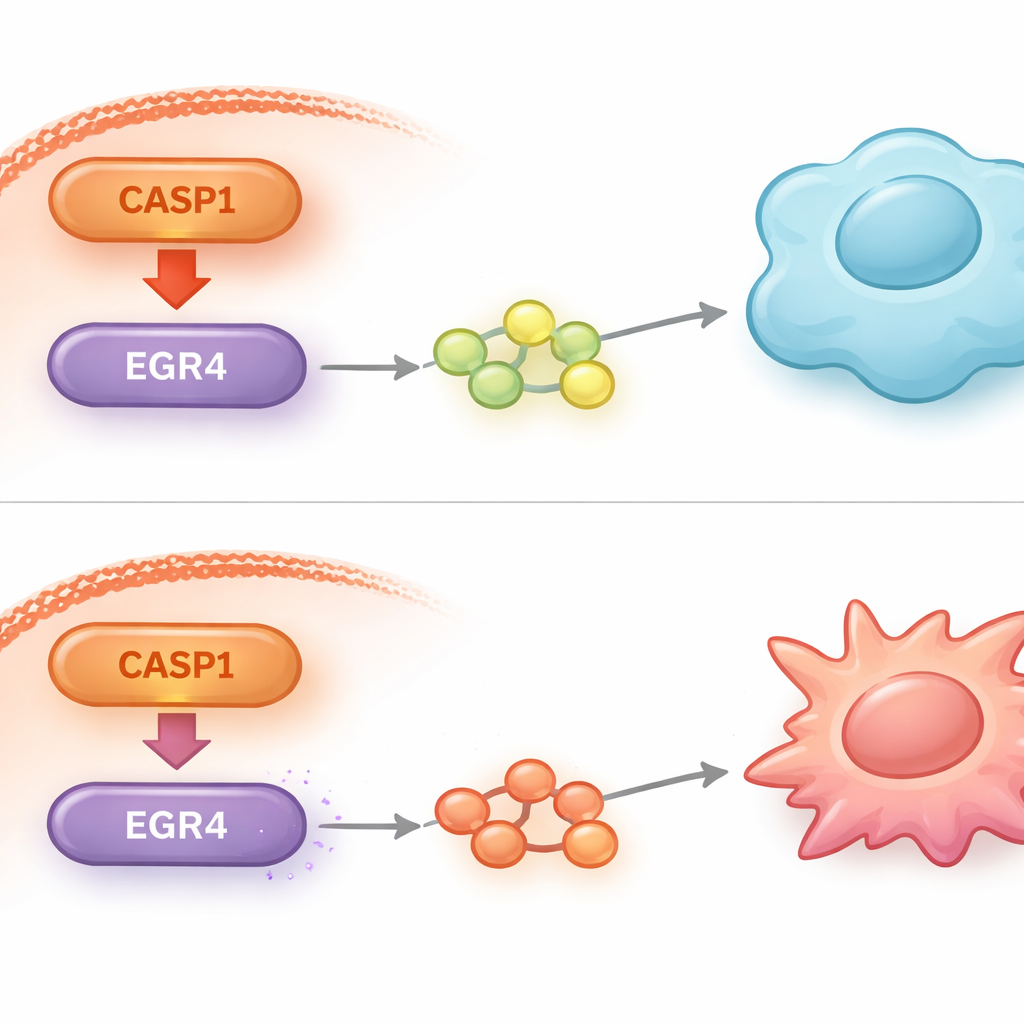
Para entender cómo CASP1 dentro de las células leucémicas podía influir tan fuertemente en macrófagos externos, los investigadores examinaron la actividad genética global tras la reducción de CASP1. Descubrieron que los niveles de un factor de transcripción llamado EGR4 aumentaban notablemente cuando CASP1 se suprimía. Pruebas adicionales confirmaron que EGR4 actúa como un freno molecular sobre la capacidad de la célula leucémica para impulsar a los macrófagos hacia el estado M2. Cuando los científicos redujeron deliberadamente EGR4 de nuevo en células deficientes en CASP1, el cambio beneficioso previo en el comportamiento de los macrófagos se perdió parcialmente. Esto indicó que EGR4 es un actor aguas abajo crucial a través del cual CASP1 ejerce sus efectos en el microambiente tumoral.
Cómo una vía inclina el equilibrio
Indagando más a fondo, el estudio vinculó el emparejamiento CASP1–EGR4 con otra vía de señalización bien conocida, la vía IL‑10/STAT3, que favorece con fuerza a los macrófagos de tipo M2 y que apoyan el tumor. Cuando CASP1 se redujo en las células leucémicas, las señales que normalmente activan esta vía en los macrófagos cercanos se atenuaron, en particular la molécula antiinflamatoria IL‑10 y su compañero, STAT3 fosforilado. La disminución de EGR4 deshizo gran parte de esta atenuación, subrayando de nuevo su papel central. En ratones implantados con células humanas de LMA, bloquear CASP1 no solo ralentizó el crecimiento tumoral, sino que también remodeló el microambiente tumoral: los macrófagos se alejaron de rasgos M2, descendieron los marcadores de división celular y aumentaron los niveles de EGR4, todo ello consistente con un nicho menos favorable para las células leucémicas.
Qué podría significar esto para tratamientos futuros
Para un público no especialista, la conclusión principal es que las células leucémicas no actúan solas; están activamente instruyendo a las células inmunitarias cercanas para que las protejan. Este trabajo identifica una cadena de mando específica: CASP1 controla a EGR4, que a su vez moldea señales que empujan a los macrófagos hacia un papel favorable al tumor. Romper esta cadena hace que el entorno tumoral sea menos propicio y ralentiza el crecimiento del cáncer en modelos animales. Dado que existen fármacos inhibidores de CASP1 que ya se han probado en humanos para otras condiciones, la vía CASP1–EGR4 ofrece un ángulo prometedor para terapias destinadas a reactivar las defensas inmunitarias del propio organismo contra la LMA.
Cita: Qian, Y., Chen, Y., Feng, ZX. et al. The Caspase-1-EGR4 axis regulates macrophage repolarization in acute myeloid leukemia cells. Sci Rep 16, 11319 (2026). https://doi.org/10.1038/s41598-026-41381-x
Palabras clave: leucemia mieloide aguda, microambiente tumoral, polarización de macrófagos, caspasa‑1, señalización STAT3