Clear Sky Science · it
L’asse Caspase-1–EGR4 regola la ripolarizzazione dei macrofagi nelle cellule della leucemia mieloide acuta
Ribilanciare le cellule che combattono il cancro nell’organismo
La leucemia mieloide acuta (LMA) è un cancro del sangue aggressivo che non si limita a crescere in modo incontrollato: rimodella anche in modo silenzioso il sistema immunitario per favorire la sopravvivenza del tumore. Questo studio rivela come le cellule leucemiche possano spingere i macrofagi circostanti verso uno stato che supporta il tumore e identifica un “interruttore” molecolare che potrebbe essere azionato per riportare quelle stesse cellule a uno stato anti-tumorale. Comprendere questo interruttore potrebbe aprire nuove strade per rendere più efficaci le terapie immunitarie esistenti.
Aiutanti immunitari amichevoli e ostili
I macrofagi sono globuli bianchi che normalmente difendono l’organismo e ripuliscono i tessuti danneggiati. In molti tumori, inclusa la LMA, possono essere “rieducati” a svolgere un ruolo protettivo che tutela le cellule tumorali invece di attaccarle. Questi macrofagi associati al tumore tendono ad assumere uno stato simile a M2, che attenua l’infiammazione e sostiene la sopravvivenza delle cellule neoplastiche, mentre lo stato M1 è più aggressivo e ostile al tumore. Gli autori si sono concentrati su come le cellule leucemiche influenzino questo equilibrio, chiedendosi quali segnali provenienti dalle cellule tumorali stesse inducano i macrofagi a diventare o aiutanti dannosi o combattenti utili.
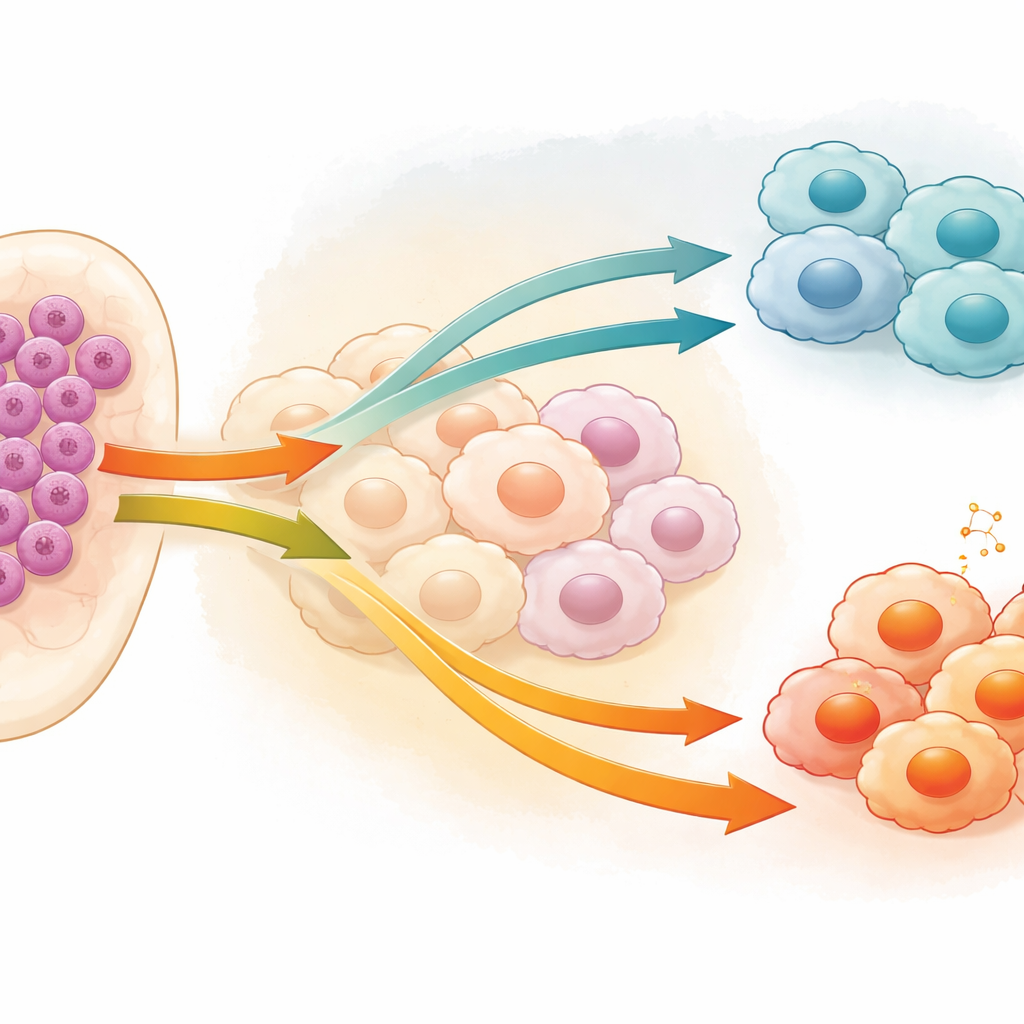
Una via di segnalazione nascosta all’interno delle cellule leucemiche
Il gruppo ha focalizzato l’attenzione su una proteina chiamata caspasi-1 (CASP1), nota soprattutto per il suo ruolo nella morte cellulare infiammatoria, ma il cui comportamento nel cancro è complesso e talvolta contraddittorio. Hanno scoperto che le cellule di LMA spesso presentano livelli elevati di CASP1 e che questo aumento è associato a una maggiore presenza di macrofagi di tipo M2 che supportano il tumore. Utilizzando due linee cellulari umane di LMA, hanno ridotto l’attività di CASP1 e raccolto il cocktail di molecole che queste cellule leucemiche modificate rilasciavano nell’ambiente. Quando questo mezzo condizionato è stato applicato a macrofagi coltivati in vitro, i macrofagi hanno mostrato meno caratteristiche M2 e più tratti associati allo stato M1, anti-tumorale. Questo cambiamento è emerso a livello genico, nei marcatori proteici sulla superficie cellulare e nel profilo complessivo delle popolazioni cellulari.
Scoprire un freno chiave: EGR4
Per capire come CASP1 all’interno delle cellule leucemiche potesse influenzare così marcatamente i macrofagi esterni, i ricercatori hanno analizzato l’attività genica globale dopo la riduzione di CASP1. Hanno scoperto che i livelli di un fattore di trascrizione chiamato EGR4 aumentavano drasticamente quando CASP1 veniva inattivata. Ulteriori test hanno confermato che EGR4 funziona come un freno molecolare sulla capacità delle cellule leucemiche di indirizzare i macrofagi verso lo stato M2. Quando gli scienziati hanno volutamente abbassato nuovamente EGR4 in cellule carenti di CASP1, il precedente cambiamento favorevole nel comportamento dei macrofagi è stato parzialmente annullato. Ciò indica che EGR4 è un attore a valle cruciale attraverso il quale CASP1 esercita i suoi effetti sul microambiente tumorale.
Come una via sposta l’equilibrio
Approfondendo, lo studio ha collegato l’accoppiamento CASP1–EGR4 a un’altra nota via di segnalazione, la via IL-10/STAT3, che favorisce fortemente i macrofagi di tipo M2, promotori del tumore. Quando CASP1 è stato ridotto nelle cellule leucemiche, i segnali che normalmente attivano questa via nei macrofagi vicini sono risultati attenuati, in particolare la molecola anti-infiammatoria IL-10 e il suo partner, STAT3 fosforilato. L’abbassamento di EGR4 ha annullato gran parte di questa attenuazione, sottolineandone ancora una volta il ruolo centrale. In topi impiantati con cellule umane di LMA, il blocco di CASP1 non solo ha rallentato la crescita tumorale, ma ha anche rimodellato il microambiente: i macrofagi si sono allontanati dalle caratteristiche M2, i marcatori di divisione cellulare sono diminuiti e i livelli di EGR4 sono aumentati, tutti segnali coerenti con un nicchia meno accogliente per le cellule leucemiche.
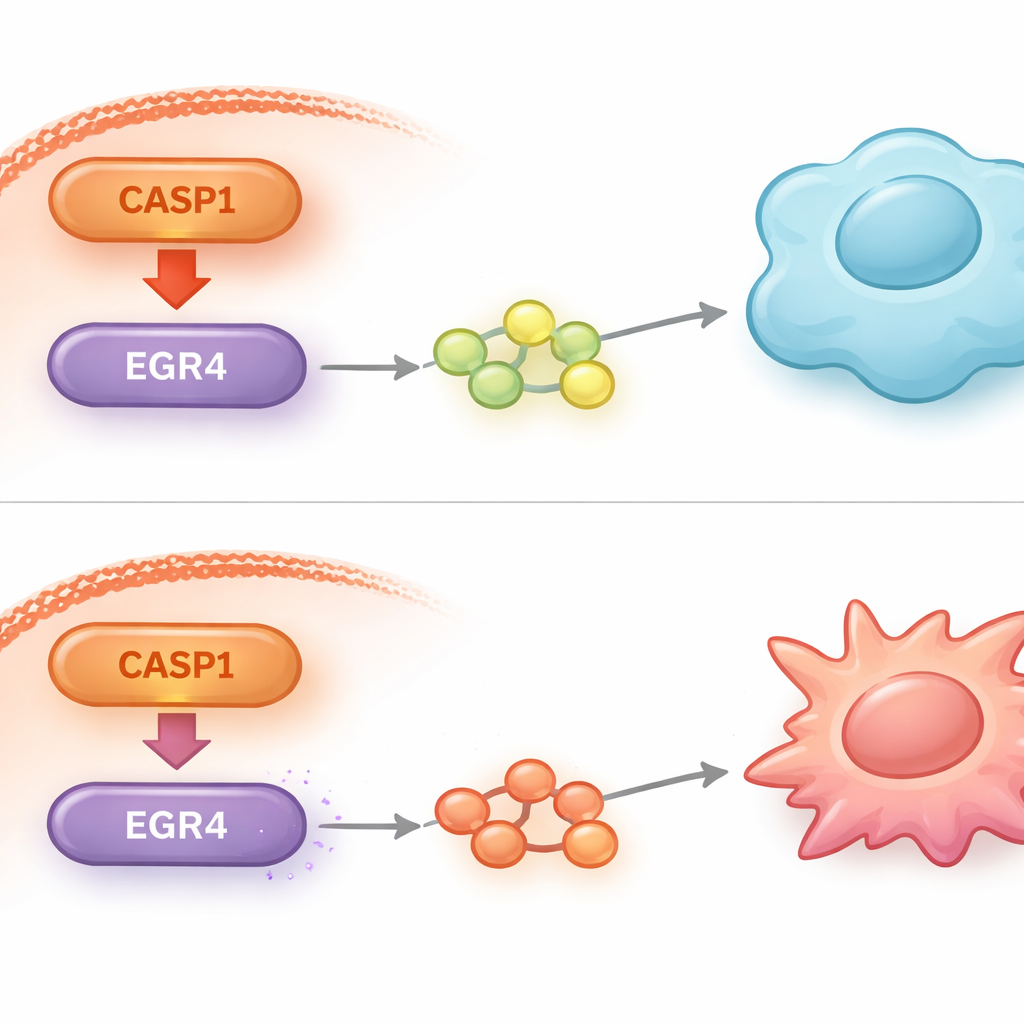
Cosa potrebbe significare per i trattamenti futuri
Per un lettore non specialista, la conclusione principale è che le cellule leucemiche non agiscono da sole: addestrano attivamente le cellule immunitarie vicine a proteggerle. Questo lavoro identifica una catena di comando specifica—CASP1 che controlla EGR4, il quale a sua volta modula i segnali che spingono i macrofagi verso un ruolo favorevole al tumore. Interrompere questa catena rende l’ambiente tumorale meno permissivo e rallenta la crescita del cancro negli animali. Poiché esistono già farmaci inibitori di CASP1 che sono stati testati nell’uomo per altre condizioni, la via CASP1–EGR4 offre un promettente punto di partenza per terapie mirate a risvegliare le difese immunitarie dell’organismo contro la LMA.
Citazione: Qian, Y., Chen, Y., Feng, ZX. et al. The Caspase-1-EGR4 axis regulates macrophage repolarization in acute myeloid leukemia cells. Sci Rep 16, 11319 (2026). https://doi.org/10.1038/s41598-026-41381-x
Parole chiave: leucemia mieloide acuta, microambiente tumorale, polarizzazione dei macrofagi, caspasi-1, segnalazione STAT3