Clear Sky Science · pl
TECs pozytywne na RASIP1 w gruczolakoraku trzustki: potencjalnie nowy typ komórek śródbłonka skorelowany z „gorącymi” nowotworami
Dlaczego naczynia krwionośne mają znaczenie w raku trzustki
Rak trzustki należy do najbardziej śmiertelnych nowotworów, częściowo dlatego, że własne mechanizmy obronne organizmu mają trudności z dotarciem i zaatakowaniem guza. W przeciwieństwie do niektórych nowotworów obfitujących w komórki odpornościowe i dobrze odpowiadających na współczesne immunoterapie, wiele guzów trzustki jest „zimnych” — ubogich w pomocne limfocyty T. W tym badaniu zbadano niespodziewanego sprzymierzeńca wewnątrz naczyń guza: szczególny rodzaj komórek wyściełających naczynia, który zdaje się przyciągać komórki T zwalczające raka, potencjalnie pomagając przemienić „zimny” guz w „gorący”, łatwiejszy do leczenia.
Bliższe spojrzenie na naczynia krwionośne guza
Naczynia krwionośne to więcej niż zwykłe rury. Wyścielone są komórkami śródbłonka, które decydują, co wchodzi i wychodzi z krwiobiegu, w tym komórki odpornościowe. Nowotwory trzustki zazwyczaj są słabo ukrwione, co tworzy barierę dla leków i komórek odpornościowych. Wykorzystując zaawansowane pojedynczokomórkowe sekwencjonowanie RNA — technikę odczytującą aktywność poszczególnych komórek — badacze zmapowali wiele typów komórek wewnątrz guzów trzustki. Potwierdzili, że normalne, zdrowe komórki naczyń stają się rzadsze w miarę postępu choroby, podczas gdy pozostałe komórki śródbłonka związane z guzem zmieniają swoje zachowanie i ekspresję genów.
Odkrycie pomocnego typu komórek naczyniowych
Wśród tych komórek naczyń guza zespół zidentyfikował odrębną podgrupę oznaczoną wysokim poziomem białka nazwanego RASIP1. Te nowotworowe komórki śródbłonka pozytywne na RASIP1 wykazywały bardzo inny profil genowy niż inne komórki naczyń. Były wzbogacone w geny zaangażowane w ułatwianie przejścia białych krwinek przez ścianę naczynia — kluczowy etap pozwalający limfocytom T opuścić krwiobieg i dostać się do guza. Pacjenci, których guzy wykazywały wyższą ekspresję RASIP1 w komórkach śródbłonka, mieli skłonność do dłuższego przeżycia, a sygnał ten nie odzwierciedlał po prostu zaawansowania choroby, co sugeruje, że sam ten szczególny stan naczyń może być korzystny.
Powiązanie specjalnych naczyń z immunologicznymi „gorącymi punktami”
Aby sprawdzić, gdzie te komórki występują w rzeczywistych guzach, badacze użyli transkryptomiki przestrzennej — technologii pokazującej, które geny są aktywne w precyzyjnych lokalizacjach na plasterku tkanki. Obszary bogate w komórki śródbłonka pozytywne na RASIP1 pokrywały się z regionami wykazującymi silne sygnały od aktywnych limfocytów T i interferonu gamma, charakterystycznego dla „gorących” nowotworów. W rzeczywistych wycinkach tkanki barwionych pod mikroskopem naczynia bogate w RASIP1 były otoczone gęstymi pierścieniami cytotoksycznych komórek T CD8 i komórek pozytywnych na Granzyme B, podczas gdy naczynia o niskim poziomie RASIP1 miały bardzo niewiele pobliskich komórek odpornościowych. Analizy dużych zestawów danych nowotworowych również powiązały wyższy poziom RASIP1 z lepszą odpowiedzią na niektóre immunoterapie.
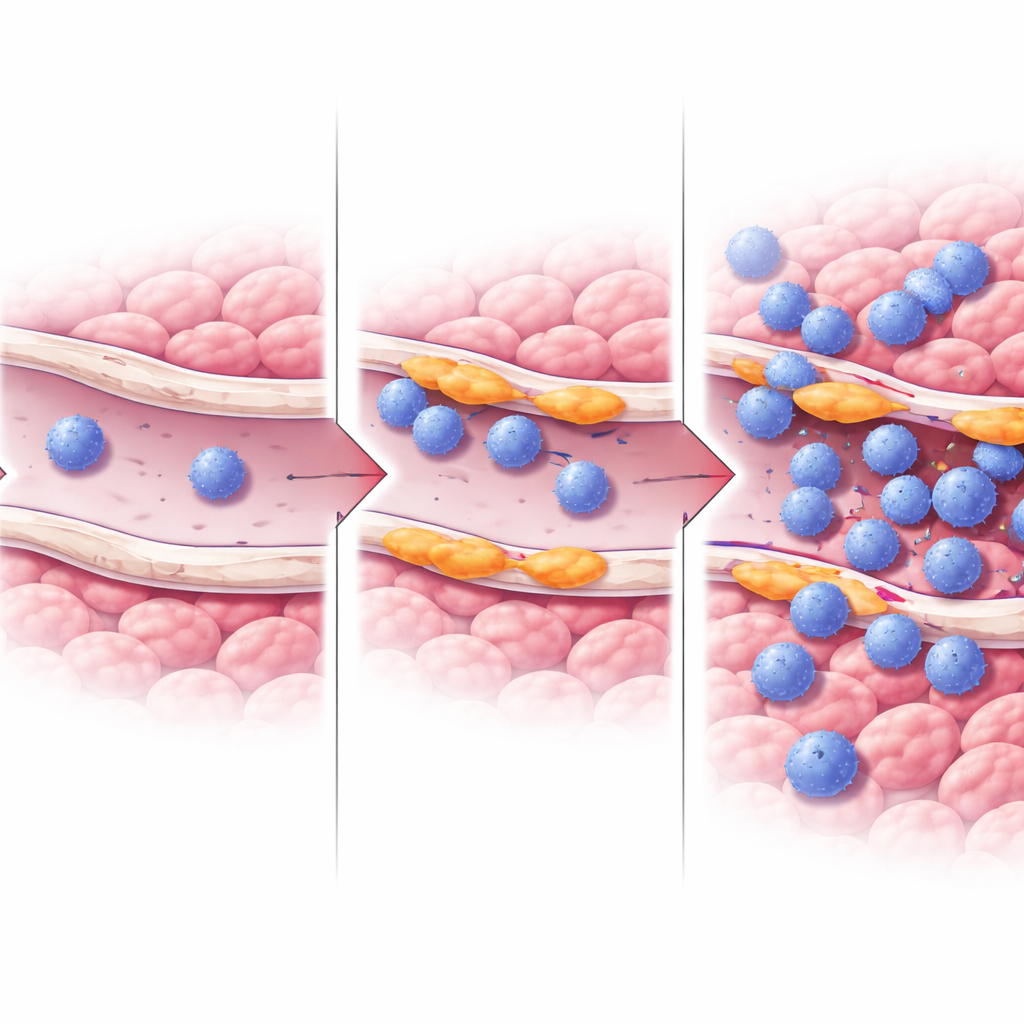
Jak te naczynia mogą pomagać limfocytom T w wnikaniu do guzów
Aby zbadać mechanizm, zespół zwrócił się do hodowanych ludzkich komórek śródbłonka i sztucznie zwiększał lub zmniejszał poziom RASIP1. Gdy zredukowano RASIP1, spadła ekspresja genów i białek zaangażowanych w przyciąganie i „przytrzymywanie” komórek odpornościowych, takich jak ICAM1 i inne białka stref kontaktu, a szlaki związane z aktywacją i ruchem limfocytów T zostały osłabione. Nadekspresja RASIP1 działała odwrotnie, zwiększając ICAM1. Praca wskazała również na zmiany w sygnalizacji ERK — kluczowej ścieżce komunikacyjnej wewnątrz komórek — jako część mechanizmu, dzięki któremu RASIP1 utrzymuje ten przyjazny limfocytom stan naczyń. Razem te eksperymenty wspierają hipotezę, że RASIP1 pomaga naczyniom tworzyć „platformy lądowania”, które pozwalają limfocytom T przyczepiać się, przeciskać przez ścianę naczynia i gromadzić się w guzie.
Co to może znaczyć dla przyszłych terapii
Mówiąc wprost, badanie sugeruje, że nie wszystkie naczynia nowotworowe są złe. Konkretna podgrupa oznaczona RASIP1 wydaje się działać jako brama umożliwiająca limfocytom T zabijającym komórki nowotworowe dostęp do guzów trzustki, a pacjenci z większą liczbą takich „bram” mają pozornie lepsze wyniki. Chociaż potrzebne są dalsze badania na modelach zwierzęcych i bezpośrednie testy funkcjonalne, wyniki rodzą intrygującą możliwość: zamiast jedynie prób odcięcia guza od unaczynienia, przyszłe terapie mogłyby także dążyć do pielęgnowania lub odtwarzania naczyń pozytywnych na RASIP1, aby „rozgrzać” guzy trzustki i zwiększyć skuteczność immunoterapii.
Cytowanie: Zhang, S., He, Y., Chang, H. et al. RASIP1-positive TECs in pancreatic adenocarcinoma: a potential novel type of endothelial cells correlated with “hot” tumors. Sci Rep 16, 11946 (2026). https://doi.org/10.1038/s41598-026-40948-y
Słowa kluczowe: rak trzustki, naczynia krwionośne guza, immunoterapia, infiltracja limfocytów T, mikrosrodowisko guza