Clear Sky Science · fr
Cellules endothéliales RASIP1-positives dans l’adénocarcinome pancréatique : un nouveau type potentiel de cellules endothéliales corrélé aux tumeurs « chaudes »
Pourquoi les vaisseaux sanguins sont importants dans le cancer du pancréas
Le cancer du pancréas est l’un des cancers les plus meurtriers, en partie parce que les défenses immunitaires de l’organisme peinent à atteindre et attaquer la tumeur. Contrairement à certains cancers riches en cellules immunitaires et réceptifs aux immunothérapies modernes, de nombreuses tumeurs pancréatiques sont « froides » — pauvres en lymphocytes T efficaces. Cette étude explore un allié inattendu à l’intérieur des vaisseaux tumoraux : un type particulier de cellule qui tapisse les vaisseaux et semble favoriser l’entrée des lymphocytes T anti-cancer, aidant potentiellement à transformer une tumeur « froide » en une tumeur « chaude » plus facile à traiter.
Un examen approfondi des vaisseaux tumoraux
Les vaisseaux sanguins ne sont pas de simples conduits. Ils sont tapissés par des cellules endothéliales qui régulent ce qui entre et sort du flux sanguin, y compris les cellules immunitaires. Les tumeurs pancréatiques sont généralement peu vascularisées, ce qui crée une barrière aux médicaments et aux cellules immunitaires. Grâce au séquençage ARN unicellulaire avancé — une technique qui lit l’activité des cellules individuelles — les chercheurs ont cartographié de nombreux types cellulaires au sein des tumeurs pancréatiques. Ils ont confirmé que les cellules vasculaires normales et saines deviennent plus rares à mesure que le cancer progresse, tandis que les cellules endothéliales associées à la tumeur modifient leur comportement et leur activité génique.
Découverte d’un type utile de cellule vasculaire
Parmi ces cellules des vaisseaux tumoraux, l’équipe a identifié un sous-groupe distinct marqué par des niveaux élevés d’une protéine appelée RASIP1. Ces cellules endothéliales tumorales RASIP1-positives présentaient un profil génique très différent de celui des autres cellules vasculaires. Elles étaient enrichies en gènes impliqués dans le passage des globules blancs à travers la paroi vasculaire — une étape cruciale qui permet aux lymphocytes T de quitter la circulation et de pénétrer dans la tumeur. Les patients dont les tumeurs présentaient une expression plus élevée de RASIP1 dans les cellules endothéliales avaient tendance à vivre plus longtemps, et ce signal ne se limitait pas à refléter le stade de leur cancer, ce qui suggère que cet état particulier des vaisseaux pourrait être bénéfique en soi.
Relier ces vaisseaux spéciaux aux « points chauds » immunitaires
Pour localiser ces cellules dans de vraies tumeurs, les chercheurs ont utilisé la transcriptomique spatiale, une technologie qui révèle quels gènes sont actifs à des emplacements précis d’une coupe tissulaire. Les zones riches en cellules endothéliales RASIP1-positives coïncidaient avec des régions présentant de forts signes d’activité des lymphocytes T et d’interféron-gamma, une molécule emblématique des tumeurs « chaudes ». Dans des sections de tissus de patients colorées au microscope, les vaisseaux riches en RASIP1 étaient entourés d’anneaux denses de cellules T cytotoxiques CD8 et Granzyme B-positives, tandis que les vaisseaux avec peu de RASIP1 avaient très peu de cellules immunitaires à proximité. Des analyses sur de larges jeux de données cancéreuses ont également associé des niveaux plus élevés de RASIP1 à de meilleures réponses à certaines immunothérapies.
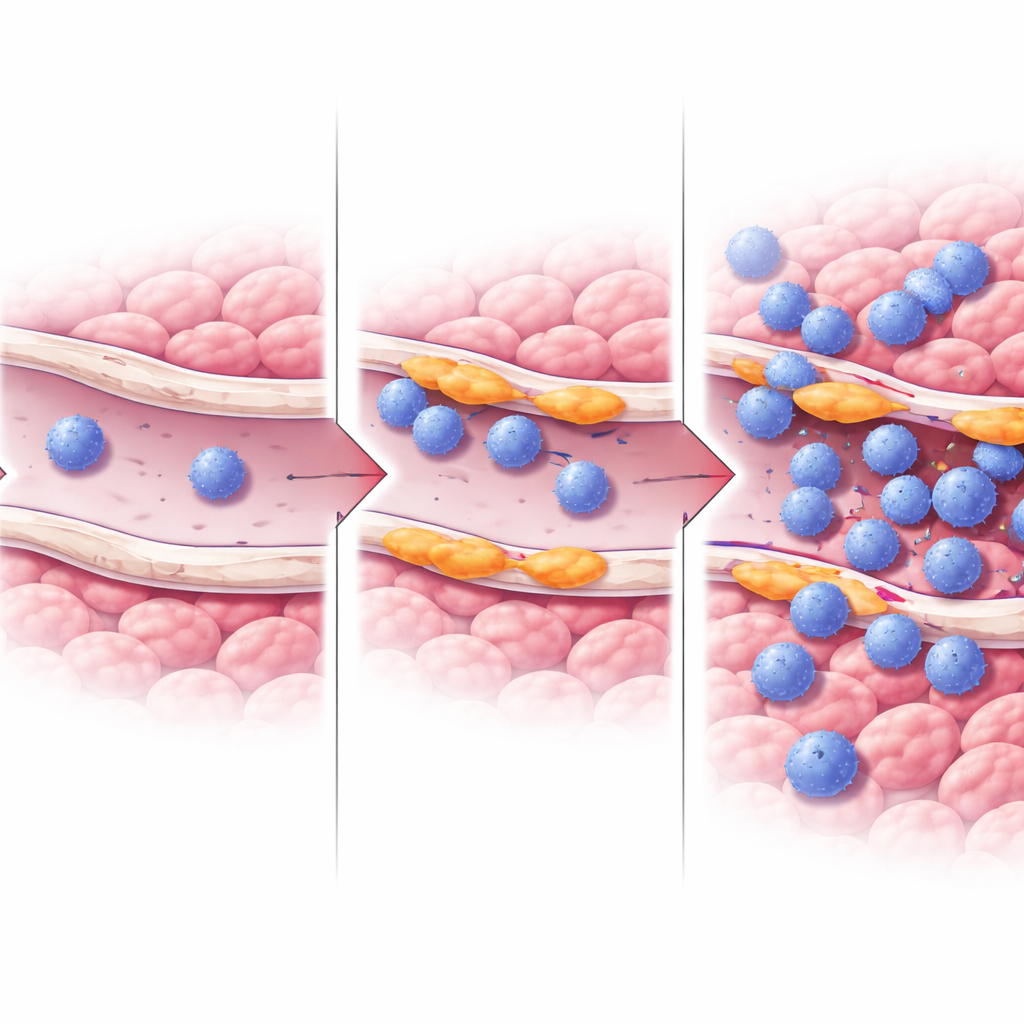
Comment ces vaisseaux pourraient aider les lymphocytes T à pénétrer dans les tumeurs
Pour étudier le mécanisme, l’équipe a utilisé des cellules endothéliales humaines en culture et a modulé artificiellement l’expression de RASIP1. Lorsqu’ils ont réduit RASIP1, les gènes et protéines impliqués dans l’attraction et l’adhérence des cellules immunitaires, tels qu’ICAM1 et d’autres molécules de jonction, ont diminué, et les voies liées à l’activation et à la migration des lymphocytes T ont été atténuées. La surexpression de RASIP1 a produit l’effet inverse, augmentant ICAM1. Les travaux ont également pointé des modifications de la signalisation ERK, une voie de communication intracellulaire clé, comme faisant partie du mécanisme par lequel RASIP1 maintient cet état vasculaire favorable aux lymphocytes T. Ensemble, ces expériences soutiennent l’idée que RASIP1 aide les vaisseaux à former des « plateformes d’atterrissage » permettant aux lymphocytes T de s’accrocher, de se faufiler à travers la paroi vasculaire et de s’accumuler dans la tumeur.
Ce que cela pourrait signifier pour les traitements futurs
En termes simples, cette étude suggère que tous les vaisseaux tumoraux ne sont pas nécessairement nuisibles. Un sous-ensemble spécifique, marqué par RASIP1, semble agir comme une porte d’entrée permettant aux lymphocytes T tueurs de cancer de pénétrer dans les tumeurs pancréatiques, et les patients qui disposent de davantage de ces vaisseaux semblent s’en sortir mieux. Bien que des travaux supplémentaires sur des modèles animaux et des tests fonctionnels directs soient nécessaires, ces résultats ouvrent une possibilité intrigante : au lieu de se contenter de couper l’approvisionnement sanguin de la tumeur, les thérapies futures pourraient aussi viser à favoriser ou recréer des vaisseaux RASIP1-positifs pour « réchauffer » les tumeurs pancréatiques et rendre les immunothérapies plus efficaces.
Citation: Zhang, S., He, Y., Chang, H. et al. RASIP1-positive TECs in pancreatic adenocarcinoma: a potential novel type of endothelial cells correlated with “hot” tumors. Sci Rep 16, 11946 (2026). https://doi.org/10.1038/s41598-026-40948-y
Mots-clés: cancer du pancréas, vaisseaux tumoraux, immunothérapie, infiltration des lymphocytes T, microenvironnement tumoral