Clear Sky Science · de
RASIP1-positive TECs im Pankreasadenokarzinom: ein potenziell neuer Endothelzelltyp, der mit „heißen“ Tumoren korreliert
Warum Blutgefäße bei Pankreaskrebs wichtig sind
Pankreaskrebs gehört zu den tödlichsten Krebsarten, mitunter weil die körpereigenen Abwehrkräfte den Tumor nur schwer erreichen und angreifen können. Anders als manche Tumoren, die reich an Immunzellen sind und gut auf moderne Immuntherapien ansprechen, sind viele Pankreastumoren „kalt“ — arm an hilfreichen T‑Zellen. Diese Studie untersucht einen unerwarteten Verbündeten in den Tumorblutgefäßen: einen speziellen Typ von gefäßauskleidenden Zellen, der offenbar krebsbekämpfende T‑Zellen anzieht und so dazu beitragen könnte, einen „kalten“ Tumor in einen „heißen“ umzuwandeln, der sich leichter behandeln lässt.
Ein genauerer Blick auf Tumorblutgefäße
Blutgefäße sind mehr als einfache Rohre. Sie sind von Endothelzellen ausgekleidet, die entscheiden, was in den Blutkreislauf gelangt und ihn verlässt — darunter auch Immunzellen. Pankreastumoren sind meist schlecht durchblutet, was sowohl für Medikamente als auch für Immunzellen eine Barriere darstellt. Mithilfe hochauflösender Einzelzell‑RNA‑Sequenzierung — einer Methode, die die Aktivität einzelner Zellen ausliest — kartierten die Forschenden viele Zelltypen innerhalb von Pankreastumoren. Sie bestätigten, dass normale, gesunde Gefäßzellen mit dem Fortschreiten des Krebses seltener werden, während die verbleibenden tumorassoziierten Endothelzellen ihr Verhalten und ihre Genaktivität verändern.
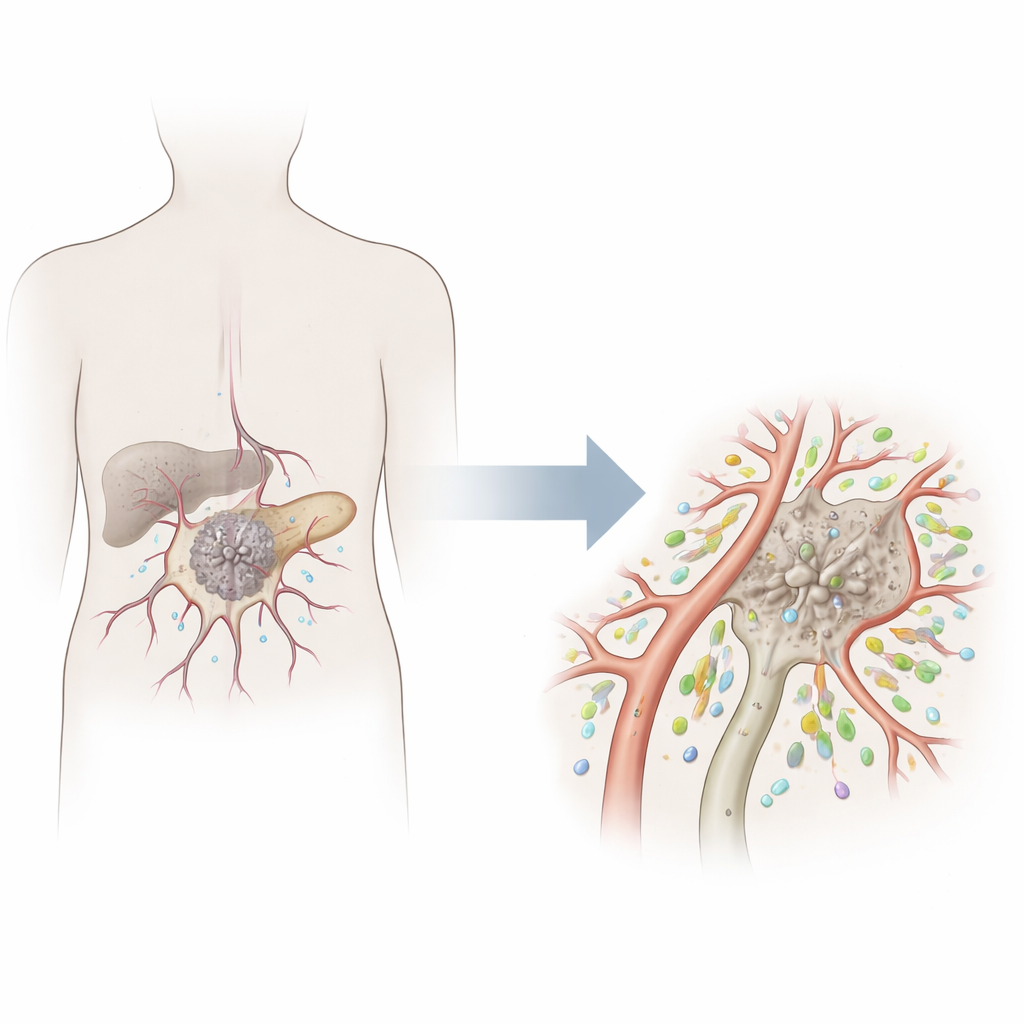
Entdeckung eines hilfreichen Gefäßzelltyps
Unter diesen Tumorblutgefäßzellen identifizierte das Team eine eigenständige Untergruppe, die durch hohe Mengen eines Proteins namens RASIP1 gekennzeichnet ist. Diese RASIP1‑positiven tumorassoziierten Endothelzellen wiesen ein sehr unterschiedliches Genprofil gegenüber anderen Gefäßzellen auf. Sie waren angereichert an Genen, die daran beteiligt sind, weiße Blutkörperchen über die Gefäßwand zu lassen — ein kritischer Schritt, damit T‑Zellen den Blutstrom verlassen und in den Tumor eindringen können. Patientinnen und Patienten, deren Tumoren höhere RASIP1‑Expression in Endothelzellen zeigten, lebten tendenziell länger; dieses Signal spiegelte nicht einfach nur das Tumorstadium wider, was darauf hindeutet, dass dieser besondere Gefäßzustand selbst vorteilhaft sein könnte.
Verknüpfung spezieller Gefäße mit immunologischen „Hotspots“
Um zu sehen, wo diese Zellen in echten Tumoren lokalisiert sind, nutzten die Forschenden räumliche Transkriptomik, eine Technik, die zeigt, welche Gene an präzisen Stellen eines Gewebes aktiv sind. Bereiche mit vielen RASIP1‑positiven Endothelzellen überlappten mit Regionen, die starke Signale aktiver T‑Zellen und Interferon‑Gamma zeigten — ein Kennzeichen „heißer“ Tumoren. In Patientenproben, die mikroskopisch gefärbt wurden, waren Gefäße mit hoher RASIP1‑Expression von dichten Ringen aus CD8‑ und Granzyme‑B‑positiven zytotoxischen T‑Zellen umgeben, während Gefäße mit wenig RASIP1 kaum nahegelegene Immunzellen aufwiesen. Analysen großer Krebsdatensätze verbanden zudem höhere RASIP1‑Werte mit besseren Ansprechraten auf bestimmte Immuntherapien.
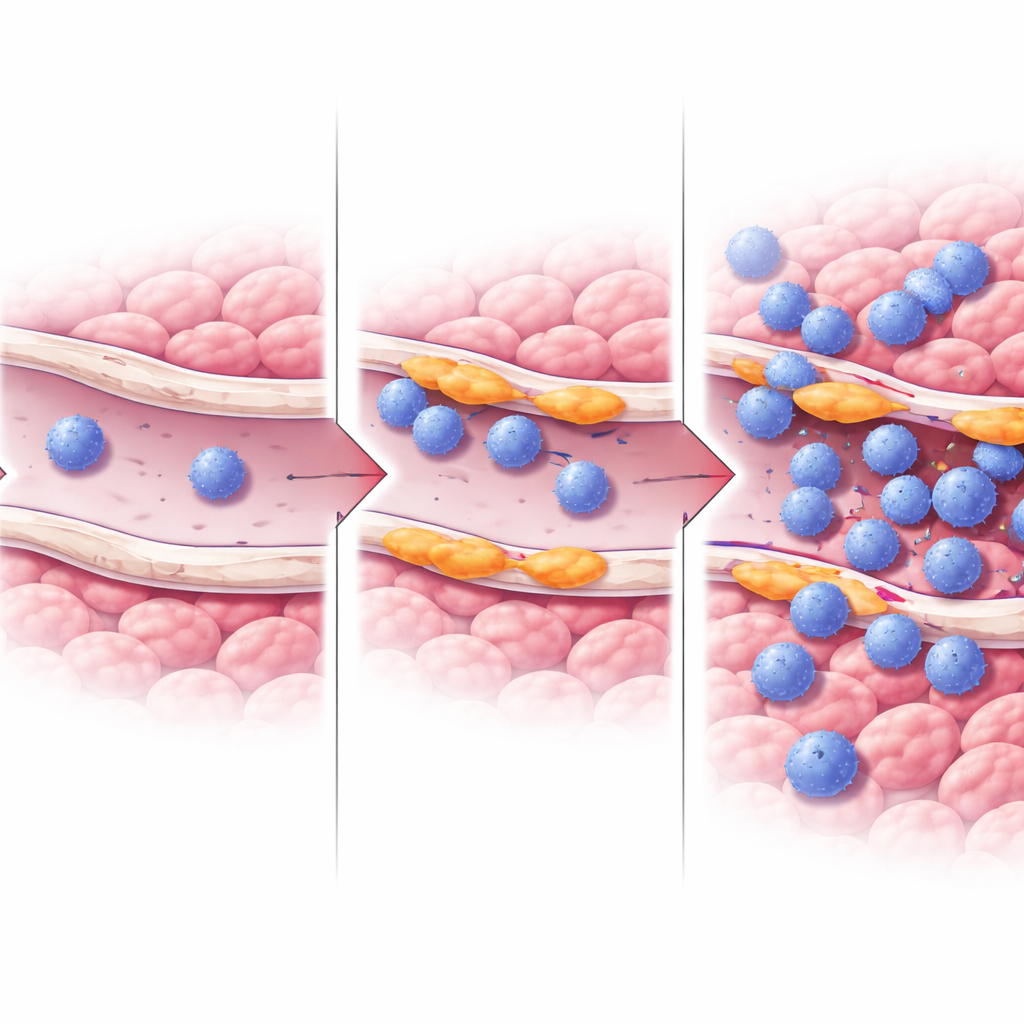
Wie diese Gefäße T‑Zellen das Eindringen in Tumoren erleichtern könnten
Um den Mechanismus zu untersuchen, arbeiteten die Forschenden mit kultivierten humanen Endothelzellen und steigerten oder senkten künstlich die RASIP1‑Expression. Bei Reduktion von RASIP1 gingen Gene und Proteine zurück, die Immunzellen anziehen und festhalten — etwa ICAM1 und weitere Junction‑Moleküle — und Signalwege, die mit T‑Zell‑Aktivierung und Bewegung zusammenhängen, wurden abgeschwächt. Die Überexpression von RASIP1 zeigte den umgekehrten Effekt und steigerte unter anderem ICAM1. Die Arbeit deutet außerdem auf Veränderungen in der ERK‑Signalübertragung hin, einem zentralen intrazellulären Kommunikationsweg, als Teil dessen, wie RASIP1 diesen T‑Zell‑freundlichen Gefäßzustand aufrechterhält. Zusammen stützen diese Experimente die Idee, dass RASIP1 Gefäße zu „Landeflächen“ formt, die es T‑Zellen ermöglichen, anzudocken, sich durch die Gefäßwand zu quetschen und sich im Tumor anzusammeln.
Was das für zukünftige Behandlungen bedeuten könnte
Vereinfacht gesagt legt diese Studie nahe, dass nicht alle Tumorblutgefäße schädlich sind. Eine spezifische Untergruppe, gekennzeichnet durch RASIP1, scheint als Tor zu fungieren, das krebsvernichtenden T‑Zellen den Zutritt zu Pankreastumoren ermöglicht; Patientinnen und Patienten mit mehr dieser Tor‑Gefäße scheinen besser abzuschneiden. Obwohl weitere Arbeiten in Tiermodellen und direkte funktionelle Tests nötig sind, eröffnen die Befunde eine interessante Möglichkeit: Anstatt nur darauf zu zielen, die Blutversorgung eines Tumors zu kappen, könnten künftige Therapien auch darauf abzielen, RASIP1‑positive Gefäße zu fördern oder nachzubilden, um Pankreastumoren „aufzuwärmen“ und Immuntherapien wirksamer zu machen.
Zitation: Zhang, S., He, Y., Chang, H. et al. RASIP1-positive TECs in pancreatic adenocarcinoma: a potential novel type of endothelial cells correlated with “hot” tumors. Sci Rep 16, 11946 (2026). https://doi.org/10.1038/s41598-026-40948-y
Schlüsselwörter: Pankreaskrebs, Tumorblutgefäße, Immuntherapie, T‑Zell‑Infiltration, Tumormikroumgebung