Clear Sky Science · pl
Ulepszanie diagnozy ostrej białaczki limfoblastycznej dzięki sieci VGG19 z modułem uwagi CBAM
Dlaczego szybsze badania krwi mają znaczenie
Ostra białaczka limfoblastyczna (ALL) to agresywny nowotwór krwi, który w ciągu kilku tygodni może stać się zagrażający życiu, jeśli nie zostanie szybko wykryty i leczony. Obecnie lekarze często diagnozują ALL, oglądając komórki ze szpiku i krwi pod mikroskopem — to uważne, czasochłonne zadanie, które w dużym stopniu zależy od doświadczenia specjalistów. W badaniu analizowano, czy dostosowana forma sztucznej inteligencji (AI) może pomóc lekarzom szybciej i bardziej konsekwentnie wykrywać ALL i jego podtypy na podstawie obrazów mikroskopowych, przyspieszając opiekę, a jednocześnie pozostawiając specjalistów w roli decydującej.
Bliższe spojrzenie na dziecięcy nowotwór krwi
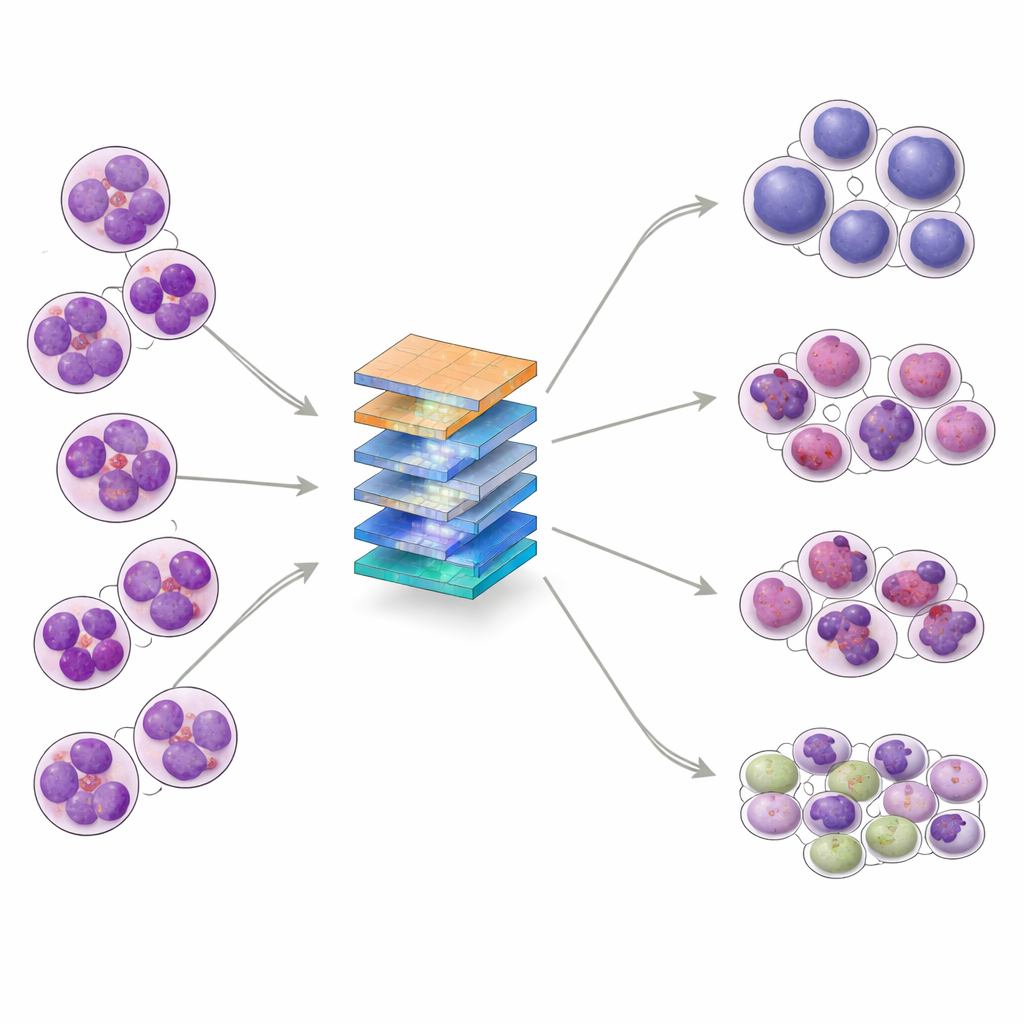
ALL rozwija się, gdy niedojrzałe białe krwinki, zwane limfoblastami, rozmnażają się niekontrolowanie w szpiku kostnym i przedostają się do krwiobiegu. Te nieprawidłowe komórki wypierają zdrowe elementy krwi i mogą szerzyć się do układu nerwowego. ALL jest najczęstszym nowotworem u dzieci, choć występuje też u dorosłych. Pod mikroskopem specjaliści dzielą ALL na trzy główne podtypy — L1, L2 i L3 — na podstawie rozmiaru i kształtu komórek, struktury materiału genetycznego oraz wyglądu otaczającego płynu. Rozróżnienie tych podtypów oraz odróżnienie ich od zdrowego szpiku jest ważne dla wyboru leczenia, jednak nawet eksperci mają trudności, gdy wygląd komórek jest bardzo podobny.
Nauczanie komputerów widzenia podobnego do ekspertów
Naukowcy postanowili zbudować system AI, który potrafi klasyfikować obrazy szpiku kostnego do czterech grup: trzech podtypów ALL oraz próbki normalne (bez białaczki). Zebrali 328 zdjęć o wysokim powiększeniu z laboratorium klinicznego w Pakistanie, obejmujących pacjentów w wieku 10–45 lat, a następnie zastosowali techniki augmentacji danych — takie jak rotacja, odbicia i subtelne zmiany jasności lub kontrastu — aby uzyskać 1 585 różnorodnych przykładów treningowych, zachowując przy tym kluczowe struktury komórek. Zestaw danych podzielono na zbiory treningowy, walidacyjny i testowy oraz przeanalizowano za pomocą narzędzi statystycznych, które wykazały złożone zachodzenie klas na siebie, podkreślając, że zadanie nie jest trywialne nawet dla zaawansowanych algorytmów.
Jak nowy model AI zwraca uwagę
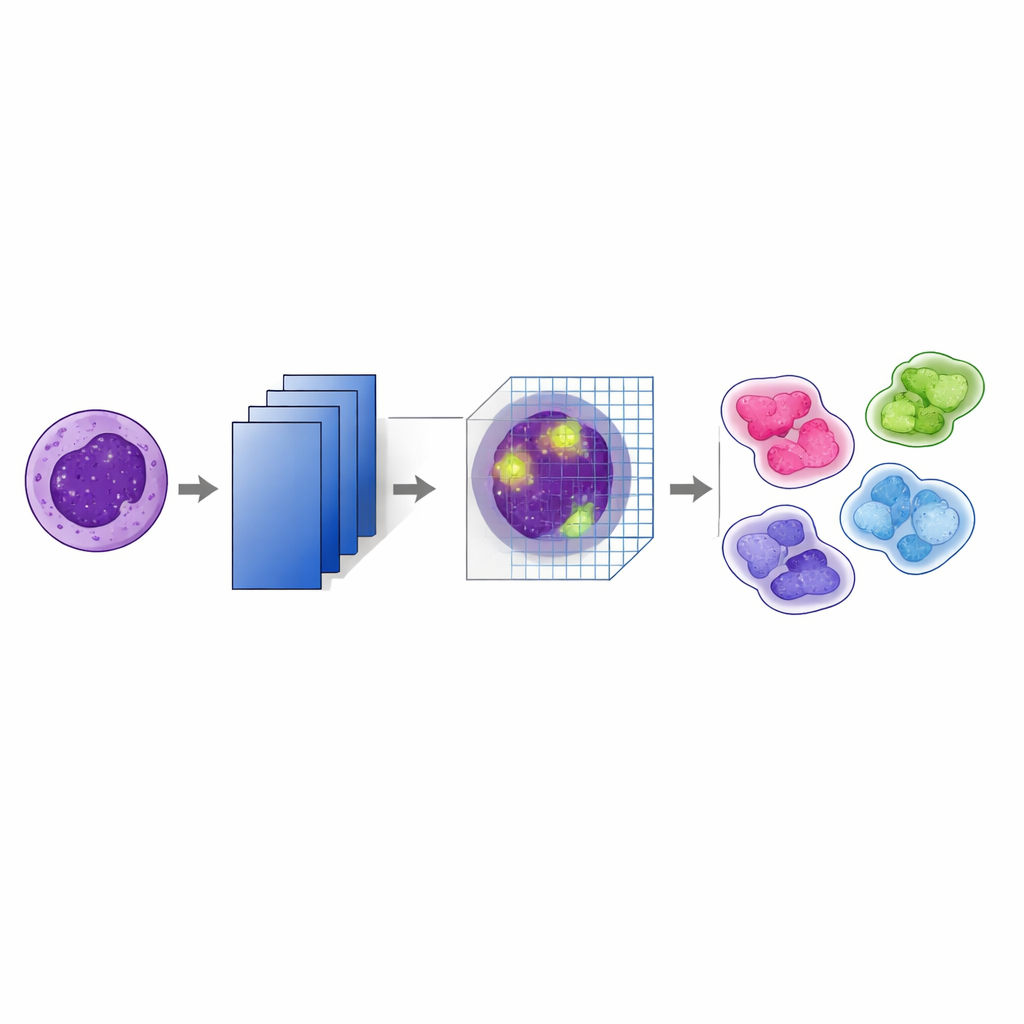
W centrum badania znajduje się zmodyfikowana wersja dobrze znanej sieci rozpoznawania obrazów VGG19. Autorzy dodali do niej „moduł uwagi bloków konwolucyjnych” (CBAM) po każdym większym kroku agregacji (poolingu). W prostych słowach model najpierw uczy się wielu warstwowych cech obrazów, a następnie mechanizm uwagi decyduje, które cechy i które obszary na obrazie zasługują na większą wagę. Jedna część mechanizmu uwagi podkreśla najbardziej informacyjne kanały — wzorce takie jak krawędzie jąder czy wewnętrzna tekstura — podczas gdy inna część wskazuje najważniejsze lokalizacje wewnątrz komórki. Stosując te kroki uwagi na różnych głębokościach sieci, system śledzi subtelne wskazówki wizualne, które pomagają rozróżnić na przykład blisko spokrewnione podtypy białaczki.
Jak dobrze działa system
Model VGG19 ze zintegrowanym CBAM porównano z kilkoma popularnymi architekturami głębokiego uczenia, w tym DenseNet, Inception, MobileNet oraz oryginalnym VGG19. Stosując standardowe miary wydajności, nowy model osiągnął ogólną dokładność 98,73%, co jest o około 5,7 punktu procentowego więcej niż VGG19 bez modułu uwagi i lepszym wynikiem niż wszystkie konkurencyjne modele na tych samych danych. Szczegółowe wyniki wykazały wysoką precyzję i czułość we wszystkich czterech klasach, w tym rzadkim podtypie L3, a krzywe charakterystyki odbiornika (ROC) były bliskie idealnym. Zespół przeprowadził również walidację krzyżową k‑fold — trenowanie i testowanie na wielu podziałach danych — aby sprawdzić stabilność wyników, oraz eksperymenty „ablacyjne”, które pokazały, że użycie zarówno uwagi kanałowej, jak i przestrzennej na wielu etapach było kluczowe dla uzyskanych korzyści.
Co to może znaczyć dla pacjentów i lekarzy
Choć wyniki są obiecujące, autorzy podkreślają, że system nie jest jeszcze gotowy, by zastąpić ekspertów ani być stosowany samodzielnie w klinice. Badanie opiera się na stosunkowo niewielkim, jednocentrowym zbiorze danych i brakuje niezależnych testów wieloszpitalnych, które potwierdziłyby, że model działa równie dobrze w różnych warunkach i populacjach. Mimo to praca pokazuje, że starannie zaprojektowane mechanizmy uwagi mogą pomóc AI skupić się na tych samych drobnych detalach wizualnych, z których korzystają patolodzy oceniający preparaty ze szpiku. W przyszłości podobne systemy, zwalidowane na znacznie większych i bardziej zróżnicowanych zbiorach danych, mogłyby służyć jako narzędzia wspomagające decyzje — szybko wskazując podejrzane przypadki, sugerując prawdopodobne podtypy ALL i pokazując mapy cieplne regionów wpływających na predykcje — tak aby lekarze mogli stawiać szybsze i pewniejsze diagnozy.
Cytowanie: Rahman, S.I.U., Abbas, N., Ali, S. et al. Improving acute lymphoblastic leukemia diagnosis through CBAM-enhanced VGG19 deep learning. Sci Rep 16, 11027 (2026). https://doi.org/10.1038/s41598-026-40184-4
Słowa kluczowe: ostra białaczka limfoblastyczna, Sztuczna inteligencja w obrazowaniu medycznym, diagnoza za pomocą głębokiego uczenia, mechanizmy uwagi, mikroskopia szpiku kostnego