Clear Sky Science · fr
Améliorer le diagnostic de la leucémie lymphoblastique aiguë grâce à l’apprentissage profond VGG19 enrichi par CBAM
Pourquoi accélérer les dépistages du cancer du sang est important
La leucémie lymphoblastique aiguë (LLA) est un cancer du sang agressif qui peut devenir mortel en quelques semaines si elle n’est pas détectée et traitée rapidement. Aujourd’hui, les médecins diagnostiquent souvent la LLA en examinant la moelle osseuse et les cellules sanguines au microscope — une tâche minutieuse et longue qui dépend fortement du jugement d’experts. Cette étude examine comment une forme adaptée d’intelligence artificielle (IA) pourrait aider les cliniciens à repérer la LLA et ses sous‑types plus rapidement et de façon plus cohérente à partir d’images microscopiques, accélérant potentiellement la prise en charge tout en maintenant les spécialistes aux commandes.
Un regard plus précis sur un cancer infantile du sang
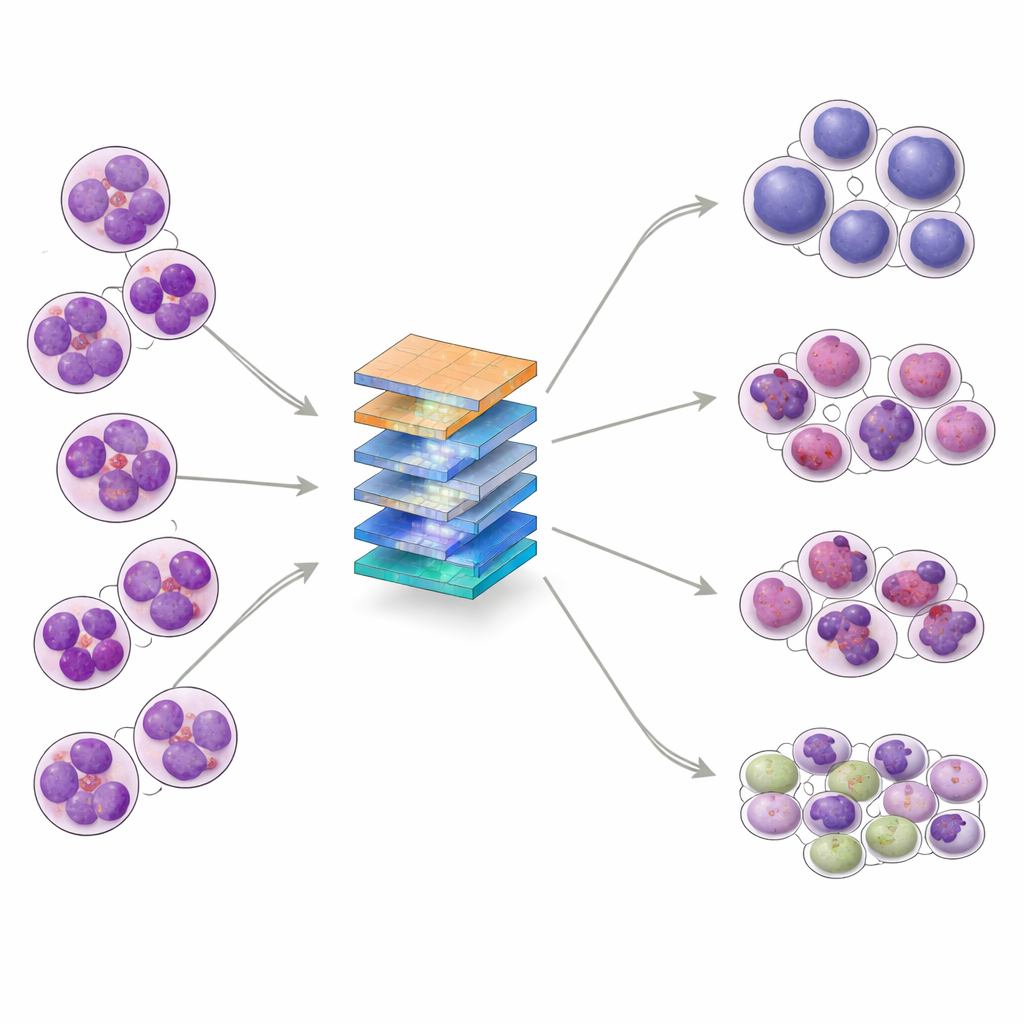
La LLA survient lorsque des globules blancs immatures, appelés lymphoblastes, prolifèrent de façon incontrôlée dans la moelle osseuse et passent dans la circulation sanguine. Ces cellules anormales remplacent les cellules sanguines saines et peuvent se propager au système nerveux. La LLA est le cancer le plus fréquent chez l’enfant, mais elle touche aussi des adultes. Au microscope, les spécialistes répartissent la LLA en trois sous‑types principaux — L1, L2 et L3 — en fonction de la taille et de la forme des cellules, de l’aspect de leur matériel génétique et de l’apparence du milieu environnant. Distinguer ces sous‑types, et les séparer d’une moelle osseuse normale, est important pour choisir le traitement, mais même les experts peuvent être confrontés à des difficultés quand les apparences cellulaires sont très similaires.
Apprendre aux ordinateurs à voir comme les experts
Les chercheurs ont cherché à construire un système d’IA capable de classer les images de moelle osseuse en quatre groupes : les trois sous‑types de LLA et des échantillons normaux (non leucémiques). Ils ont rassemblé 328 images en fort grossissement dans un laboratoire clinique au Pakistan, couvrant des patients âgés de 10 à 45 ans, puis ont utilisé des techniques d’augmentation des données — telles que la rotation, le retournement et des ajustements subtils de la luminosité ou du contraste — pour créer 1 585 exemples d’entraînement variés tout en préservant les structures cellulaires clés. Le jeu de données a été divisé en ensembles d’entraînement, de validation et de test, puis analysé avec des outils statistiques montrant que les classes se chevauchent de manière complexe, ce qui confirme que la tâche n’est pas triviale même pour des algorithmes avancés.
Comment le nouveau modèle d’IA « fait attention »
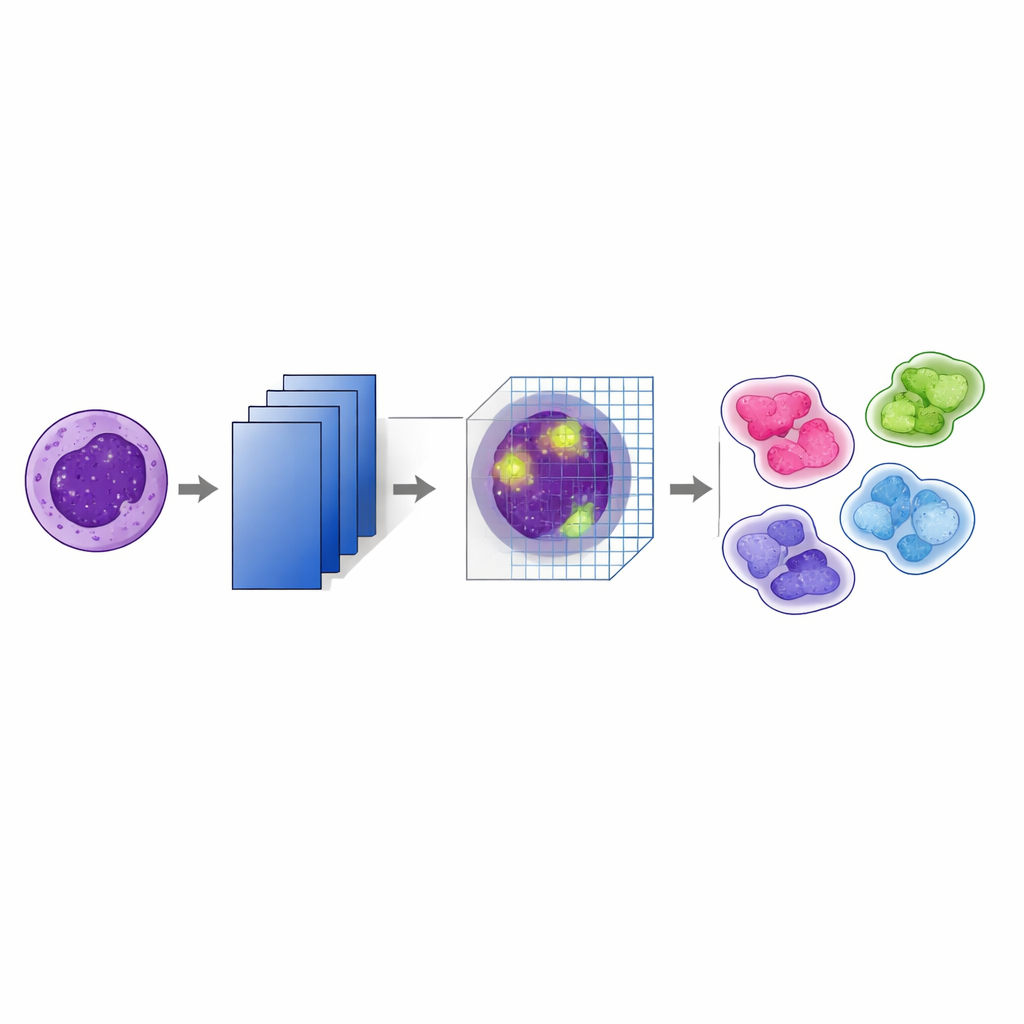
Au cœur de l’étude se trouve une version modifiée d’un réseau de reconnaissance d’images bien connu, le VGG19. Les auteurs y ont ajouté un « module d’attention par blocs convolutionnels » (CBAM) après chaque étape majeure de mise en commun (pooling). En termes simples, le modèle apprend d’abord de nombreuses caractéristiques superposées à partir des images, puis utilise l’attention pour décider quelles caractéristiques et quelles régions de chaque image méritent plus de poids. Une partie du mécanisme d’attention met l’accent sur les canaux les plus informatifs — des motifs comme les bords nucléaires ou la texture interne — tandis qu’une autre partie souligne les emplacements les plus importants à l’intérieur de la cellule. En empilant ces étapes d’attention à plusieurs profondeurs du réseau, le système suit des indices visuels subtils qui aident à distinguer, par exemple, des sous‑types de leucémie très proches.
Performances du système
Le modèle VGG19 enrichi par CBAM a été testé face à plusieurs architectures d’apprentissage profond populaires, notamment DenseNet, Inception, MobileNet et le VGG19 original. En utilisant des mesures de performance standard, le nouveau modèle a atteint une précision globale de 98,73 %, soit environ 5,7 points de pourcentage de plus que le VGG19 sans attention et de meilleures performances que tous les modèles concurrents sur les mêmes données. Les résultats détaillés ont montré une forte précision et un bon rappel pour les quatre classes, y compris le rare sous‑type L3, et les courbes ROC étaient proches de l’idéal. L’équipe a également réalisé une validation croisée en k‑fold — entraînement et test sur plusieurs découpages des données — pour vérifier la stabilité des résultats, et mené des expériences d’« ablation » démontrant que l’utilisation conjointe de l’attention par canal et spatiale à plusieurs niveaux était cruciale pour les gains observés.
Que cela signifie pour les patients et les médecins
Si les chiffres sont prometteurs, les auteurs soulignent que ce système n’est pas prêt à remplacer les experts humains ni à être utilisé seul en clinique. L’étude s’appuie sur un jeu de données relativement petit et monocentrique, et il n’existe pas de test indépendant multi‑hôpitaux prouvant que le modèle fonctionne de la même façon dans des contextes ou des populations différentes. Néanmoins, le travail montre que des mécanismes d’attention soigneusement conçus peuvent aider l’IA à se concentrer sur les mêmes détails visuels fins que les pathologistes utilisent lorsqu’ils lisent des lames de moelle osseuse. À l’avenir, des systèmes similaires, validés sur des jeux de données beaucoup plus larges et diversifiés, pourraient servir d’outils d’aide à la décision — signalant rapidement les cas suspects, suggérant les sous‑types probables de LLA et affichant des cartes thermiques des régions ayant influencé leurs prédictions — afin que les médecins puissent poser des diagnostics plus rapides et plus sûrs.
Citation: Rahman, S.I.U., Abbas, N., Ali, S. et al. Improving acute lymphoblastic leukemia diagnosis through CBAM-enhanced VGG19 deep learning. Sci Rep 16, 11027 (2026). https://doi.org/10.1038/s41598-026-40184-4
Mots-clés: leucémie lymphoblastique aiguë, IA pour l’imagerie médicale, diagnostic par apprentissage profond, mécanismes d’attention, microscopie de la moelle osseuse