Clear Sky Science · nl
Verbetering van de diagnose van acute lymfatische leukemie door CBAM-verrijkte VGG19 deep learning
Waarom snellere controles op bloedkanker ertoe doen
Acute lymfatische leukemie (ALL) is een agressieve bloedkanker die binnen enkele weken levensbedreigend kan worden als ze niet snel wordt opgespoord en behandeld. Tegenwoordig stellen artsen vaak een ALL‑diagnose door beenmerg- en bloedcellen onder de microscoop te bekijken — een zorgvuldig, tijdrovend werk dat sterk afhankelijk is van specialistisch oordeel. Deze studie onderzoekt hoe een aangepaste vorm van kunstmatige intelligentie (AI) artsen kan helpen ALL en de subtypes sneller en consistenter te detecteren uit microscoopbeelden, mogelijk het zorgtraject te versnellen terwijl specialisten de controle behouden.
Een nadere blik op een kinderkanker van het bloed
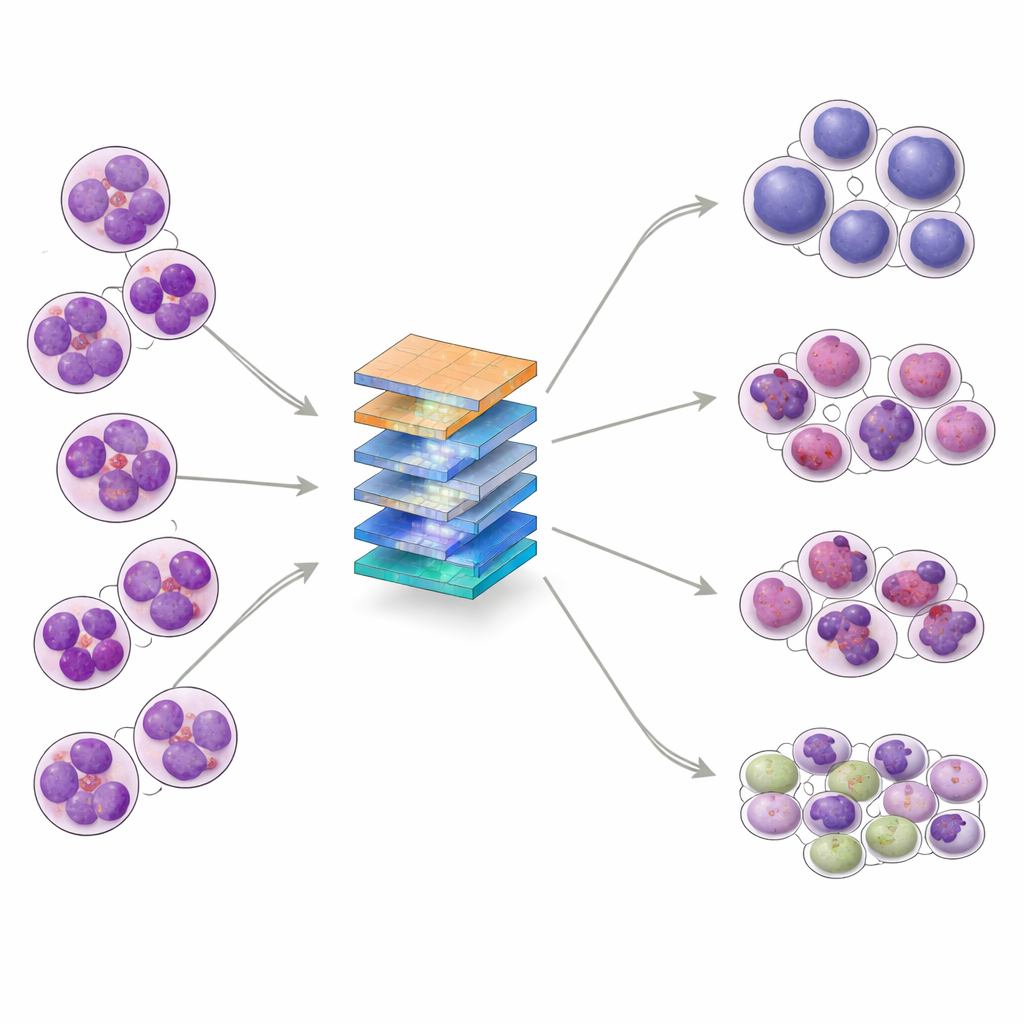
ALL ontstaat wanneer onrijpe witte bloedcellen, lymfoblasten genaamd, ongecontroleerd groeien in het beenmerg en in de bloedbaan terechtkomen. Deze abnormale cellen verdringen gezonde bloedcellen en kunnen zich naar het zenuwstelsel verspreiden. ALL is de meest voorkomende kinderkanker, maar komt ook bij volwassenen voor. Onder de microscoop verdelen specialisten ALL in drie hoofdsubtypes — L1, L2 en L3 — op basis van grootte en vorm van de cellen, de structuur van hun genetisch materiaal en het uiterlijk van het omgevende vocht. Het onderscheiden van deze subtypes, en het scheiden van gezond beenmerg, is belangrijk voor de behandelkeuze, maar zelfs experts kunnen dit lastig vinden wanneer de celuiterlijkheden sterk op elkaar lijken.
Computers leren zien wat experts zien
De onderzoekers wilden een AI‑systeem bouwen dat beenmergbeelden in vier groepen kan indelen: de drie ALL‑subtypes en normaal (niet‑leukemisch) materiaal. Ze verzamelden 328 hoogvergrotingsbeelden uit een klinisch laboratorium in Pakistan, van patiënten van 10 tot 45 jaar, en gebruikten vervolgens data‑augmentatietechnieken — zoals rotatie, spiegelen en subtiele aanpassingen in helderheid of contrast — om 1.585 gevarieerde trainingsvoorbeelden te creëren terwijl sleutelstructuren van cellen behouden bleven. De dataset werd verdeeld in trainings-, validatie- en testsets en verder geanalyseerd met statistische hulpmiddelen die lieten zien dat de klassen op complexe manieren overlappen, wat benadrukt dat de taak niet triviaal is, zelfs niet voor geavanceerde algoritmen.
Hoe het nieuwe AI‑model aandacht besteedt
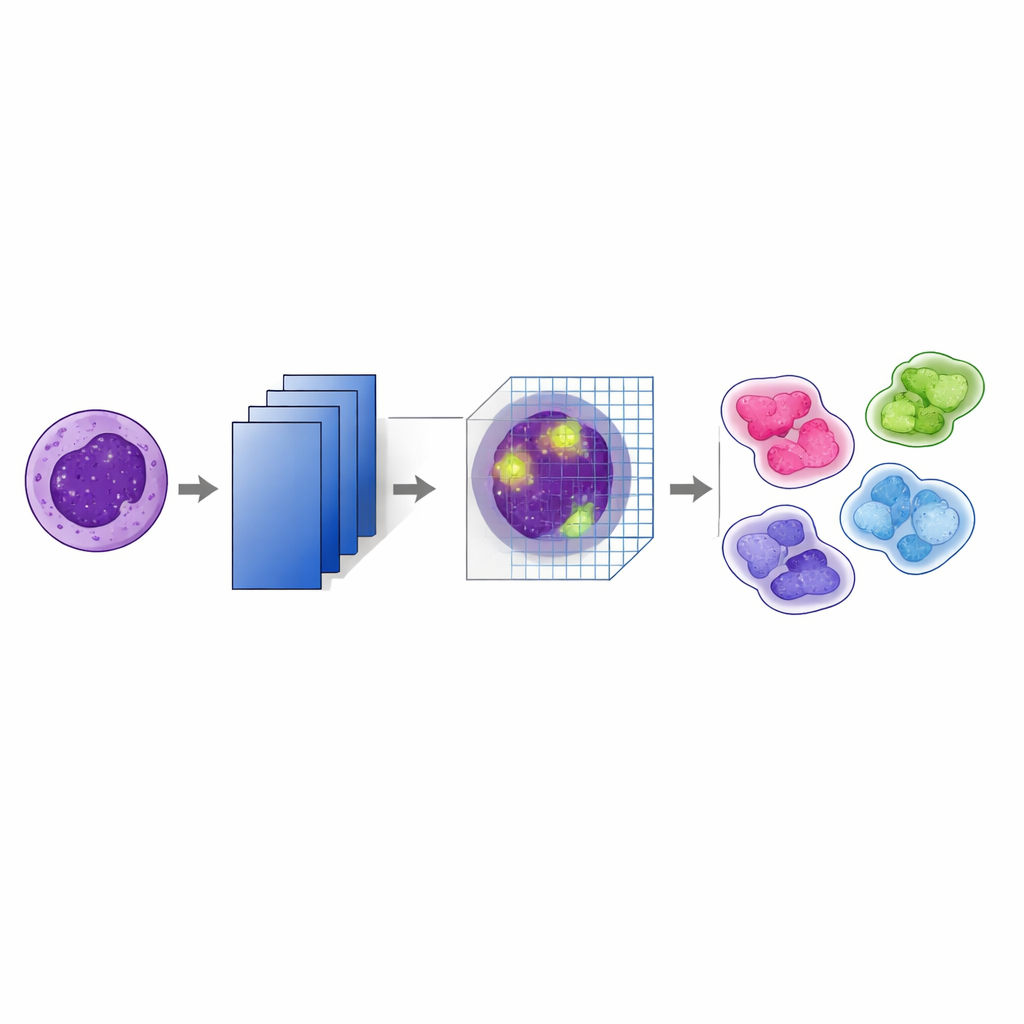
Centraal in de studie staat een aangepaste versie van een bekend beeldherkenningsnetwerk genaamd VGG19. Daarboven bouwden de auteurs een "convolutional block attention module" (CBAM) in na elke belangrijke poolingstap. Simpel gezegd leert het model eerst vele gelaagde kenmerken uit de beelden en gebruikt daarna aandacht om te beslissen welke kenmerken en welke regio’s in elk beeld meer gewicht verdienen. Een deel van het aandachtmechanisme benadrukt de meest informatieve kanalen — patronen zoals nucleaire randen of interne textuur — terwijl een ander deel de belangrijkste locaties binnen de cel uitlicht. Door deze aandachtstappen op meerdere dieptes in het netwerk te stapelen, houdt het systeem subtiele visuele aanwijzingen bij die helpen onderscheiden, bijvoorbeeld tussen nauwe verwante leukemiesubtypes.
Hoe goed het systeem presteert
Het CBAM‑verrijkte VGG19‑model werd getest tegenover verschillende populaire deep‑learningarchitecturen, waaronder DenseNet, Inception, MobileNet en de originele VGG19. Met behulp van standaard prestatiematen bereikte het nieuwe model een totale nauwkeurigheid van 98,73%, ongeveer 5,7 procentpunt hoger dan VGG19 zonder aandacht en beter dan alle concurrerende modellen op dezelfde data. Gedetailleerde resultaten toonden sterke precisie en recall over alle vier klassen, inclusief het zeldzame L3‑subtype, en de receiver‑operating‑characteristic‑curves lagen dicht bij ideaal. Het team voerde ook k‑fold cross‑validatie uit — trainen en testen op meerdere data‑splits — om te controleren dat de resultaten stabiel waren, en voerde "ablation"‑experimenten uit die aantonen dat het gebruik van zowel kanaal‑ als ruimtelijke aandacht op meerdere niveaus cruciaal was voor de verbeteringen.
Wat dit kan betekenen voor patiënten en artsen
Hoewel de cijfers veelbelovend zijn, benadrukken de auteurs dat dit systeem niet klaar is om menselijke experts te vervangen of zelfstandig in de kliniek te worden gebruikt. De studie berust op een relatief kleine, eencenter‑dataset en er is geen onafhankelijke, multizaal‑ of multicentrumtest om te bewijzen dat het model even goed werkt in andere omgevingen of populaties. Toch laat het werk zien dat zorgvuldig ontworpen aandachtmechanismen AI kunnen helpen zich te richten op dezelfde fijne visuele details die pathologen gebruiken bij het beoordelen van beenmergpreparaten. In de toekomst zouden vergelijkbare systemen, gevalideerd op veel grotere en meer diverse datasets, als decision‑supporttools kunnen dienen — snel verdachte gevallen signaleren, waarschijnlijke ALL‑subtypes suggereren en heatmaps tonen van de regio’s die hun voorspellingen beïnvloedden — zodat artsen sneller en met meer vertrouwen diagnoses kunnen stellen.
Bronvermelding: Rahman, S.I.U., Abbas, N., Ali, S. et al. Improving acute lymphoblastic leukemia diagnosis through CBAM-enhanced VGG19 deep learning. Sci Rep 16, 11027 (2026). https://doi.org/10.1038/s41598-026-40184-4
Trefwoorden: acute lymfatische leukemie, medische beeldvorming AI, deep learning diagnose, aandachtmechanismen, beenmergmicroscopie