Clear Sky Science · de
Verbesserung der Diagnose der akuten lymphoblastischen Leukämie durch CBAM‑verstärktes VGG19‑Deep‑Learning
Warum schnellere Blutkrebskontrollen wichtig sind
Die akute lymphoblastische Leukämie (ALL) ist ein aggressiver Blutkrebs, der unbehandelt binnen Wochen lebensbedrohlich werden kann. Heute diagnostizieren Ärztinnen und Ärzte ALL häufig durch die Betrachtung von Knochenmark- und Blutproben unter dem Mikroskop — eine sorgfältige, zeitaufwändige Aufgabe, die stark von der Expertise der Beurteilenden abhängt. Diese Studie untersucht, wie eine gezielt angepasste Form künstlicher Intelligenz (KI) Ärzten dabei helfen könnte, ALL und ihre Subtypen schneller und konsistenter in Mikroskopbildern zu erkennen, wodurch die Versorgung beschleunigt werden könnte, während Spezialistinnen und Spezialisten weiterhin die Kontrolle behalten.
Ein genauerer Blick auf einen kindlichen Blutkrebs
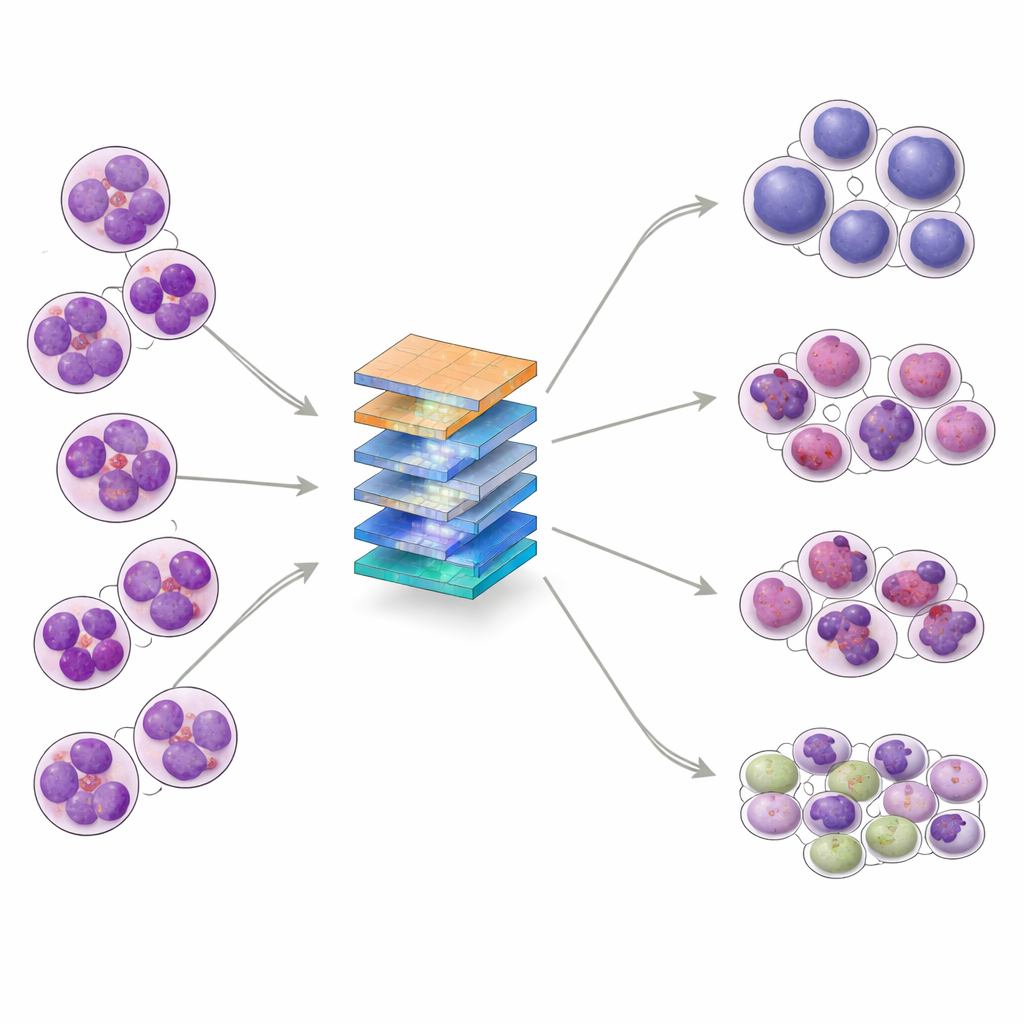
ALL entsteht, wenn unreife weiße Blutkörperchen, sogenannte Lymphoblasten, im Knochenmark unkontrolliert wachsen und ins Blut gelangen. Diese abnormen Zellen verdrängen gesunde Blutzellen und können sich bis ins Nervensystem ausbreiten. ALL ist der häufigste Krebs im Kindesalter, tritt aber auch bei Erwachsenen auf. Unter dem Mikroskop teilen Fachleute ALL in drei Hauptsubtypen — L1, L2 und L3 — ein, basierend auf Zellgröße und ‑form, der Textur des Erbguts und dem Erscheinungsbild des umgebenden Materials. Diese Subtypen voneinander zu unterscheiden und sie von gesundem Knochenmark abzugrenzen ist wichtig für die Therapieauswahl, fällt aber selbst Expertinnen und Experten schwer, wenn die Zellbilder einander sehr ähneln.
Computern beibringen, das zu sehen, was Fachleute sehen
Die Forschenden entwickelten ein KI‑System, das Knochenmarkbilder in vier Gruppen einordnen kann: die drei ALL‑Subtypen und normale (nicht‑leukämische) Proben. Sie sammelten 328 hochvergrößerte Bilder aus einem klinischen Labor in Pakistan von Patienten im Alter von 10 bis 45 Jahren und verwendeten dann Datenaugmentierung — etwa Rotation, Spiegelung und subtile Änderungen von Helligkeit oder Kontrast —, um 1.585 unterschiedliche Trainingsbeispiele zu erzeugen, wobei zentrale Zellstrukturen erhalten blieben. Der Datensatz wurde in Trainings-, Validierungs‑ und Testmengen aufgeteilt und statistisch untersucht; die Analysen zeigten, dass sich die Klassen auf komplexe Weise überlappen, was bestätigt, dass die Aufgabe selbst für fortgeschrittene Algorithmen nicht trivial ist.
Wie das neue KI‑Modell aufmerksamer wird
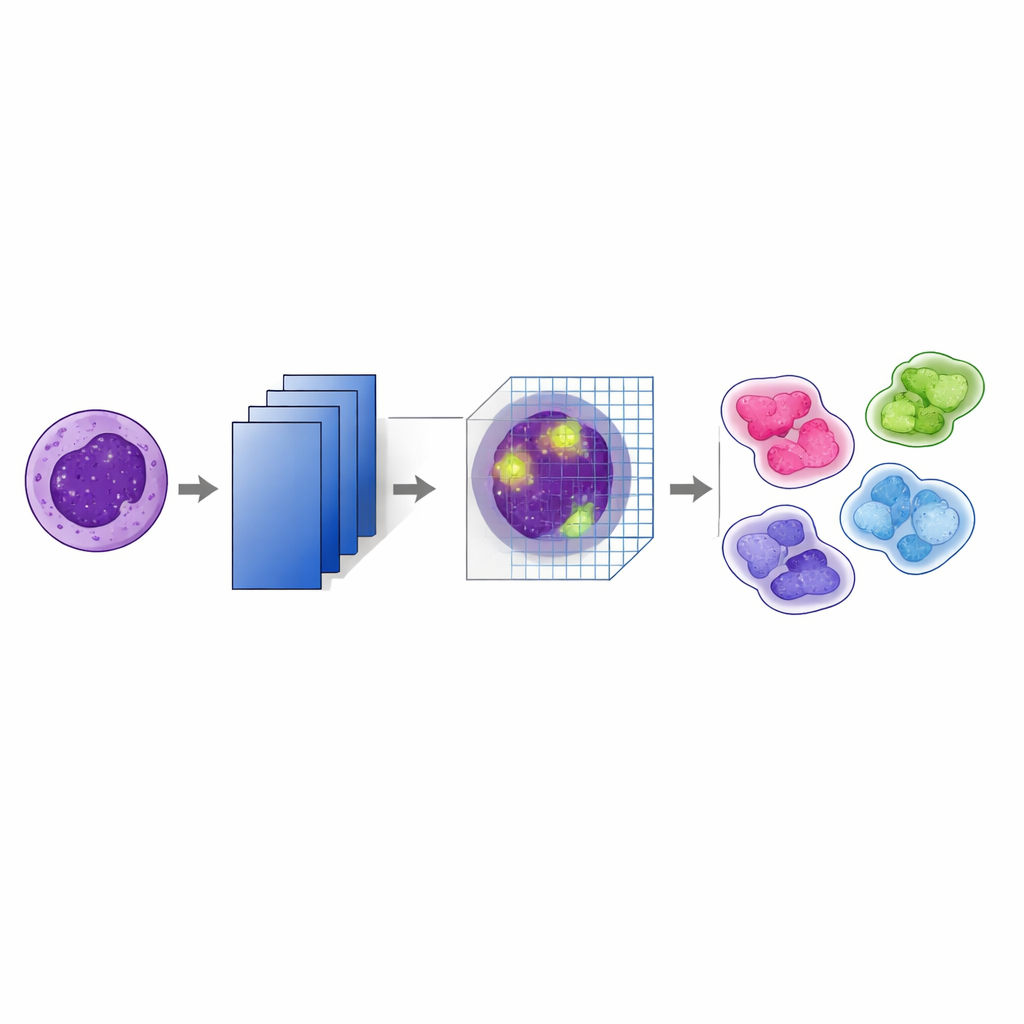
Im Zentrum der Studie steht eine modifizierte Version eines bekannten Bilderkennungsnetzes namens VGG19. Darauf aufbauend fügten die Autorinnen und Autoren nach jedem größeren Pooling‑Schritt ein „convolutional block attention module“ (CBAM) hinzu. Vereinfacht gesagt lernt das Modell zunächst viele geschichtete Merkmale aus den Bildern und verwendet dann Attention, um zu entscheiden, welche Merkmale und welche Bildregionen stärker gewichtet werden sollten. Ein Teil des Aufmerksamkeitsmechanismus betont die informativsten Kanäle — Muster wie Kernränder oder innere Textur —, während ein anderer Teil die wichtigsten Orte innerhalb der Zelle hervorhebt. Durch das Stapeln dieser Attention‑Schritte auf mehreren Ebenen behält das System feine visuelle Hinweise im Blick, die helfen, etwa eng verwandte Leukämie‑Subtypen zu unterscheiden.
Wie gut das System abschneidet
Das CBAM‑verstärkte VGG19‑Modell wurde mit mehreren populären Deep‑Learning‑Architekturen verglichen, darunter DenseNet, Inception, MobileNet und das ursprüngliche VGG19. Gemessen an üblichen Leistungskennzahlen erzielte das neue Modell eine Gesamtgenauigkeit von 98,73 %, etwa 5,7 Prozentpunkte mehr als VGG19 ohne Attention und besser als alle konkurrierenden Modelle auf denselben Daten. Detaillierte Ergebnisse zeigten starke Präzision und Sensitivität über alle vier Klassen, einschließlich des seltenen Subtyps L3, und die ROC‑Kurven lagen nahe am Ideal. Das Team führte zudem k‑fache Kreuzvalidierung durch — Training und Testen auf mehreren Aufteilungen der Daten — um die Stabilität der Ergebnisse zu prüfen, und führte „Ablations“‑Experimente durch, die zeigten, dass die Verwendung sowohl von Kanal‑ als auch von räumlicher Attention in mehreren Stufen entscheidend für die Leistungssteigerung war.
Welche Bedeutung das für Patientinnen, Patienten und Ärztinnen, Ärzte haben könnte
Obwohl die Zahlen vielversprechend sind, betonen die Autorinnen und Autoren, dass das System nicht bereit ist, menschliche Expertinnen und Experten zu ersetzen oder eigenständig klinisch eingesetzt zu werden. Die Studie stützt sich auf einen relativ kleinen, single‑center Datensatz, und es fehlt ein unabhängiger, multizentrischer Test, der belegen würde, dass das Modell in unterschiedlichen Einrichtungen oder Populationen gleichermaßen funktioniert. Dennoch zeigt die Arbeit, dass sorgfältig gestaltete Attention‑Mechanismen KI dabei unterstützen können, sich auf dieselben feinen visuellen Details zu konzentrieren, die Pathologen beim Lesen von Knochenmarkpräparaten heranziehen. In Zukunft könnten ähnliche Systeme, validiert an deutlich größeren und vielfältigeren Datensätzen, als Entscheidungsunterstützung dienen — verdächtige Fälle schnell markieren, wahrscheinliche ALL‑Subtypen vorschlagen und Heatmaps der Regionen zeigen, die ihre Vorhersagen beeinflusst haben — sodass Ärztinnen und Ärzte schneller und sicherer diagnostizieren können.
Zitation: Rahman, S.I.U., Abbas, N., Ali, S. et al. Improving acute lymphoblastic leukemia diagnosis through CBAM-enhanced VGG19 deep learning. Sci Rep 16, 11027 (2026). https://doi.org/10.1038/s41598-026-40184-4
Schlüsselwörter: akute lymphoblastische Leukämie, medizinische Bildgebung KI, Deep‑Learning‑Diagnose, Achtsamkeitsmechanismen, Knochenmarkmikroskopie