Clear Sky Science · es
Mejora del diagnóstico de la leucemia linfoblástica aguda mediante aprendizaje profundo VGG19 potenciado con CBAM
Por qué importan las pruebas más rápidas para el cáncer de sangre
La leucemia linfoblástica aguda (LLA) es un cáncer de la sangre agresivo que puede volverse potencialmente mortal en pocas semanas si no se detecta y trata con rapidez. Hoy en día, los médicos suelen diagnosticar la LLA examinando la médula ósea y las células sanguíneas al microscopio: una tarea minuciosa y que consume tiempo, que depende en gran medida del juicio de expertos. Este estudio explora cómo una forma adaptada de inteligencia artificial (IA) podría ayudar a los médicos a detectar la LLA y sus subtipos de forma más rápida y consistente a partir de imágenes de microscopio, acelerando potencialmente la atención sin dejar de mantener a los especialistas al mando.
Una mirada más cercana a un cáncer infantil de la sangre
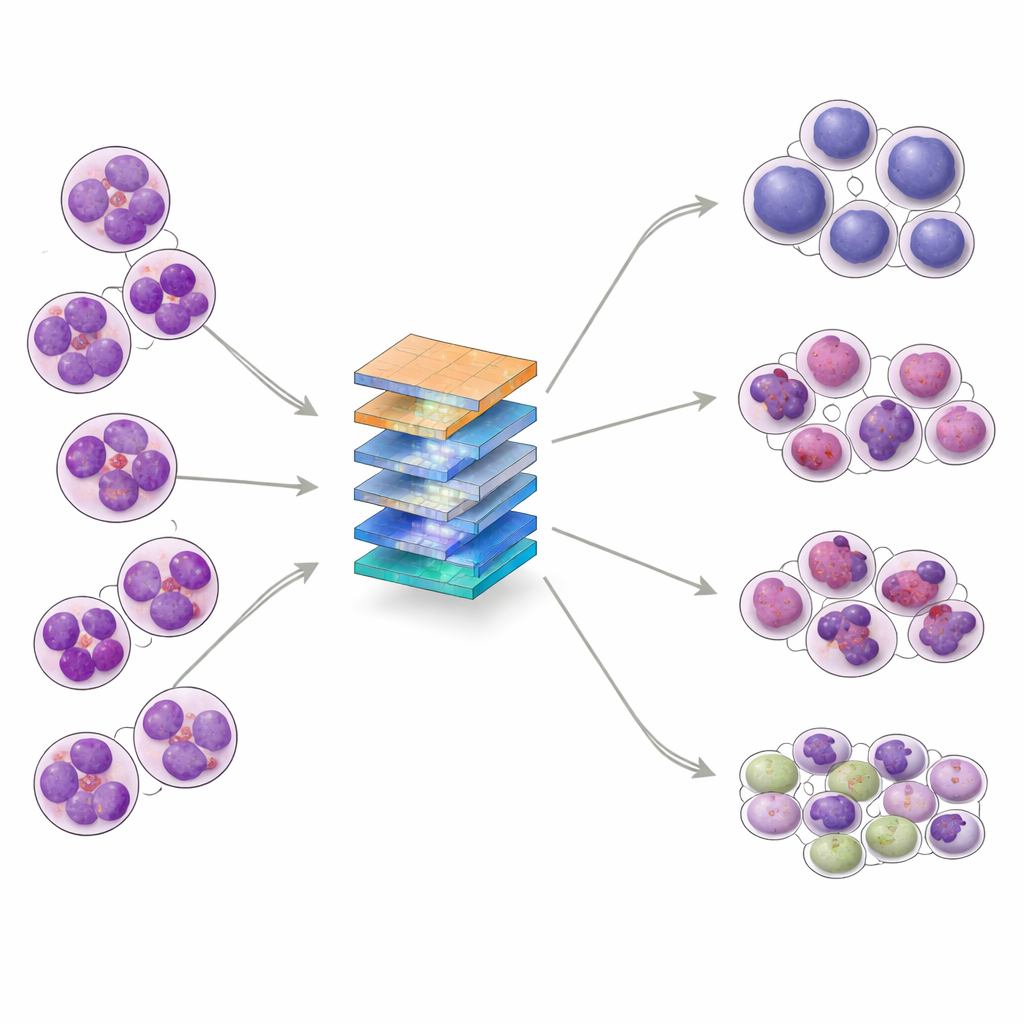
La LLA surge cuando células blancas inmaduras, llamadas linfoblastos, proliferan de forma descontrolada en la médula ósea y pasan al torrente sanguíneo. Estas células anómalas desplazan a las células sanguíneas sanas y pueden propagarse al sistema nervioso. La LLA es el cáncer infantil más frecuente, aunque también se presenta en adultos. Al microscopio, los especialistas dividen la LLA en tres subtipos principales —L1, L2 y L3— según el tamaño y la forma de las células, la textura de su material genético y el aspecto del fluido circundante. Distinguir estos subtipos, y separarlos de la médula ósea sana, es importante para escoger el tratamiento; sin embargo, incluso los expertos pueden tener dificultades cuando las apariencias celulares son muy similares.
Enseñar a las máquinas a ver lo que ven los expertos
Los investigadores se propusieron construir un sistema de IA capaz de clasificar las imágenes de médula ósea en cuatro grupos: los tres subtipos de LLA y muestras normales (no leucémicas). Reunieron 328 imágenes de alta ampliación de un laboratorio clínico en Pakistán, con pacientes de entre 10 y 45 años, y luego emplearon técnicas de aumento de datos —como rotación, volteo y cambios sutiles en brillo o contraste— para crear 1.585 ejemplos de entrenamiento variados preservando las estructuras celulares clave. El conjunto de datos se dividió en conjuntos de entrenamiento, validación y prueba, y se examinó además con herramientas estadísticas que mostraron que las clases se solapan de maneras complejas, lo que refuerza que la tarea no es trivial ni siquiera para algoritmos avanzados.
Cómo el nuevo modelo de IA presta atención
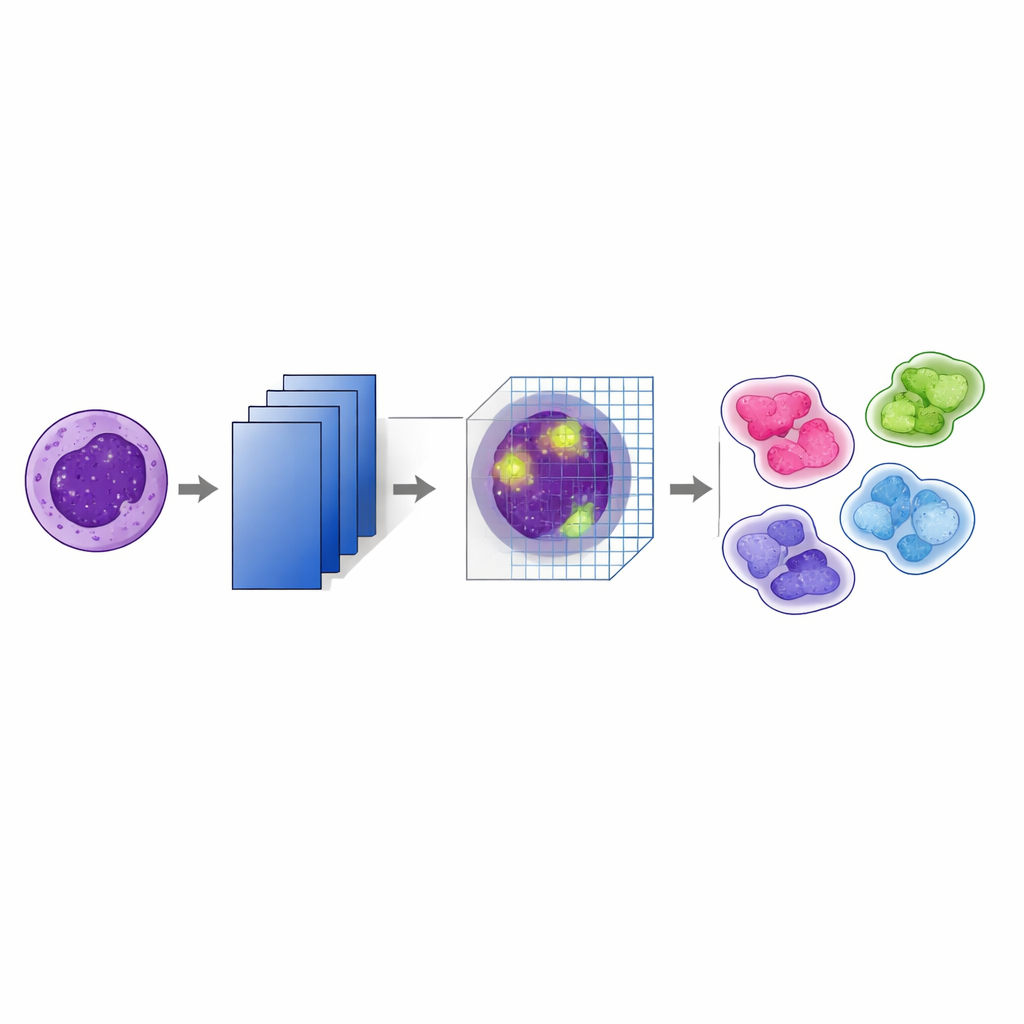
El núcleo del estudio es una versión modificada de una red de reconocimiento de imágenes bien conocida llamada VGG19. Sobre esta, los autores añadieron un “módulo de atención por bloques convolucionales” (CBAM) tras cada paso importante de agrupamiento (pooling). En términos sencillos, el modelo primero aprende múltiples características en capas a partir de las imágenes y después usa atención para decidir qué características y qué regiones de cada imagen merecen más peso. Una parte del mecanismo de atención enfatiza los canales más informativos —patrones como los bordes nucleares o la textura interna— mientras que otra parte destaca las ubicaciones más importantes dentro de la célula. Al apilar estos pasos de atención en varios niveles de la red, el sistema sigue pistas visuales sutiles que ayudan a distinguir, por ejemplo, entre subtipos de leucemia estrechamente relacionados.
Qué tan bien funciona el sistema
El modelo VGG19 potenciado con CBAM se probó frente a varias arquitecturas populares de aprendizaje profundo, incluidas DenseNet, Inception, MobileNet y la VGG19 original. Utilizando medidas estándar de rendimiento, el nuevo modelo alcanzó una precisión global del 98,73%, aproximadamente 5,7 puntos porcentuales más que la VGG19 sin atención y mejor que todos los modelos competidores con los mismos datos. Los resultados detallados mostraron alta precisión y sensibilidad en las cuatro clases, incluido el raro subtipo L3, y las curvas ROC (característica operativa del receptor) se acercaron al ideal. El equipo también realizó validación cruzada k-fold —entrenando y probando en múltiples particiones del conjunto— para comprobar la estabilidad de los resultados, y llevó a cabo experimentos de “ablación” que demostraron que usar atención de canal y espacial en varias etapas fue crucial para las mejoras.
Qué podría significar esto para pacientes y médicos
Aunque las cifras son prometedoras, los autores subrayan que este sistema no está listo para sustituir a los expertos humanos ni para usarse de forma autónoma en la clínica. El estudio se basa en un conjunto de datos relativamente pequeño y de un único centro, y no existe una prueba independiente multi-hospitalaria que demuestre que el modelo funciona igualmente bien en distintos entornos o poblaciones. Aun así, el trabajo muestra que los mecanismos de atención diseñados con cuidado pueden ayudar a la IA a centrarse en los mismos detalles visuales finos que usan los patólogos al leer los frotis de médula ósea. En el futuro, sistemas similares, validados con conjuntos de datos mucho más grandes y diversos, podrían servir como herramientas de apoyo a la decisión —marcando rápidamente casos sospechosos, sugiriendo los subtipos probables de LLA y mostrando mapas de calor de las regiones que influyeron en sus predicciones— para que los médicos tomen diagnósticos más rápidos y con mayor confianza.
Cita: Rahman, S.I.U., Abbas, N., Ali, S. et al. Improving acute lymphoblastic leukemia diagnosis through CBAM-enhanced VGG19 deep learning. Sci Rep 16, 11027 (2026). https://doi.org/10.1038/s41598-026-40184-4
Palabras clave: leucemia linfoblástica aguda, IA en imágenes médicas, diagnóstico mediante aprendizaje profundo, mecanismos de atención, microscopía de médula ósea