Clear Sky Science · it
Migliorare la diagnosi della leucemia linfoblastica acuta tramite VGG19 potenziata con CBAM e deep learning
Perché controlli più rapidi per i tumori del sangue sono importanti
La leucemia linfoblastica acuta (LLA) è un tumore del sangue aggressivo che può diventare pericoloso per la vita in poche settimane se non viene identificato e trattato tempestivamente. Oggi i medici spesso diagnosticano la LLA osservando al microscopio midollo osseo e cellule del sangue—un compito accurato e dispendioso in termini di tempo che dipende fortemente dal giudizio di specialisti. Questo studio esplora come una forma mirata di intelligenza artificiale (IA) possa aiutare i medici a individuare la LLA e i suoi sottotipi in modo più rapido e coerente dalle immagini al microscopio, potenzialmente accelerando le cure pur mantenendo il controllo agli specialisti.
Uno sguardo più attento a un tumore ematico infantile
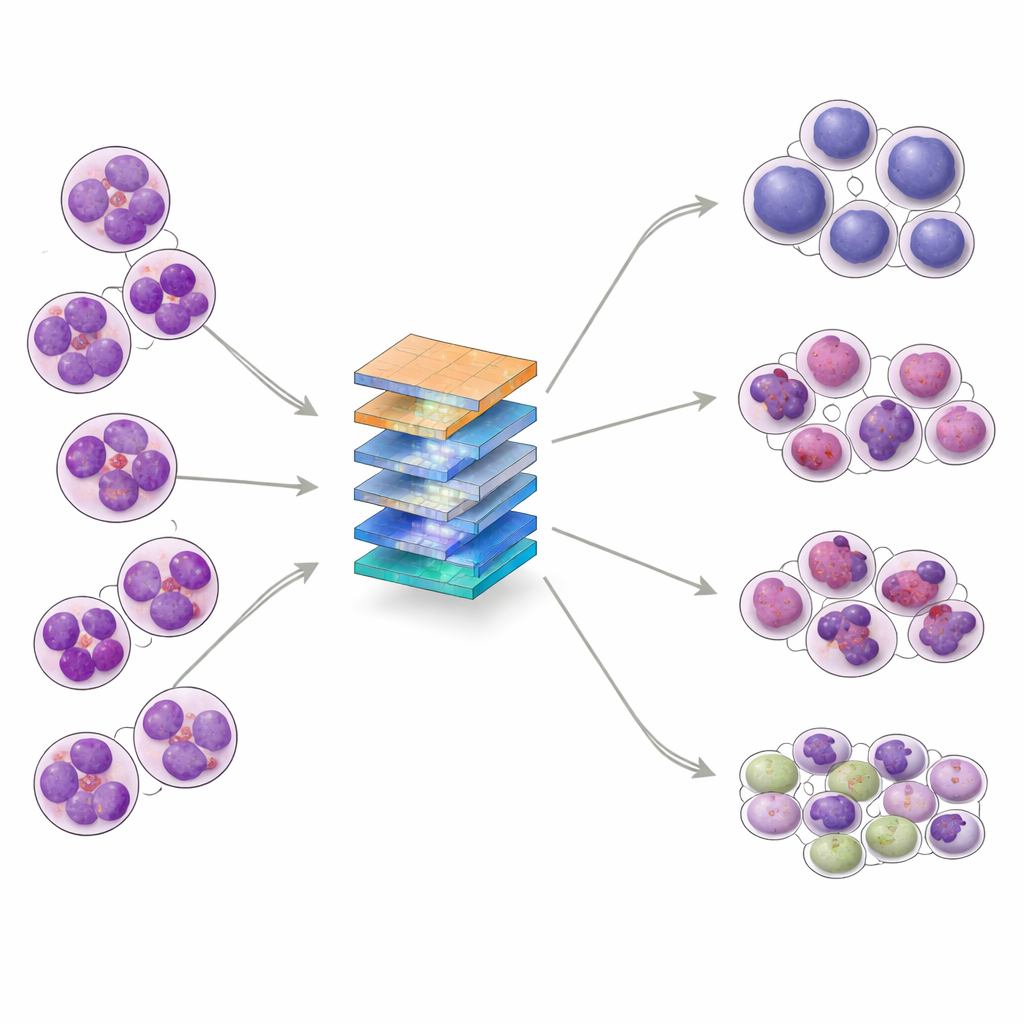
La LLA insorge quando globuli bianchi immaturi, chiamati linfoblasti, crescono in modo incontrollato nel midollo osseo e si riversano nel sangue. Queste cellule anomale soppiantano le cellule ematiche sane e possono diffondersi al sistema nervoso. La LLA è il tumore più comune in età pediatrica, ma si presenta anche negli adulti. Al microscopio, gli specialisti suddividono la LLA in tre principali sottotipi—L1, L2 e L3—in base a dimensione e forma delle cellule, alla trama del materiale genetico e all’aspetto del liquido circostante. Distinguere questi sottotipi e separare i campioni sani dal midollo leucemico è importante per scegliere la terapia, ma anche gli esperti possono trovare difficile il compito quando l’aspetto cellulare è molto simile.
Insegnare ai computer a vedere ciò che vedono gli esperti
I ricercatori hanno voluto costruire un sistema di IA in grado di classificare le immagini del midollo osseo in quattro gruppi: i tre sottotipi di LLA e i campioni normali (non leucemici). Hanno raccolto 328 immagini a elevata ingrandimento da un laboratorio clinico in Pakistan, relative a pazienti di età compresa tra 10 e 45 anni, e hanno poi applicato tecniche di data augmentation—come rotazioni, ribaltamenti e variazioni sottili di luminosità o contrasto—per creare 1.585 esempi di addestramento variati preservando le strutture cellulari chiave. Il dataset è stato suddiviso in insiemi di addestramento, validazione e test, e analizzato con strumenti statistici che hanno mostrato come le classi si sovrappongano in modi complessi, confermando che il compito non è banale nemmeno per algoritmi avanzati.
Come il nuovo modello di IA presta attenzione
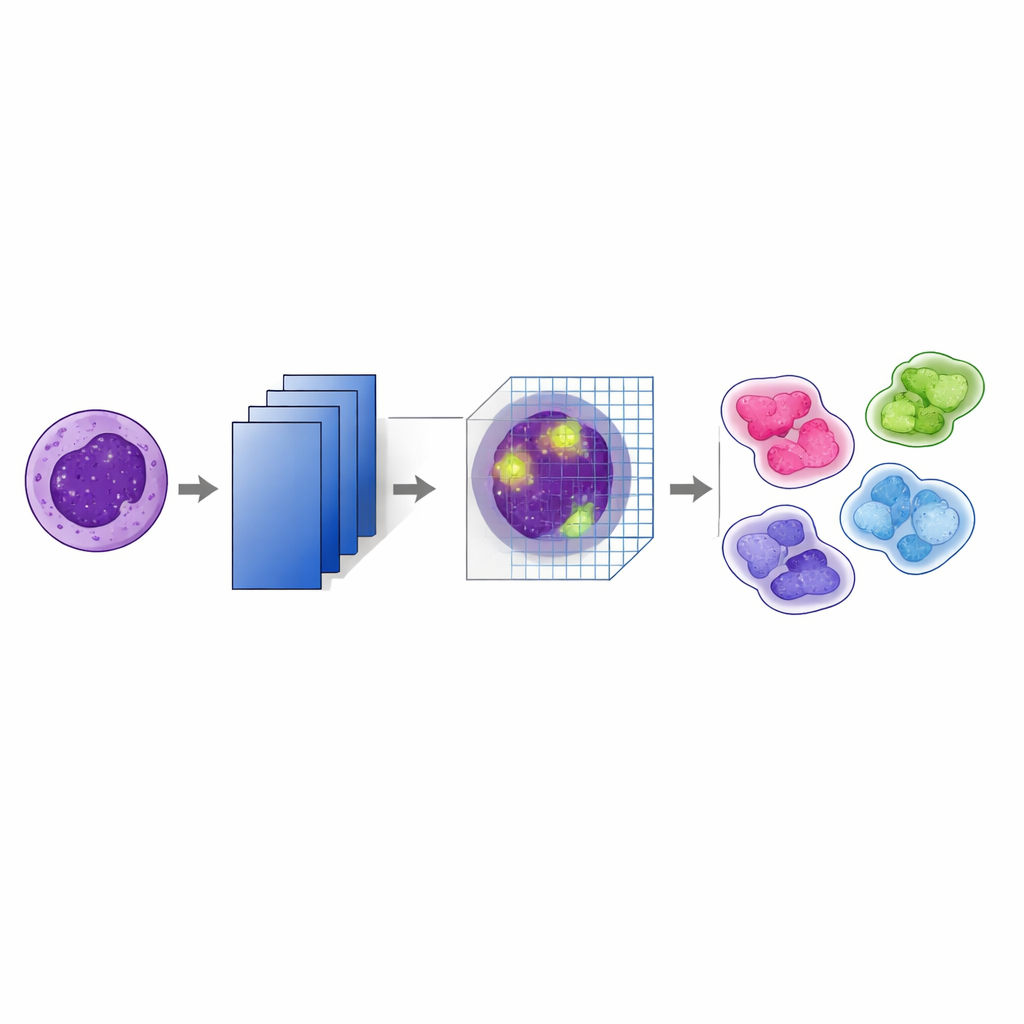
Al centro dello studio c’è una versione modificata di una nota rete per il riconoscimento delle immagini chiamata VGG19. Su questa, gli autori hanno aggiunto un “convolutional block attention module” (CBAM) dopo ogni principale passaggio di pooling. In termini semplici, il modello prima apprende molte caratteristiche stratificate dalle immagini, poi usa l’attenzione per decidere quali caratteristiche e quali regioni di ciascuna immagine meritano maggiore importanza. Una parte del meccanismo di attenzione enfatizza i canali più informativi—pattern come i bordi nucleari o la texture interna—mentre un’altra parte mette in evidenza le posizioni più rilevanti all’interno della cellula. Impilando questi passaggi di attenzione a diversi livelli della rete, il sistema tiene traccia di indizi visivi sottili che aiutano a distinguere, per esempio, sottotipi leucemici molto simili tra loro.
Quanto bene funziona il sistema
Il modello VGG19 potenziato con CBAM è stato confrontato con diverse architetture deep‑learning popolari, tra cui DenseNet, Inception, MobileNet e la VGG19 originale. Usando misure standard di performance, il nuovo modello ha raggiunto un’accuratezza complessiva del 98,73%, circa 5,7 punti percentuali in più rispetto alla VGG19 senza attenzione e superiore a tutti i modelli concorrenti sugli stessi dati. I risultati dettagliati hanno mostrato elevata precisione e richiamo per tutte e quattro le classi, incluso il raro sottotipo L3, e le curve ROC si sono avvicinate all’ideale. Il team ha inoltre eseguito una validazione incrociata k‑fold—addestrando e testando su più suddivisioni dei dati—per verificare la stabilità dei risultati, e ha condotto esperimenti di “ablation” che dimostrano come l’uso combinato di attenzione sui canali e spaziale a più stadi fosse cruciale per i miglioramenti ottenuti.
Cosa potrebbe significare per pazienti e medici
Pur essendo i numeri promettenti, gli autori sottolineano che questo sistema non è pronto a sostituire gli esperti umani né a essere usato da solo in clinica. Lo studio si basa su un dataset relativamente piccolo e di un unico centro, e manca una prova indipendente su più ospedali per dimostrare che il modello funzioni allo stesso modo in contesti o popolazioni differenti. Tuttavia, il lavoro dimostra che meccanismi di attenzione progettati con cura possono aiutare l’IA a concentrarsi sugli stessi dettagli visivi fini che i patologi usano nell’analisi dei vetrini del midollo. In futuro, sistemi simili, validati su dataset molto più grandi e diversificati, potrebbero fungere da strumenti di supporto decisionale—segnalando rapidamente i casi sospetti, suggerendo i sottotipi di LLA più probabili e mostrando mappe di calore delle regioni che hanno influenzato le predizioni—così che i medici possano formulare diagnosi più rapide e sicure.
Citazione: Rahman, S.I.U., Abbas, N., Ali, S. et al. Improving acute lymphoblastic leukemia diagnosis through CBAM-enhanced VGG19 deep learning. Sci Rep 16, 11027 (2026). https://doi.org/10.1038/s41598-026-40184-4
Parole chiave: leucemia linfoblastica acuta, IA per imaging medico, diagnosi con deep learning, meccanismi di attenzione, microscopia del midollo osseo