Clear Sky Science · pl
Reaktywacja wyczerpanych limfocytów T penetrujących nowotwór za pomocą bispecyficznego łącznika DC–T w modelach mysich
Przywracanie aktywności zmęczonym komórkom odpornościowym
Nowotwór często wygrywa nie dlatego, że nasz układ odpornościowy go nie rozpoznaje, ale dlatego, że komórki walczące z nowotworem ulegają wyczerpaniu i przestają skutecznie działać. Badanie na myszach opisuje pomysłowy nowy białkowy lek, który fizycznie łączy dwa kluczowe rodzaje komórek odpornościowych wewnątrz guza, umożliwiając im ponowną komunikację. W efekcie "wybudza" wyczerpane komórki T zabójcze, zmniejsza guzy i pozostawia po sobie pamięć immunologiczną nowotworu, co potencjalnie zapobiega nawrotom.
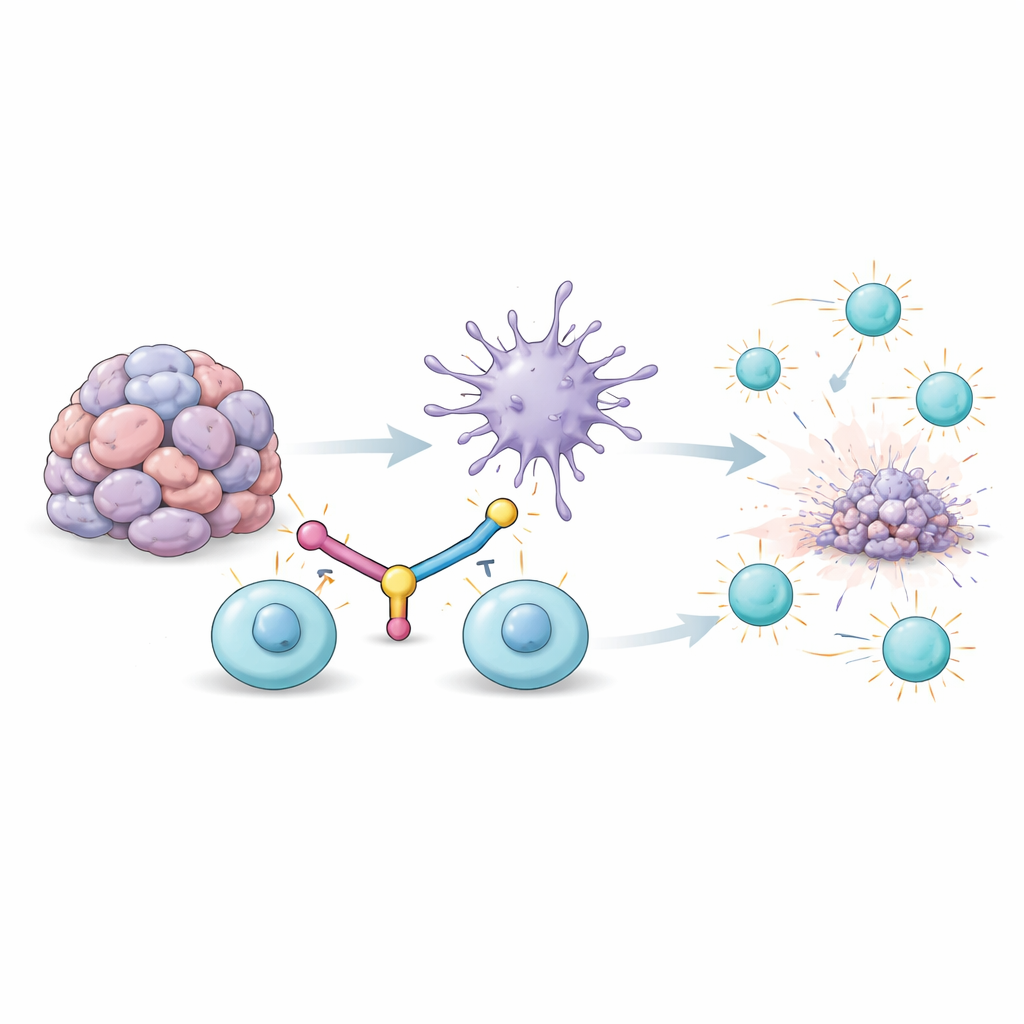
Dlaczego komórki walczące z nowotworem tracą siły
Głęboko w obrębie guzów specjalne białe krwinki zwane limfocytami T rozpoznają i atakują komórki nowotworowe. Jednak przy długotrwałej ekspozycji na sygnały wydzielane przez guz przechodzą one w stan wyczerpania: przestają się dzielić, wytwarzają mniej molekuł efektorowych i mogą obumierać. Jednym z białek powierzchniowych powiązanych z tym stanem jest TIM3. Równocześnie inny typ komórek odpornościowych — komórki dendrytyczne — powinien szkolić limfocyty T, prezentując im fragmenty guza i przekazując silne sygnały „do działania”. W guzie jednak komórki dendrytyczne są często osłabione przez mikrośrodowisko nowotworu i otrzymują zbyt mało potężnego przekaźnika immunologicznego, typu I interferonu. W wyniku tego powstaje podwójna porażka: limfocyty T są wyczerpane, a ich główni „trenerzy” nie potrafią ich prawidłowo pobudzić.
Mostkowa cząsteczka do ponownego połączenia sojuszników odpornościowych
Naukowcy zaprojektowali pojedyncze białko fuzyjne, nazwane bispecyficznym łącznikiem DC–T (BiDT), aby rozwiązać oba problemy jednocześnie. Jeden koniec BiDT to przeciwciało rozpoznające TIM3 na wyczerpanych limfocytach T. Drugi koniec to zmodyfikowana postać interferonu-alfa, która silnie aktywuje komórki dendrytyczne przez ich receptor dla interferonu, ale została dostrojona tak, by ograniczyć niepożądane efekty w innych częściach organizmu. Podawany myszom z guzami, BiDT kumuluje się w obrębie guza, gdzie TIM3 jest obficie obecny na limfocytach T. Tam dosłownie łączy komórki dendrytyczne i wyczerpane limfocyty T, wymuszając bliski kontakt i jednocześnie przełączając komórki dendrytyczne w bardziej aktywny, stymulacyjny stan.
Obudzeni zabójcy i trwała pamięć immunologiczna
Gdy ten most zostanie utworzony, komórki dendrytyczne zwiększają kluczowe sygnały „współstymulujące” na swojej powierzchni i pomagają limfocytom T wznowić szlaki przeżycia i proliferacji. Wyczerpane limfocyty T zaczynają wyglądać i zachowywać się jak skuteczni bojownicy: wykazują większe poziomy białek sprzyjających przetrwaniu (dzięki czemu rzadziej obumierają), odzyskują produkcję ważnych molekuł takich jak IL-2 i interferon-gamma oraz zwiększają swoją liczbę. W modelach raka jelita grubego i czerniaka u myszy leczenie BiDT często usuwało ustalone guzy i poprawiało przeżywalność przy mniejszej utracie masy ciała i mniejszej toksyczności ogólnoustrojowej niż podawanie interferonu i przeciwciała przeciw TIM3 oddzielnie. Co więcej, myszy wyleczone za pomocą BiDT były odporne na ponowne wszczepienie guza, a ich komórki odpornościowe mogły przenieść tę ochronę na inne zwierzęta, co dowodzi powstania trwałej, swoistej pamięci przeciwnowotworowej.
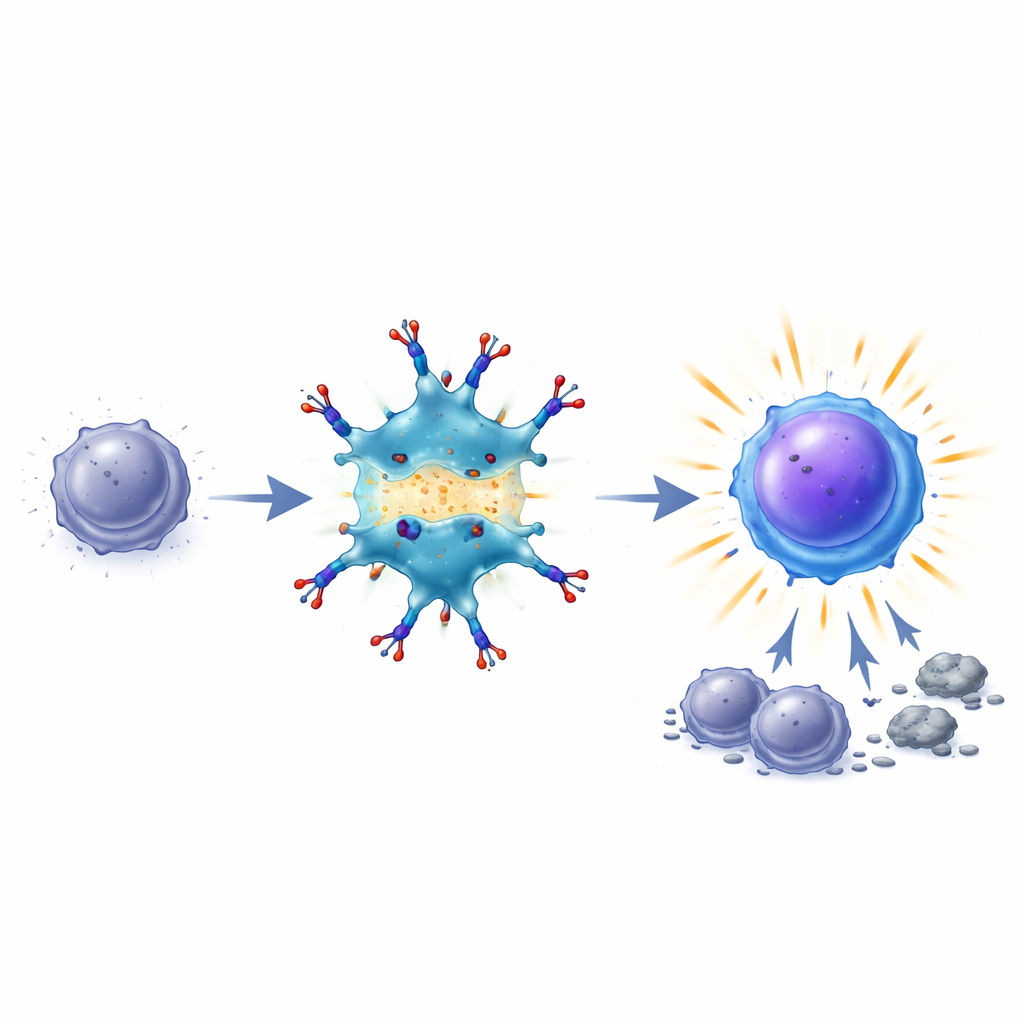
Działanie wewnątrz guza, a nie tylko w węzłach chłonnych
Precyzyjne eksperymenty genetyczne i polegające na eliminacji komórek wykazały, że skuteczność BiDT zależy od istniejących już w guzie limfocytów T zabójczych i komórek dendrytycznych, a nie od nowych limfocytów napływających z węzłów chłonnych. Sygnał interferonowy musi działać na komórki dendrytyczne, podczas gdy zaangażowanie TIM3 na limfocytach T jest kluczowe dla ich uratowania. Obudzone limfocyty T silnie odpowiadają na sygnały IL-2 i wydzielają fale interferonu-gamma, który z kolei pomaga niszczyć komórki nowotworowe. W „zimnym” modelu czerniaka, który zwykle opiera się standardowym lekom blokującym punkty kontrolne, BiDT częściowo pokonał tę oporność. W połączeniu z przeciwciałem blokującym PD-L1, które usuwa osobny hamulec na limfocytach T, terapia ta w znacznej części myszy doprowadziła do eradykacji guzów i wygenerowała długotrwałą ochronę.
Bezpieczniejsze wersje i nadzieje na przyszłość
Ponieważ terapie oparte na interferonie mogą być u pacjentów dość toksyczne, zespół opracował także wersję „proleku”, Pro-BiDT, w której część interferonowa jest nieaktywna dopóki enzymy obfite w guzie nie uwolnią jej działania; enzymy te występują rzadko w zdrowych tkankach. U myszy Pro-BiDT zachował silne efekty przeciwnowotworowe oryginalnego BiDT przy jednoczesnym znacznym zmniejszeniu objawów zapalenia i toksyczności krwi. Razem te wyniki sugerują nową strategię leczenia nowotworów: zamiast tylko zewnętrznie zdejmować hamulce z limfocytów T, precyzyjnie ponownie łącz i wzmacniaj obwody odpornościowe wewnątrz samego guza. Jeśli podobne efekty uda się uzyskać u ludzi, takie leki mogłyby pomóc uratować zmęczone odpowiedzi immunologiczne, przezwyciężyć oporność na obecne immunoterapie i zapewnić dłużej trwającą ochronę przed rakiem.
Cytowanie: Zhang, X., Gao, Y., Hu, W. et al. Reactivating exhausted tumor-infiltrating T cells by a bispecific DC-T cell engager in mice. Nat Commun 17, 4081 (2026). https://doi.org/10.1038/s41467-026-70876-4
Słowa kluczowe: immunoterapia nowotworów, wyczerpanie limfocytów T, komórki dendrytyczne, przeciwciała bispecyficzne, interferon alfa