Clear Sky Science · ar
إعادة تنشيط الخلايا التائية المستنزفة المتسللة إلى الورم بواسطة مصلّب ثنائي النوع يربط الخلايا الشجرية والخلايا التائية في الفئران
إعادة تشغيل الخلايا المناعية المتعبة
غالباً ما ينتصر السرطان ليس لأن جهازنا المناعي يعجز عن رؤيته، بل لأن الخلايا المكافحة للورم تُنهك وتتوقف عن العمل بشكل فعّال. تصف هذه الدراسة في الفئران دواءً بروتينياً ذكيّاً يربط فعلياً بين نوعين رئيسيين من الخلايا المناعية داخل الأورام حتى تتمكن من التواصل مجدداً. بهذا يعيد تنبيه الخلايا التائية القاتلة «المرهقة»، ويقلص الأورام، وحتى يترك وراءه ذاكرة للسرطان قد تمنع عودته.
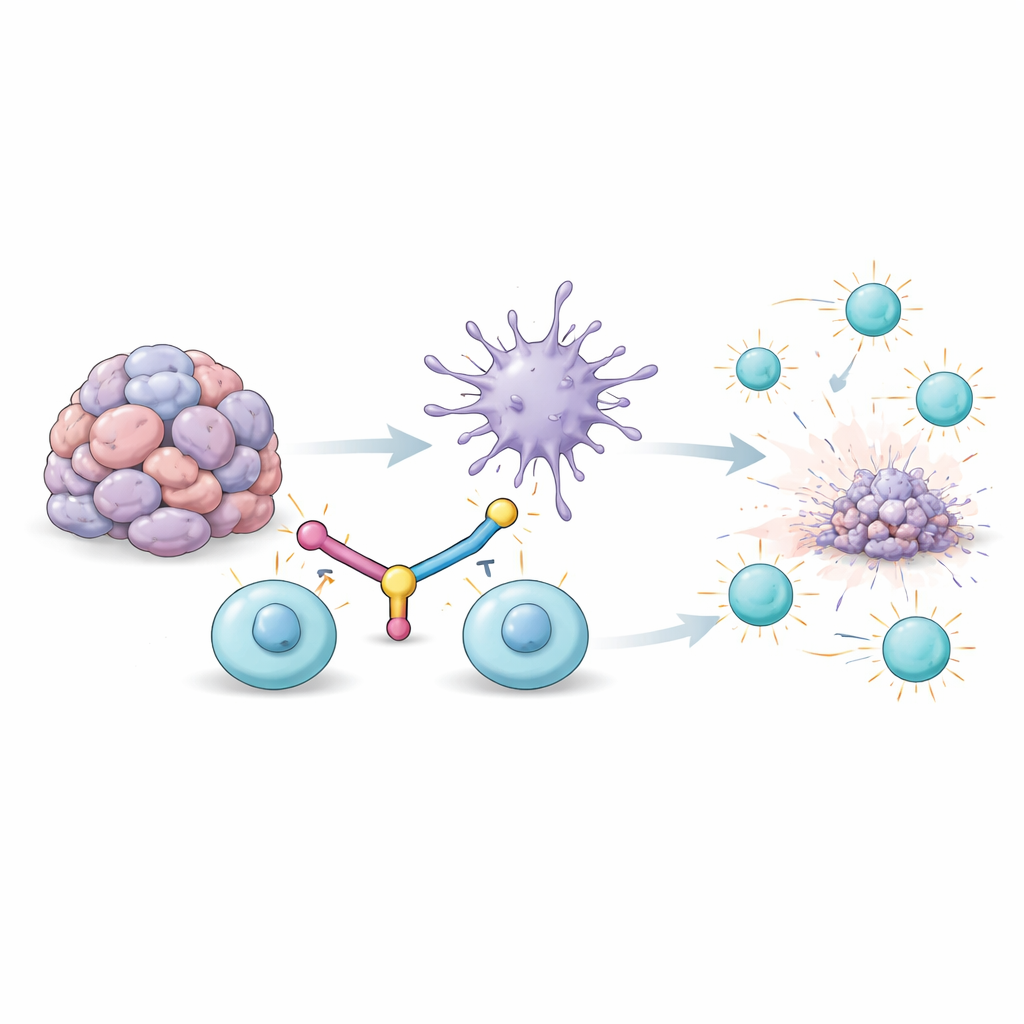
لماذا تنفد طاقة الخلايا المكافحة للأورام
في أعماق الأورام، تتعرف خلايا بيضاء متخصصة تُدعى الخلايا التائية على السرطان وتهاجمه. لكن عند تعرضها لإشارات الورم لفترة طويلة، تدخل هذه الخلايا في حالة إرهاق: تتوقف عن التكاثر، تنتج جزيئات هجوم أقل، وقد تموت أحياناً. يُرتبط أحد البروتينات السطحية بهذه الحالة ويُسمى TIM3. في الوقت نفسه، يفترض أن تقوم خلايا مناعية أخرى، الخلايا الشجرية، بتوجيه الخلايا التائية عبر عرض شظايا الورم ومنحها إشارات «انطلاق» قوية. داخل الأورام، مع ذلك، تكون الخلايا الشجرية غالباً مُثبطة بفعل بيئة الورم وتتلقى قدراً ناقصاً من رسول مناعي قوي يدعى نوع I من الإنترفيرون. النتيجة هي فشل مزدوج: الخلايا التائية مُنهكة، ومدرِّبوها الرئيسيون غير قادرين على إيقاظها بشكل صحيح.
جزيء جسر لإعادة ربط الحلفاء المناعيين
صمم الباحثون بروتين اندماجي واحد سموه مصلّب شطرين يربط الخلايا الشجرية والخلايا التائية (BiDT) لمعالجة المشكلتين معاً. أحد طرفي BiDT عبارة عن جسم مضاد يتعرف على TIM3 على الخلايا التائية المنهكة. والطرف الآخر نسخة معدلة من إنترفيرون-ألفا تنشط الخلايا الشجرية بقوة عبر مستقبلات الإنترفيرون لديها لكنها مُعدَّلة لتقليل التأثيرات غير المرغوبة في أنحاء الجسم الأخرى. عند إعطاء BiDT لفئران حاملة للأورام، يتراكم داخل الأورام حيث TIM3 وفير على الخلايا التائية. هناك، يعمل حرفياً كجسر بين الخلايا الشجرية والخلايا التائية المنهكة، يجبرهما على الاقتراب من بعضهما البعض بينما يحول الخلايا الشجرية إلى حالة أكثر نشاطاً وتحفيزاً.
القاتلون المستعادون وذاكرة مناعية دائمة
بمجرد إقامة هذا الجسر، تعزز الخلايا الشجرية إشارات «التنبيه المساعد» الرئيسية على سطحها وتساعد الخلايا التائية على إعادة تشغيل مسارات البقاء والنمو. تبدأ الخلايا التائية المنهكة بالظهور والتصرف كالمقاتلين الفعّالين: تعبر عن بروتينات بقاء أكثر (ممّا يقلل احتمال موتها)، تستعيد إنتاج جزيئات مهمة مثل IL-2 والإنترفيرون-غاما، وتتوسع عدديًا. في نماذج سرطان القولون والورم الميلانيني لدى الفئران، أدى علاج BiDT غالباً إلى إزالة الأورام القائمة وتحسين البقاء مع إحداث خسارة وزن وسمية جهازية أقل مقارنةً بإعطاء الإنترفيرون وجسم مضاد ضد TIM3 بشكل منفصل. ولافت أن الفئران التي تعافت بواسطة BiDT قاومت إعادة تحدي الورم لاحقاً، وكانت خلايا مناعتها قادرة على نقل الحماية إلى حيوانات أخرى، مما يدل على تكوّن ذاكرة مناعية قوية ومحددة للورم.
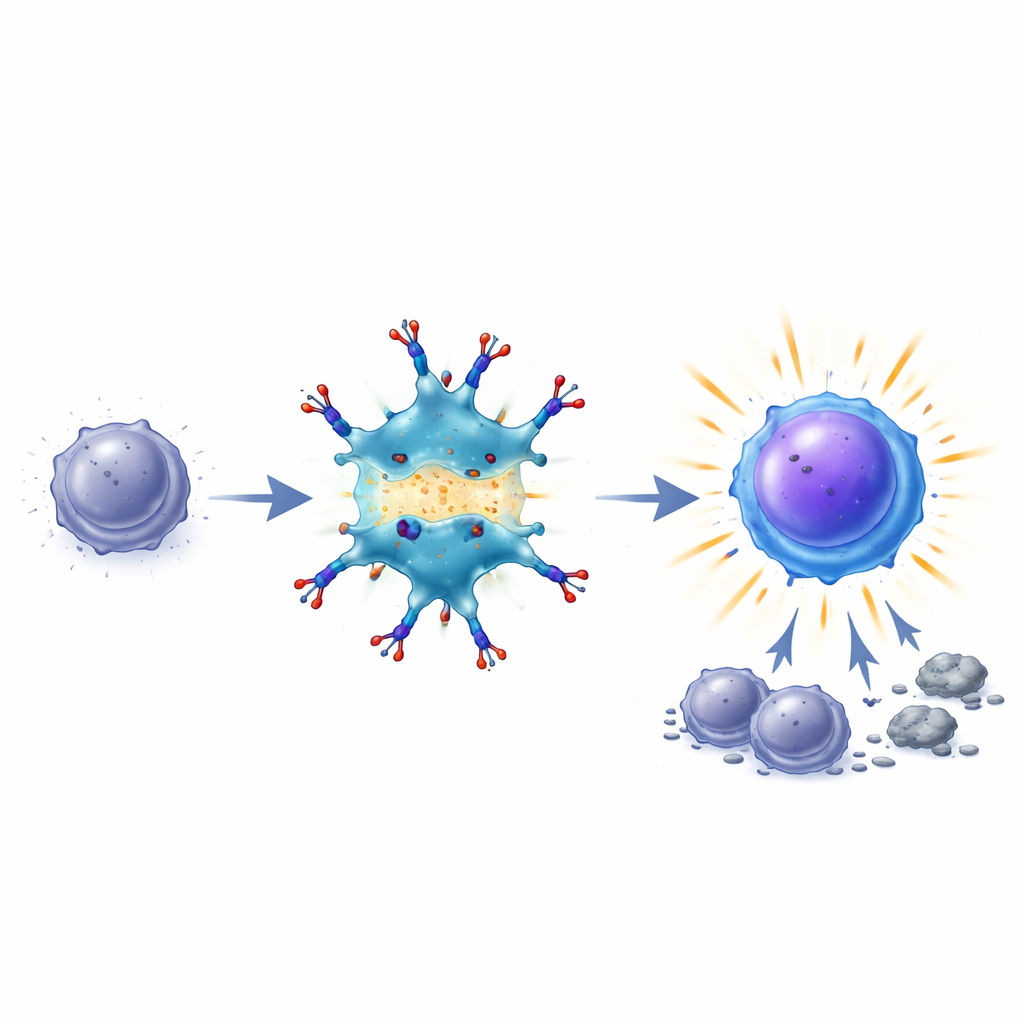
العمل داخل الورم، وليس فقط في العقد اللمفاوية
أظهرت تجارب جينية وتجارب إزالة الخلايا بعناية أن نجاح BiDT يعتمد على خلايا تائية قاتلة وخلايا شجرية موجودة مسبقاً داخل الورم، بدلاً من اعتمادها على خلايا تائية جديدة قادمة من العقد اللمفاوية. يحتاج إشارة الإنترفيرون إلى العمل على الخلايا الشجرية، بينما يكون تفعيل TIM3 على الخلايا التائية حاسماً لإنقاذها. تستجيب الخلايا التائية المعاد تنشيطها بشدة لإشارات IL-2 وتنتج دفعات من الإنترفيرون-غاما، الذي يساعد بدوره في تدمير خلايا الورم. في نموذج ميلانيني «بارد» يقاوم عادةً أدوية نقاط التفتيش القياسية، تغلب BiDT جزئياً على هذا المقاومة. وعند الجمع مع جسم مضاد مانع لـ PD-L1، الذي يزيل كابحاً منفصلاً على الخلايا التائية، قضت المعالجة على الأورام في جزء كبير من الفئران وولدت حماية طويلة الأمد.
نسخ أكثر أماناً وآمال مستقبلية
نظراً لأن العلاجات المعتمدة على الإنترفيرون قد تكون سامة إلى حد كبير لدى المرضى، أنشأ الفريق أيضاً نسخة «برودراغ» تسمى Pro-BiDT، حيث يبقى جزء الإنترفيرون غير نشط حتى يُفصل بواسطة إنزيمات وفيرة في الأورام ونادرة في الأنسجة الصحية. في الفئران، حافظ Pro-BiDT على التأثيرات المضادة للورم القوية للأصل BiDT مع تقليل كبير في علامات الالتهاب وسمية الدم. تشير هذه النتائج مجتمعة إلى طريقة جديدة لعلاج السرطان: بدلاً من مجرد تحرير مكابح الخلايا التائية من الخارج، أعد ربط دوائر الجهاز المناعي داخل الورم بدقة وتنشيطها. إذا أمكن تحقيق نتائج مماثلة في البشر، فقد تساعد مثل هذه الأدوية على إنقاذ الاستجابات المناعية المتعبة، والتغلب على مقاومة العلاجات المناعية الحالية، وتوفير حماية أطول أمداً ضد السرطان.
الاستشهاد: Zhang, X., Gao, Y., Hu, W. et al. Reactivating exhausted tumor-infiltrating T cells by a bispecific DC-T cell engager in mice. Nat Commun 17, 4081 (2026). https://doi.org/10.1038/s41467-026-70876-4
الكلمات المفتاحية: العلاج المناعي للسرطان, إرهاق الخلايا التائية, الخلايا الشجرية, الأجسام المضادة ثنائية النوع, إنترفيرون-ألفا