Clear Sky Science · de
Wiederaktivierung erschöpfter tumorinfiltrierender T‑Zellen durch einen bispezifischen DC‑T‑Zell‑Engager bei Mäusen
Ausgeschaltete Immunzellen wieder aktivieren
Krebs gewinnt oft nicht, weil unser Immunsystem ihn nicht erkennt, sondern weil die tumorbekämpfenden Zellen erschöpfen und ihre Funktion verlieren. Diese Studie an Mäusen beschreibt ein raffiniertes neues Proteinarzneimittel, das zwei zentrale Immunzellen im Tumor physisch miteinander verknüpft, damit sie wieder miteinander kommunizieren können. Dadurch weckt es „erschöpfte“ Killer‑T‑Zellen, verkleinert Tumoren und hinterlässt sogar ein immunologisches Gedächtnis gegen den Tumor, das dessen Wiederauftreten verhindern könnte.
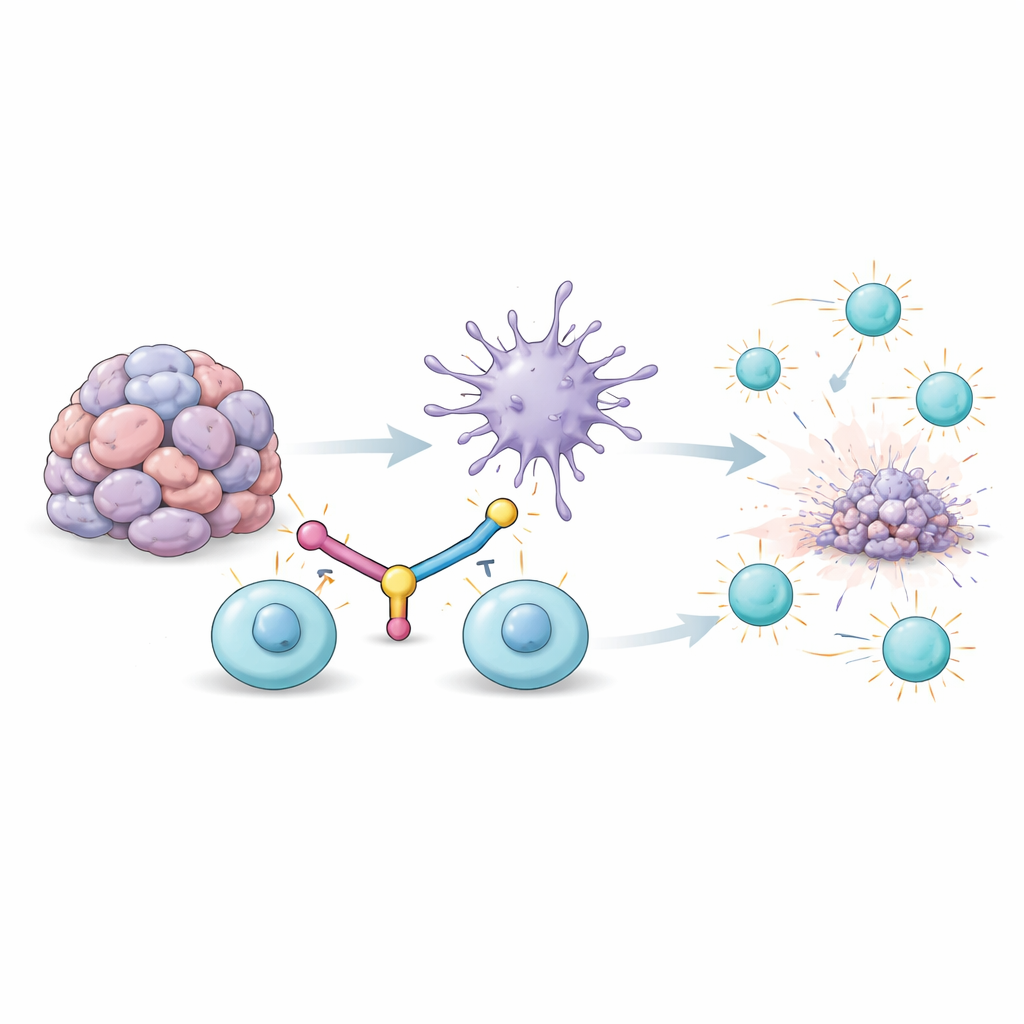
Warum tumorbekämpfende Zellen erschöpfen
Tief im Tumor erkennen und attackieren spezielle weiße Blutkörperchen, die T‑Zellen, Krebszellen. Werden sie jedoch zu lange den Signalen des Tumors ausgesetzt, gelangen sie in einen erschöpften Zustand: Sie teilen sich weniger, produzieren weniger Angriffsmoleküle und sterben möglicherweise vermehrt ab. Ein Oberflächenprotein, das mit dieser Erschöpfung verbunden ist, heißt TIM3. Gleichzeitig sollten dendritische Zellen die T‑Zellen anleiten, indem sie ihnen Tumorfragmente zeigen und starke „An‑“Signale geben. Im Tumormilieu sind dendritische Zellen jedoch häufig geschwächt und erhalten zu wenig eines mächtigen Immunbotens namens Typ‑I‑Interferon. Das Ergebnis ist ein doppeltes Versagen: T‑Zellen sind erschöpft, und ihre wichtigsten Lehrzellen können sie nicht richtig wieder wecken.
Ein Brückenmolekül, das Immunverbündete wieder verbindet
Die Forscher entwarfen ein einzelnes Fusionsprotein, einen bispezifischen DC–T‑Zell‑Engager (BiDT), um beide Probleme gleichzeitig zu beheben. Ein Ende des BiDT ist ein Antikörper, der TIM3 auf erschöpften T‑Zellen erkennt. Das andere Ende ist eine modifizierte Form von Interferon‑alpha, die dendritische Zellen über ihren Interferonrezeptor stark aktiviert, aber so angepasst ist, dass unerwünschte Wirkungen im übrigen Körper reduziert werden. Wird BiDT an tumortragende Mäuse verabreicht, reichert es sich im Tumor an, wo TIM3 auf T‑Zellen reichlich vorhanden ist. Dort überbrückt es dendritische Zellen und erschöpfte T‑Zellen, bringt sie in engen Kontakt und schaltet gleichzeitig die dendritischen Zellen in einen aktiveren, stimulierenden Zustand.
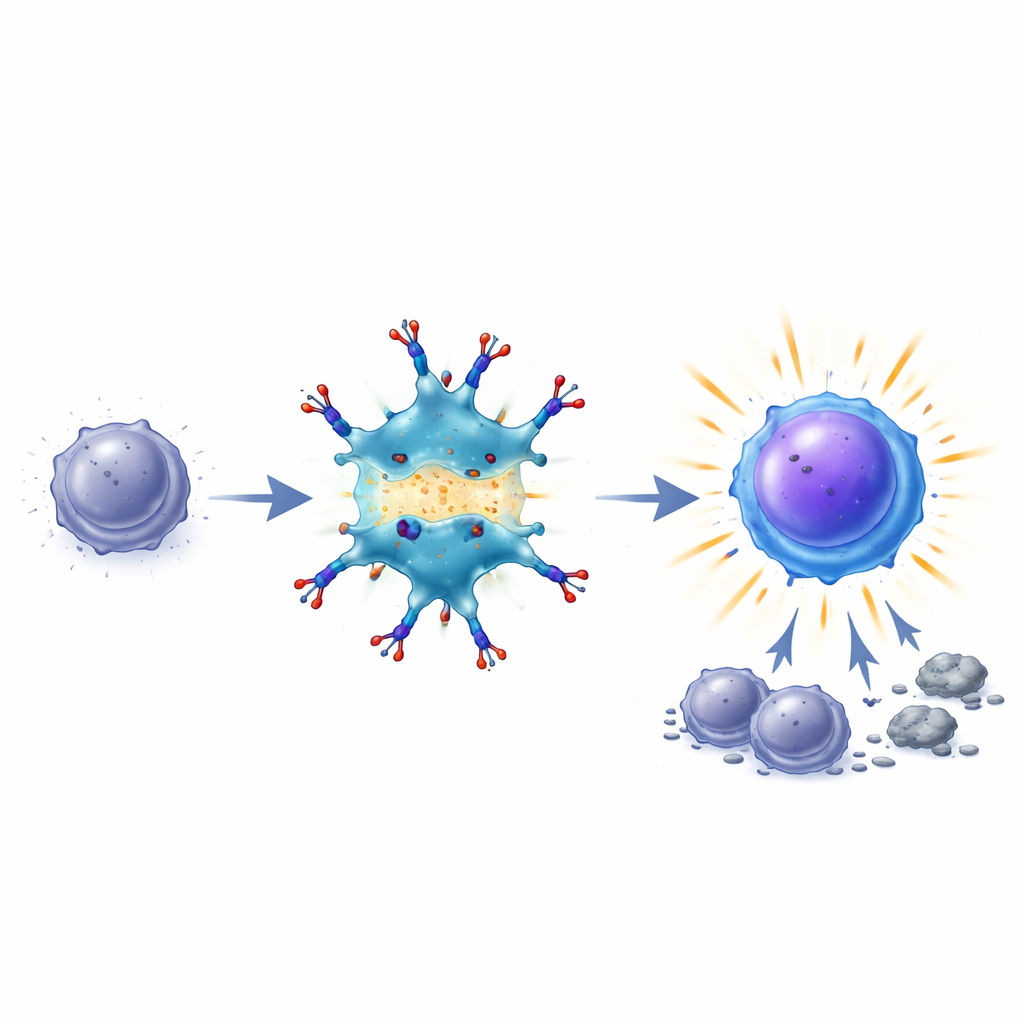
Wiedererweckte Killer und anhaltendes immunologisches Gedächtnis
Sobald diese Brücke besteht, erhöhen dendritische Zellen zentrale „Kostimulations“signale an ihrer Oberfläche und helfen T‑Zellen, Überlebens‑ und Wachstumspfade wieder zu aktivieren. Erschöpfte T‑Zellen beginnen, wieder wie effektive Kämpfer auszusehen und zu funktionieren: Sie exprimieren mehr Überlebensproteine (sind also weniger anfällig für Zelltod), stellen wieder wichtige Moleküle wie IL‑2 und Interferon‑gamma her und vergrößern ihre Zahl. In Mausmodellen von Darmkrebs und Melanom beseitigte die BiDT‑Behandlung häufig etablierte Tumoren und verbesserte das Überleben, wobei sie weniger Gewichtsverlust und geringere systemische Toxizität verursachte als die getrennte Gabe von Interferon und TIM3‑Antikörper. Bemerkenswerterweise widerstanden mit BiDT geheilte Mäuse einer späteren Tumorneuimplantation, und ihre Immunzellen konnten Schutz auf andere Tiere übertragen — ein Hinweis darauf, dass ein robustes, tumorspezifisches Gedächtnis entstanden war.
Wirken im Tumor, nicht nur in den Lymphknoten
Sorgfältige genetische und Depletions‑Experimente zeigten, dass BiDTs Erfolg von bereits vorhandenen Killer‑T‑Zellen und dendritischen Zellen im Tumor abhängt und nicht von frisch aus Lymphknoten zugewanderten T‑Zellen. Das Interferonsignal muss auf dendritische Zellen wirken, während die Bindung an TIM3 auf T‑Zellen für deren Rettung entscheidend ist. Die wiedererweckten T‑Zellen reagieren stark auf IL‑2‑Signale und produzieren Schübe von Interferon‑gamma, was wiederum zur Zerstörung von Tumorzellen beiträgt. In einem „kalten“ Melanommodell, das normalerweise Standard‑Checkpoint‑Therapien widersteht, überwand BiDT diese Resistenz teilweise. In Kombination mit einem PD‑L1‑blockierenden Antikörper, der eine andere Bremse an T‑Zellen entfernt, beseitigte die Therapie bei einem beträchtlichen Anteil der Mäuse Tumoren und erzeugte lang anhaltenden Schutz.
Sicherere Versionen und Ausblick
Da interferonbasierte Behandlungen beim Menschen recht toxisch sein können, entwickelten die Autoren außerdem eine „Prodrug“‑Variante, Pro‑BiDT, bei der der Interferon‑Teil inaktiv bleibt, bis er von Enzymen abgespalten wird, die in Tumoren reichlich vorhanden, in gesundem Gewebe jedoch selten sind. Bei Mäusen bewahrte Pro‑BiDT die starken antitumoralen Effekte des ursprünglichen BiDT und verringerte gleichzeitig deutlich Entzündungszeichen und Bluttoxizität. Insgesamt deuten diese Ergebnisse auf einen neuen Behandlungsansatz hin: Anstatt nur äußere Bremsen an T‑Zellen zu lösen, die Immunkreisläufe präzise innerhalb des Tumors wieder zu verbinden und zu stärken. Sollten sich ähnliche Resultate beim Menschen erzielen lassen, könnten solche Wirkstoffe erschöpfte Immunantworten retten, Resistenzen gegen aktuelle Immuntherapien überwinden und länger anhaltenden Schutz gegen Krebs bieten.
Zitation: Zhang, X., Gao, Y., Hu, W. et al. Reactivating exhausted tumor-infiltrating T cells by a bispecific DC-T cell engager in mice. Nat Commun 17, 4081 (2026). https://doi.org/10.1038/s41467-026-70876-4
Schlüsselwörter: Krebsimmuntherapie, T‑Zell‑Erschöpfung, Dendritische Zellen, bispezifische Antikörper, Interferon‑alpha