Clear Sky Science · pl
Polipeptyd związany z rakiem sprzężony z chromosomem X (XCP) z lncRNA1456 modyfikuje aktywność demetylazy histonowej PHF8, by regulować epigenom, ekspresję genów i ścieżki komórkowe w raku piersi
Ukryte przesłania w „śmieciowym” genomie
Przez lata dużą część naszego DNA uznawano za „śmieci”, ponieważ nie kodowała ona oczywistych białek. To badanie pokazuje, że część tego przeoczonego materiału genetycznego potrafi w rzeczywistości wytwarzać silne, wcześniej nieznane białka, które kształtują rozwój nowotworów. Odkrycie jednego takiego białka w guzach piersi ujawnia nową warstwę kontroli genów i wskazuje nowe możliwości diagnostyki oraz terapii.
Małe białko ukryte na widoku
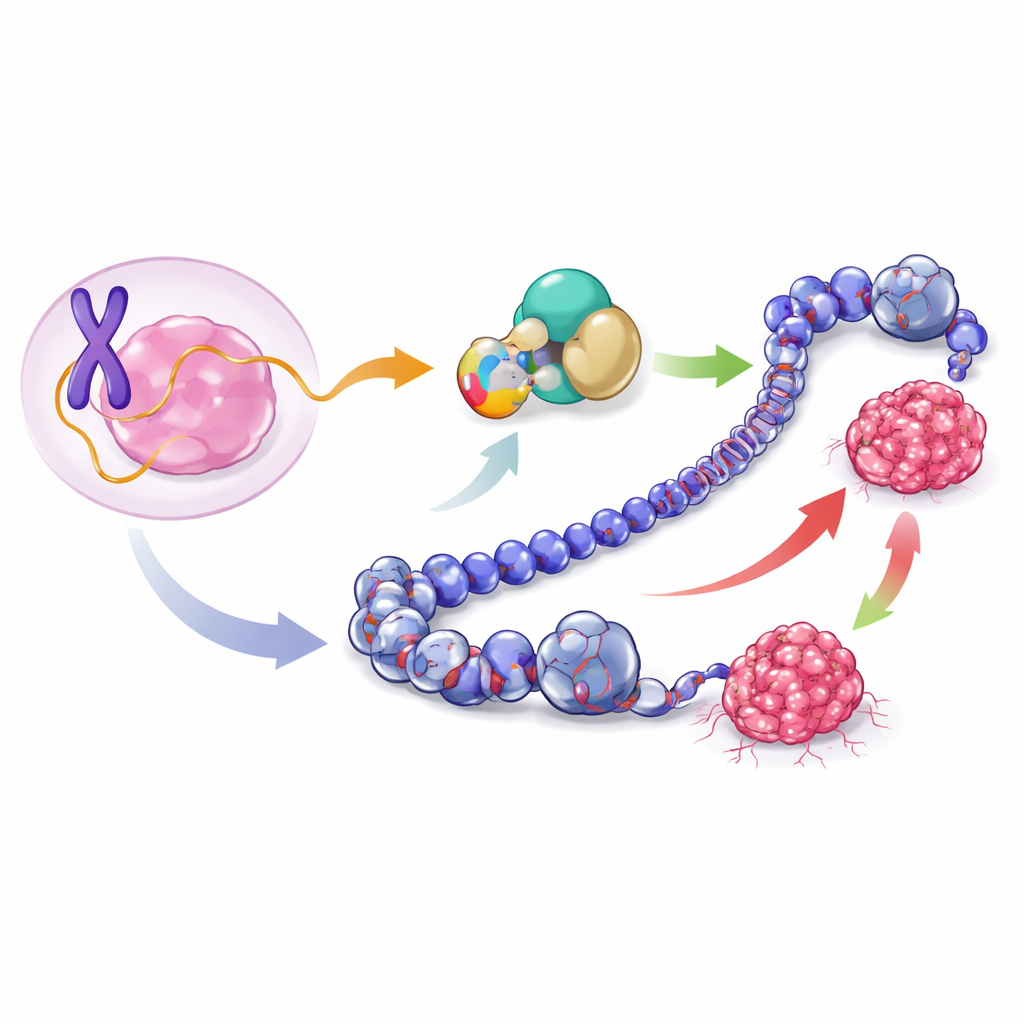
Zespół skupił się na odcinku DNA na chromosomie X, od dawna uważanym za kodujący jedynie RNA niekodujący, nazwany lncRNA1456. Przy użyciu kombinacji sekwencjonowania RNA i metod wykrywania białek odkryli, że to RNA faktycznie niesie instrukcje dla krótkiego białka złożonego ze 132 aminokwasów, które nazwali XCP (X-linked Cancer-associated Polypeptide). XCP powstaje z regionu obejmującego pierwsze dwa segmenty, czyli eksony, tego RNA. W komórkach raka piersi typu luminalnego — powszechnego, typowo wrażliwego na hormony podtypu — XCP jest produkowany obficie i występuje głównie w jądrze komórkowym, gdzie znajduje się DNA i kontrolowana jest aktywność genów.
Gdzie XCP pojawia się w organizmie i w guzach
Aby sprawdzić, czy XCP nie jest artefaktem laboratoryjnym, badacze przeanalizowali wiele normalnych ludzkich tkanek. Stwierdzili, że lncRNA1456 i jego białko XCP są naturalnie aktywne niemal wyłącznie w jądrach i trzustce. W przeciwieństwie do tego, w próbkach raka piersi z dużych zbiorów pacjentów lncRNA1456 i XCP są silnie włączone w guzach, ale ledwie wykrywalne w zdrowej tkance piersi. W obrębie raków piersi wysokie poziomy XCP występują najczęściej w mniej agresywnych nowotworach dodatnich receptorów hormonalnych (typy luminal A, luminal B i HER2-wzbogacone) i są rzadkie w bardziej agresywnych nowotworach typu basalnego. Ten wzorzec sugeruje, że komórki nowotworowe mogą nieprawidłowo aktywować normalnie ściśle ograniczony gen sprzężony z X, przekształcając niezwykłe białko związane z jądrem w białko związane z rakiem.
Jak XCP kieruje wzrostem guza
Następnie autorzy zapytali, co XCP właściwie robi w komórkach nowotworowych. Zaprojektowali linie komórkowe raka piersi, by na żądanie wytwarzały dodatkowy XCP, i wszczepili te komórki do myszy, aby tworzyły guzy. W komórkach luminalnych MCF-7 nadmiar XCP przyspieszał wzrost guza, co sugeruje, że XCP może działać jak onkogen w tym kontekście. Zaskakująco, kiedy to samo białko było wymuszone w komórkach typu basalnego MDA-MB-231, guzy rosły wolniej, co wskazuje na rolę supresorową w tym otoczeniu. Analiza globalnej aktywności genów w powstałych guzach pokazała, że XCP włącza i wyłącza różne zbiory genów i ścieżek w każdym typie komórek: w komórkach luminalnych wzmacnia programy cyklu komórkowego i wzrostu, podczas gdy w komórkach basalnych tłumi szlaki związane z inwazją i przebudową tkanki. Tak więc jedno małe białko może kierować rakiem w przeciwnych kierunkach w zależności od środowiska komórkowego.
Molekularny partner, który przepisuje kod epigenetyczny
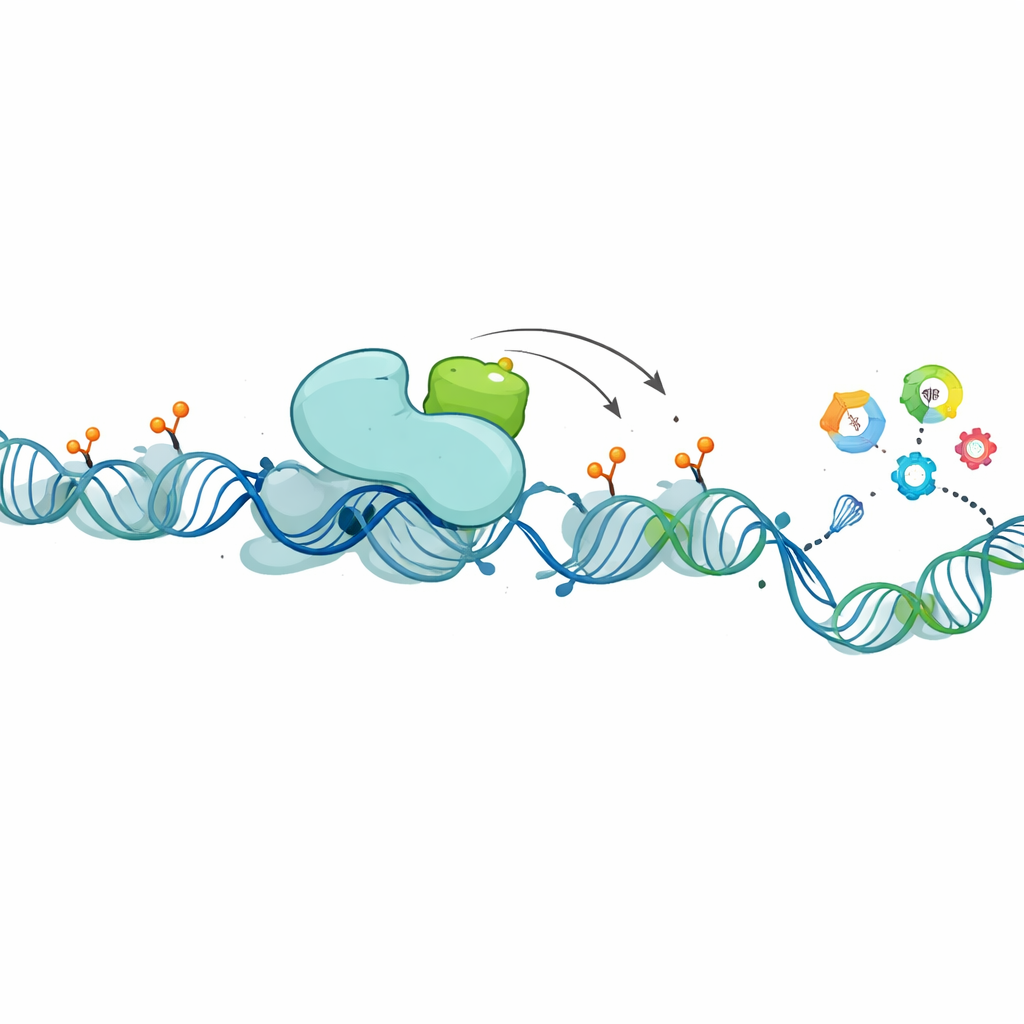
Pogłębiając badania, naukowcy poszukiwali białek fizycznie współdziałających z XCP w jądrze. Skoncentrowali się na PHF8, znanym „wymazywaczu” pewnych chemicznych znaczników na białkach histonowych — szpulach, wokół których owinięte jest DNA. Te znaczniki pomagają określić, czy pobliskie geny są aktywne czy wyciszone. PHF8, podobnie jak XCP, jest kodowany na chromosomie X, jest wysoce eksprymowany w jądrach i podniesiony w raku piersi typu luminalnego. Eksperymenty wykazały, że XCP i PHF8 wiążą się ze sobą i często występują w tych samych tkankach oraz podtypach guzów. Gdy zespół zredukował poziomy lncRNA1456 (a więc XCP), przyczepność PHF8 do DNA osłabła w setkach regionów kontrolnych genów, a wiele z tych genów zmieniło swoją aktywność. W testach biochemicznych PHF8 samodzielnie jedynie umiarkowanie usuwał określony represyjny znacznik z histonów, ale w obecności XCP stał się znacznie bardziej wydajny, a efekt wzmocnienia rósł wraz z ilością XCP. W komórkach ekspresja normalnej wersji lncRNA1456 obniżała te represyjne znaki w całym genomie, natomiast mutant niezdolny do produkcji XCP tego nie robił, podkreślając, że to białko — nie tylko RNA — napędza efekt.
Dlaczego to odkrycie ma znaczenie
Ta praca ujawnia, że gen kiedyś oznaczony jako niekodujący faktycznie produkuje małe, lecz wpływowe białko, które współpracuje z enzymem epigenetycznym, aby przekształcać aktywność wielu genów w raku piersi. XCP pomaga PHF8 wiązać się z chromatyną i zwiększa jego zdolność do usuwania hamujących chemicznych znaków, zmieniając ścieżki związane z wzrostem w sposób zależny od kontekstu. Dla szerokiej publiczności kluczowy przekaz jest taki, że nasz genom wciąż skrywa ukryte białka o znaczącym wpływie na choroby. XCP jest jednym z takich przykładów: białko sprzężone z chromosomem X związane z jądrem, które, gdy zostanie nieprawidłowo ekspresjonowane w raku piersi, może albo napędzać, albo hamować wzrost guza poprzez precyzyjne dostrajanie sposobu, w jaki czytana jest książka instrukcji DNA. W miarę jak naukowcy dalej badają te „ukryte” białka, mogą odkryć nowe biomarkery i cele leków, które były niewidoczne, gdy duże fragmenty genomu odrzucono jako niekodujące.
Cytowanie: Gadad, S.S., Camacho, C.V., Gong, X. et al. X-linked cancer-associated polypeptide (XCP) from lncRNA1456 modulates PHF8 histone demethylase activity to regulate the epigenome, gene expression, and cellular pathways in breast cancer. Oncogene 45, 1557–1571 (2026). https://doi.org/10.1038/s41388-026-03740-w
Słowa kluczowe: rak piersi, RNA niekodujące, epigenetyka, mikroproteiny, demetylaza histonowa