Clear Sky Science · fr
Polypeptide associé au cancer lié au chromosome X (XCP) issu de lncRNA1456 module l'activité de la déméthylase des histones PHF8 pour réguler l'épi-génome, l'expression génique et les voies cellulaires dans le cancer du sein
Messages cachés dans le « génome poubelle »
Pendant des années, une grande partie de notre ADN a été qualifiée de « poubelle » parce qu'elle ne semblait pas coder de protéines. Cette étude montre qu'une partie de ce matériau génétique négligé peut en réalité produire de puissantes protéines jusque-là inconnues qui influencent la croissance des cancers. En identifiant l'une de ces protéines dans des tumeurs mammaires, les chercheurs mettent au jour un niveau supplémentaire de contrôle génique et ouvrent des perspectives nouvelles pour le diagnostic et le traitement.
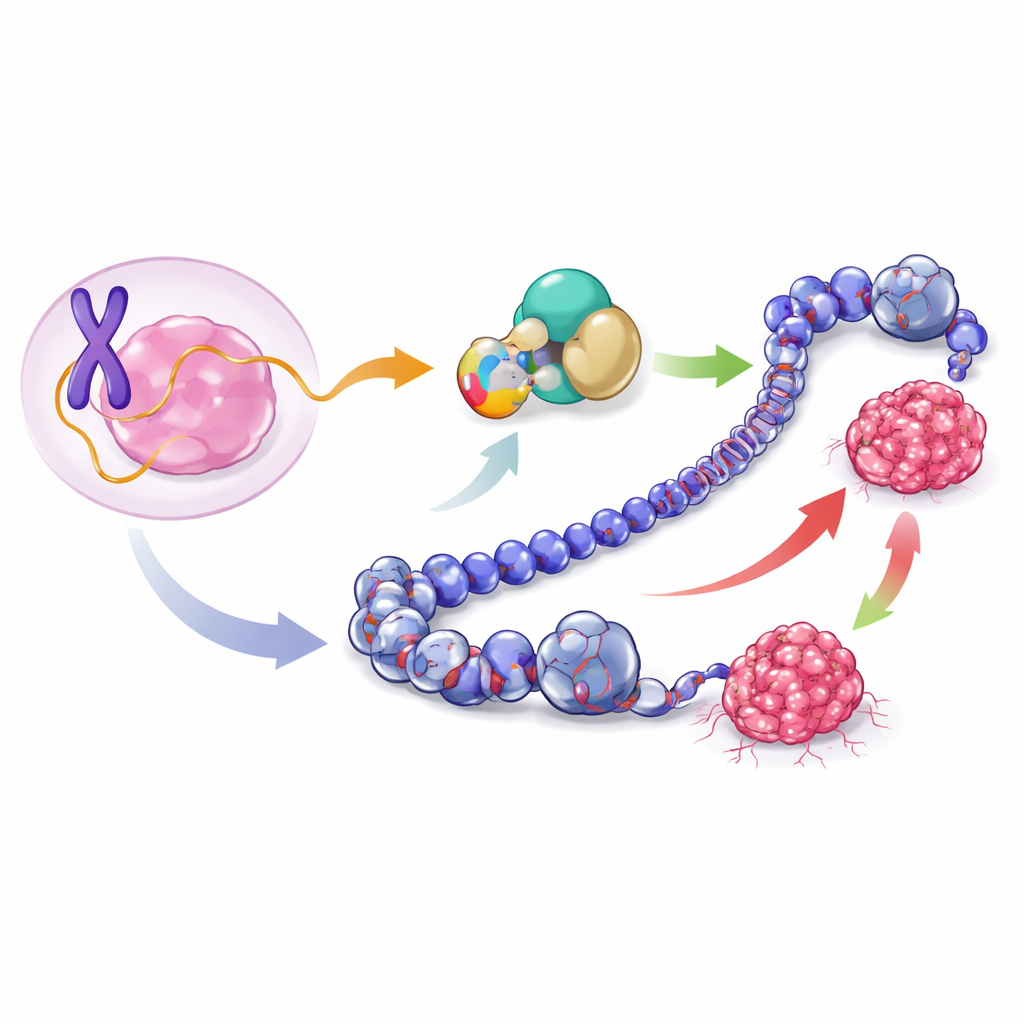
Une petite protéine cachée en pleine vue
L'équipe s'est concentrée sur une portion d'ADN du chromosome X longtemps supposée ne produire qu'un ARN non codant, nommé lncRNA1456. En combinant séquençage de l'ARN et méthodes de détection des protéines, ils ont découvert que cet ARN porte en réalité l'information pour une courte protéine de 132 acides aminés, qu'ils ont nommée XCP (Polypeptide associé au cancer lié au X). XCP est issu d'une région couvrant les deux premiers segments, ou exons, de l'ARN. Dans les cellules mammaires de type luminal — un sous-type fréquent et généralement sensible aux hormones — XCP est abondamment produit et se trouve principalement dans le noyau cellulaire, où est logé l'ADN et où s'exerce le contrôle de l'activité génique.
Où apparaît XCP dans l'organisme et dans les tumeurs
Pour vérifier si XCP n'était pas un artefact de laboratoire, les chercheurs ont examiné de nombreux tissus humains normaux. Ils ont constaté que lncRNA1456 et sa protéine XCP sont naturellement actifs presque exclusivement dans le testicule et le pancréas. En revanche, dans des échantillons de cancer du sein issus de larges bases de données de patients, lncRNA1456 et XCP sont fortement activés dans les tumeurs mais à peine détectables dans le tissu mammaire sain. Au sein des cancers du sein, de forts niveaux de XCP apparaissent surtout dans les tumeurs moins agressives, positives pour les récepteurs hormonaux (types luminal A, luminal B et enrichi en HER2), et sont rares dans les tumeurs de type basal plus agressives. Ce profil suggère que les cellules cancéreuses peuvent activer de manière inappropriée un gène lié au chromosome X normalement très restreint, transformant une protéine associée au testicule en une protéine associée au cancer.
Comment XCP oriente la croissance tumorale
Les auteurs se sont ensuite demandés ce que XCP fait réellement aux cellules cancéreuses. Ils ont modifié des lignées de cellules mammaires pour produire XCP en excès sur commande et ont implanté ces cellules chez la souris pour former des tumeurs. Dans les cellules luminales MCF-7, un excès de XCP a accéléré la croissance tumorale, ce qui suggère que XCP peut agir comme un oncogène dans ce contexte. De manière surprenante, lorsque la même protéine a été forcée d'être exprimée dans des cellules de type basal MDA-MB-231, les tumeurs ont crû plus lentement, laissant entrevoir un rôle suppressif dans ce contexte. En analysant l'activité génique globale dans les tumeurs résultantes, l'équipe a observé que XCP active et réprime des ensembles de gènes et de voies distincts selon le type cellulaire : dans les cellules luminales, il stimule les programmes du cycle cellulaire et de croissance, tandis que dans les cellules basales il atténue les voies liées à l'invasion et au remodelage tissulaire. Ainsi, une seule petite protéine peut orienter le cancer dans des directions opposées selon l'environnement cellulaire.
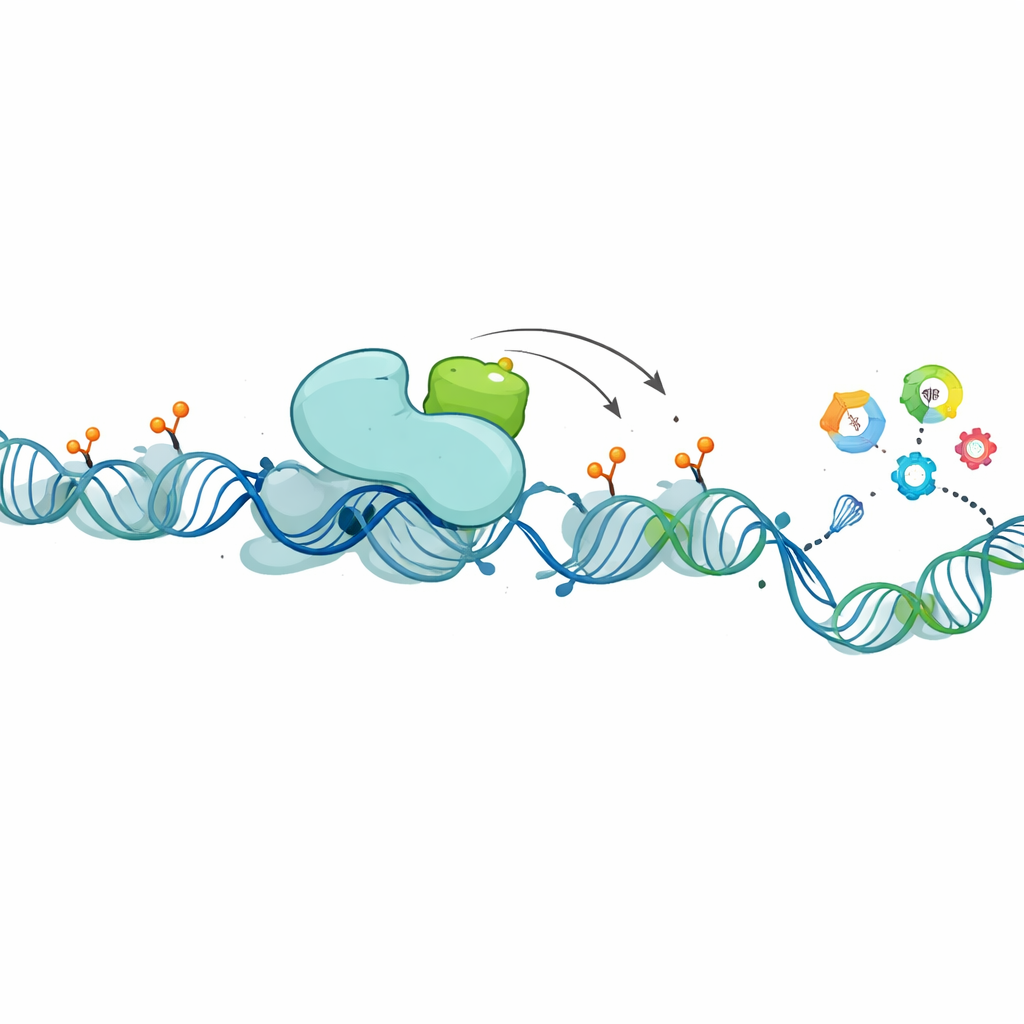
Un partenaire moléculaire qui réécrit le code épigénétique
En approfondissant, les chercheurs ont cherché les protéines qui s'associent physiquement à XCP dans le noyau. Ils ont ciblé PHF8, un « effaceur » connu de certaines marques chimiques sur les histones — les bobines autour desquelles l'ADN s'enroule. Ces marques contribuent à déterminer si les gènes proches sont actifs ou silencieux. PHF8, comme XCP, est codé sur le chromosome X, fortement exprimé dans le testicule et augmenté dans les cancers du sein luminales. Les expériences ont montré que XCP et PHF8 se lient l'un à l'autre et sont souvent présents dans les mêmes tissus et sous-types tumoraux. Lorsque l'équipe a réduit les niveaux de lncRNA1456 (et donc de XCP), l'attachement de PHF8 à l'ADN a diminué sur des centaines de régions régulatrices de gènes, et beaucoup de ces gènes ont modifié leur activité. Dans des tests biochimiques, PHF8 seul n'enlevait qu'avec modestie une marque répressive particulière des histones, mais en présence de XCP il devenait bien plus efficace, et cet effet d'augmentation croissait avec la quantité de XCP. Dans les cellules, l'expression d'une version normale de lncRNA1456 réduisait ces marques répressives à l'échelle du génome, alors qu'une version mutante incapable de produire XCP ne le faisait pas, ce qui souligne que c'est la protéine — et non l'ARN seul — qui est à l'origine de l'effet.
Pourquoi cette découverte importe
Ce travail révèle qu'un gène jadis qualifié de non codant produit en réalité une petite protéine influente qui s'associe à une enzyme épigénétique pour remodeler l'activité de nombreux gènes dans le cancer du sein. XCP aide PHF8 à se lier à la chromatine et renforce sa capacité à éliminer des marques chimiques inhibitrices, modifiant des voies liées à la croissance de manière dépendante du contexte. Pour un public général, le message clé est que notre génome recèle encore des protéines cachées ayant un impact substantiel sur la maladie. XCP en est un exemple : une protéine liée au chromosome X et au testicule qui, lorsqu'elle est mal exprimée dans le cancer du sein, peut soit alimenter soit freiner la croissance tumorale en ajustant finement la lecture du livre d'instructions de l'ADN. À mesure que les scientifiques poursuivent l'exploration de ces protéines « cachées », ils pourraient découvrir de nouveaux biomarqueurs et cibles thérapeutiques qui étaient invisibles lorsque de larges portions du génome étaient écartées comme non codantes.
Citation: Gadad, S.S., Camacho, C.V., Gong, X. et al. X-linked cancer-associated polypeptide (XCP) from lncRNA1456 modulates PHF8 histone demethylase activity to regulate the epigenome, gene expression, and cellular pathways in breast cancer. Oncogene 45, 1557–1571 (2026). https://doi.org/10.1038/s41388-026-03740-w
Mots-clés: cancer du sein, ARN non codant, épigénétique, microprotéines, déméthylase des histones