Clear Sky Science · de
X-chromosomal, krebserregendes Polypeptid (XCP) aus lncRNA1456 moduliert die Aktivität der Histon-Demethylase PHF8 zur Regulierung des Epigenoms, der Genexpression und zellulärer Signalwege beim Brustkrebs
Verborgene Botschaften im „junk“ Genom
Lange Zeit wurde ein großer Teil unserer DNA als „Junk“ abgetan, weil er offenbar keine Proteine kodierte. Diese Studie zeigt, dass ein Teil dieses übersehenen genetischen Materials tatsächlich mächtige, bisher unbekannte Proteine produzieren kann, die das Wachstum von Tumoren beeinflussen. Durch die Entdeckung eines solchen Proteins in Brusttumoren legen die Forschenden eine neue Ebene der Genregulation offen und weisen auf neue Möglichkeiten für Diagnose und Therapie hin.
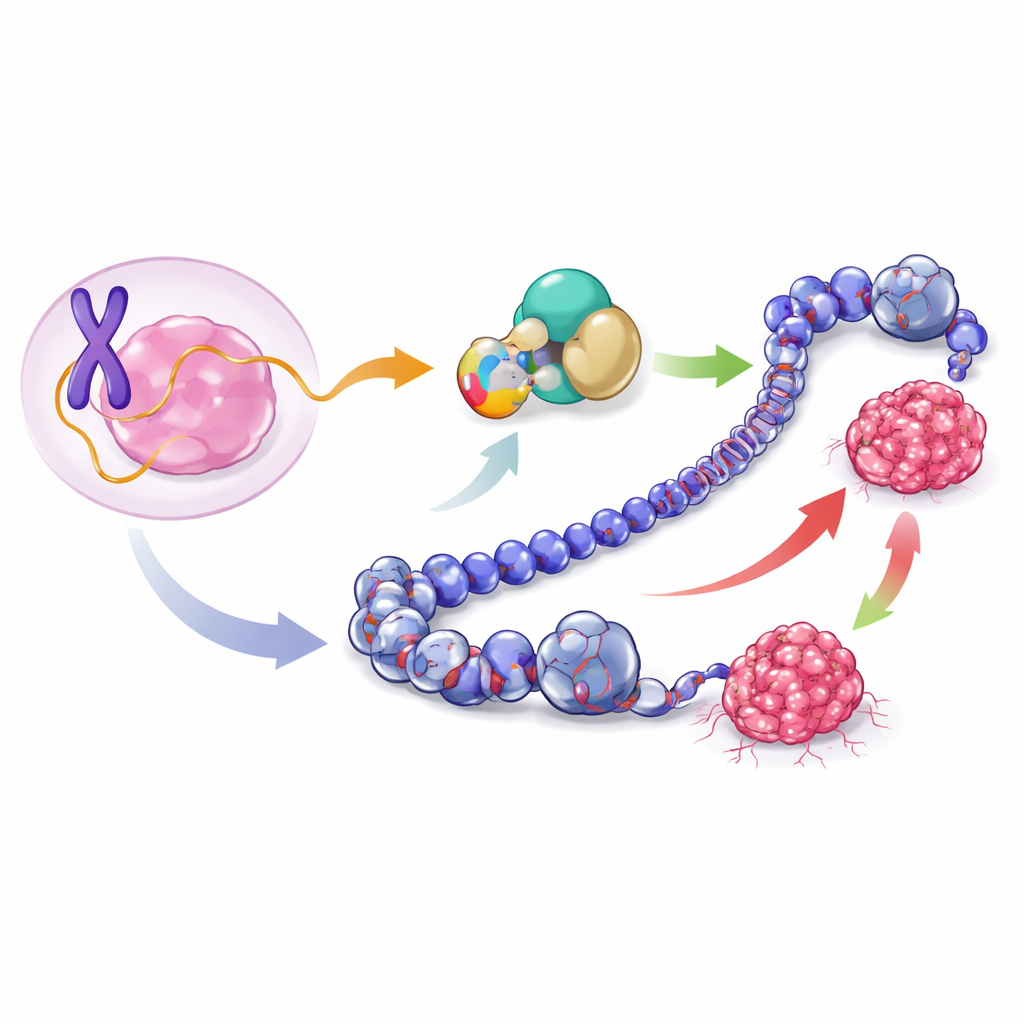
Ein kleines Protein, das im Offensichtlichen verborgen liegt
Das Team konzentrierte sich auf einen Abschnitt der DNA auf dem X-Chromosom, von dem lange angenommen wurde, er würde nur eine nichtkodierende RNA namens lncRNA1456 produzieren. Mithilfe einer Kombination aus RNA-Sequenzierung und Proteinnachweismethoden entdeckten sie, dass diese RNA tatsächlich die Information für ein kurzes Protein aus 132 Aminosäuren enthält, das sie XCP (X-chromosomal Cancer-associated Polypeptide) nannten. XCP wird aus einem Bereich produziert, der die ersten beiden Segmente, die Exons, der RNA umfasst. In luminalen Brustkrebszellen — einem häufigen, typischerweise hormonempfindlichen Subtyp — wird XCP reichlich produziert und findet sich hauptsächlich im Zellkern, wo die DNA liegt und die Genaktivität gesteuert wird.
Wo XCP im Körper und in Tumoren vorkommt
Um zu prüfen, ob XCP nur ein Laborartefakt ist, untersuchten die Forschenden viele normale menschliche Gewebe. Sie fanden, dass lncRNA1456 und sein Protein XCP natürlicherweise nahezu ausschließlich in Hoden und Bauchspeicheldrüse aktiv sind. Im Gegensatz dazu sind in Brustkrebsproben aus großen Patientendatensätzen lncRNA1456 und XCP in Tumoren stark hochreguliert, während sie im gesunden Brustgewebe kaum nachweisbar sind. Innerhalb von Brustkrebserkrankungen treten hohe XCP-Werte am häufigsten in weniger aggressiven, hormonrezeptorpositiven Tumoren auf (luminal A, luminal B und HER2-positiv) und sind in aggressiveren Basaltypen selten. Dieses Muster legt nahe, dass Krebszellen ein sonst eng eingeschränktes X-chromosomales Gen fehlaktivieren und dadurch ein ungewöhnliches, normalerweise mit den Hoden assoziiertes Protein zu einem krebsassoziierten Protein machen.
Wie XCP das Tumorwachstum steuert
Die Autoren fragten anschließend, was XCP tatsächlich in Krebszellen bewirkt. Sie konstruierten Brustkrebszelllinien, die auf Befehl zusätzliches XCP produzieren, und setzten diese Zellen in Mäuse ein, um Tumoren wachsen zu lassen. In luminalen MCF-7-Zellen beschleunigte zusätzliches XCP das Tumorwachstum, was darauf hindeutet, dass XCP in diesem Kontext wie ein Onkogen wirken kann. Überraschenderweise verlangsamte dasselbe Protein, wenn es in basale MDA-MB-231-Zellen exprimiert wurde, das Tumorwachstum, was auf eine tumorunterdrückende Rolle in diesem Umfeld hindeutet. Durch die Analyse der globalen Genaktivität in den entstehenden Tumoren zeigte das Team, dass XCP in den beiden Zelltypen jeweils unterschiedliche Gen- und Signalwegsets an- und abschaltet: In luminalen Zellen fördert es Zellzyklus- und Wachstumsprogramme, während es in basalen Zellen Signalwege dämpft, die mit Invasion und Geweberemodellierung verknüpft sind. Somit kann ein einzelnes kleines Protein das Krebsverhalten je nach zellulärem Umfeld in entgegengesetzte Richtungen lenken.
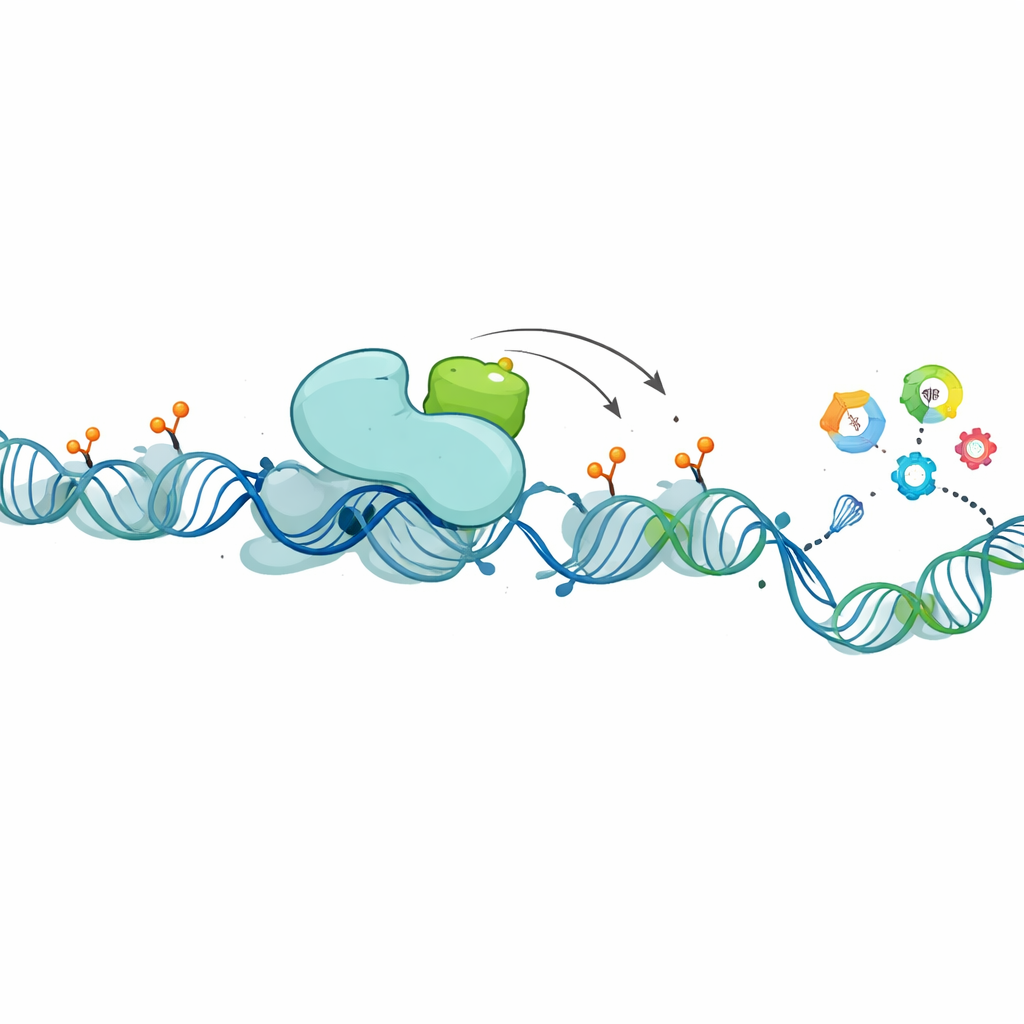
Ein molekularer Partner, der den epigenetischen Code umschreibt
Bei tiefergehenden Untersuchungen suchten die Forschenden nach Proteinen, die physisch mit XCP im Zellkern assoziieren. Sie konzentrierten sich auf PHF8, einen bekannten „Radiergummi“ für bestimmte chemische Markierungen auf Histonproteinen — den Spulen, um die DNA gewickelt ist. Diese Markierungen helfen zu bestimmen, ob nahegelegene Gene aktiv oder still sind. PHF8, wie XCP, ist auf dem X-Chromosom kodiert, wird stark in den Hoden exprimiert und ist in luminalen Brustkrebserkrankungen erhöht. Experimente zeigten, dass XCP und PHF8 aneinander binden und häufig in denselben Geweben und Tumoruntertypen vorkommen. Wenn das Team lncRNA1456 (und damit XCP) reduzierte, schwächte sich PHF8s Bindung an die DNA an Hunderten von Genregulatorregionen, und viele dieser Gene veränderten ihre Aktivität. In biochemischen Tests entfernte PHF8 allein nur mäßig eine bestimmte repressive Markierung von Histonen, in Anwesenheit von XCP wurde es jedoch deutlich effizienter, und dieser Verstärkungseffekt nahm mit steigenden XCP-Mengen zu. In Zellen senkte die Expression einer normalen lncRNA1456 diese repressiven Markierungen im gesamten Genom, während eine mutierte Version, die kein XCP produzieren kann, dies nicht tat — ein Hinweis darauf, dass das Protein und nicht nur die RNA den Effekt verursacht.
Warum diese Entdeckung wichtig ist
Diese Arbeit zeigt, dass ein einst als nichtkodierend eingestuftes Gen tatsächlich ein kleines, aber einflussreiches Protein produziert, das mit einem epigenetischen Enzym zusammenarbeitet, um die Aktivität vieler Gene beim Brustkrebs neu zu gestalten. XCP unterstützt PHF8 bei der Bindung an Chromatin und verstärkt seine Fähigkeit, hemmende chemische Markierungen zu entfernen, wodurch wachstumsbezogene Signalwege kontextabhängig verändert werden. Für ein allgemeines Publikum ist die Kernbotschaft: Unser Genom enthält noch versteckte Proteine mit erheblicher Bedeutung für Krankheiten. XCP ist ein solches Beispiel: ein hodenspezifisches X‑chromosom‑Protein, das bei Fehlregulation im Brustkrebs entweder das Tumorwachstum fördert oder hemmt, indem es fein abstimmt, wie das DNA‑Instruktionsbuch gelesen wird. Während Forschende diese „verborgenen“ Proteine weiter untersuchen, könnten sie neue Biomarker und Wirkstoffziele entdecken, die unsichtbar blieben, als große Teile des Genoms als nichtkodierend abgetan wurden.
Zitation: Gadad, S.S., Camacho, C.V., Gong, X. et al. X-linked cancer-associated polypeptide (XCP) from lncRNA1456 modulates PHF8 histone demethylase activity to regulate the epigenome, gene expression, and cellular pathways in breast cancer. Oncogene 45, 1557–1571 (2026). https://doi.org/10.1038/s41388-026-03740-w
Schlüsselwörter: Brustkrebs, nichtkodierende RNA, Epigenetik, Mikroproteine, Histon-Demethylase