Clear Sky Science · ar
ببتيد مرتبط بالسرطان على الصبغي X (XCP) من lncRNA1456 يضبط نشاط مديِّل الهيستون PHF8 لتنظيم المعلومات فوق الجينية، التعبير الجيني والمسارات الخلوية في سرطان الثدي
رسائل مخفية في «الجينوم القمامة»
لسنوات، أُهمل كثير من حمضنا النووي على أنه «قمامة» لأنه لم يكن يُظهر بوضوح أنه يُشفِّر بروتينات. تُبيّن هذه الدراسة أن بعض تلك المادة الوراثية المتجاهلة بإمكانها بالفعل إنتاج بروتينات قوية وغير معروفة سابقًا تشكّل طريقة نمو السرطانات. من خلال كشفهم لبروتين واحد من هذا النوع في أورام الثدي، يكشف الباحثون عن طبقة جديدة للتحكم الجيني ويشيرون إلى احتمالات جديدة للتشخيص والعلاج.
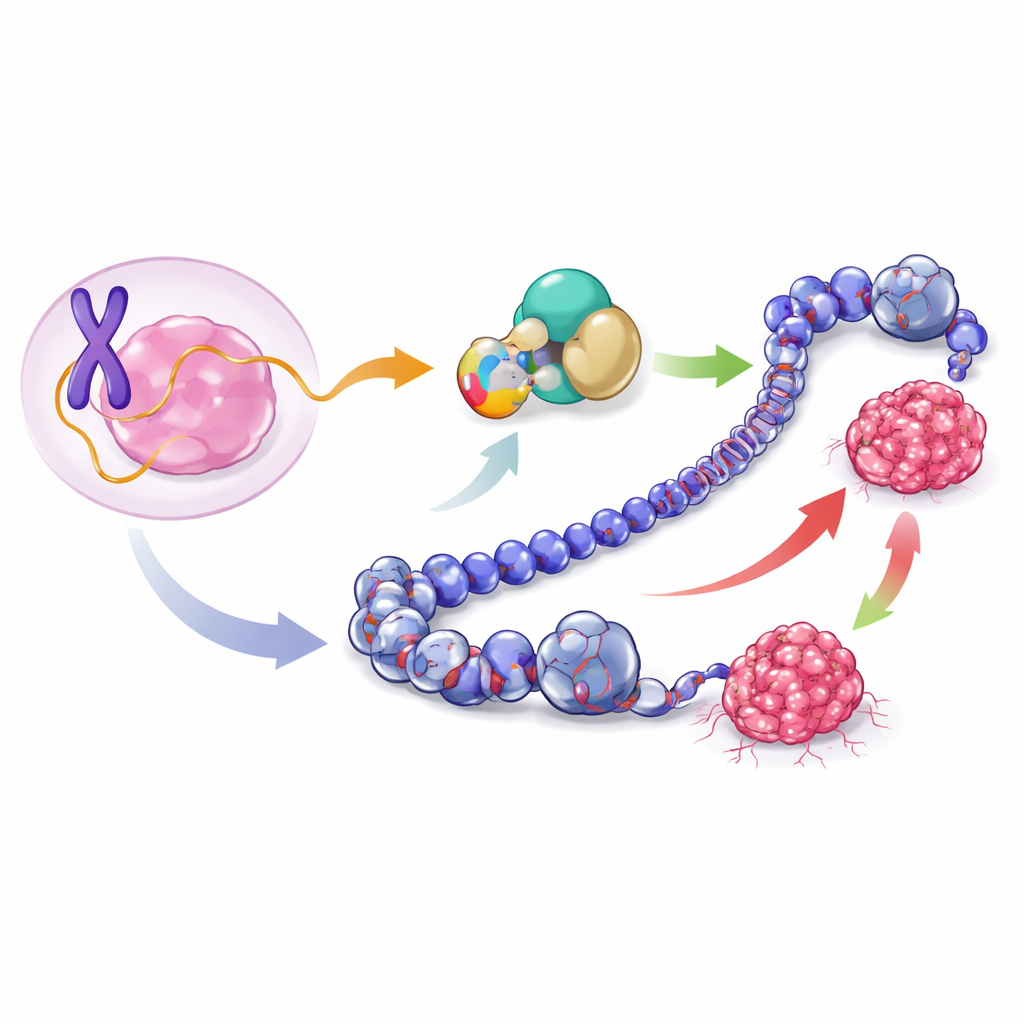
بروتين صغير مختفٍ في العلن
ركّز الفريق على مقطع من الحمض النووي على الكروموسوم X اعتُقد طويلاً أنه يصنع فقط جزيء رنا غير مشفر يُدعى lncRNA1456. باستخدام مزيج من تسلسل الرنا وطرق كشف البروتينات، اكتشفوا أن هذا الرنا يحمل فعلاً تعليمات لبروتين قصير مكوَّن من 132 وحدة بنائية، أطلقوا عليه اسم XCP (الببتيد المرتبط بالسرطان على الصبغي X). يُنتَج XCP من منطقة تمتد عبر القِطعَتين الأوليين، أو إكسونات، من الرنا. في خلايا سرطان الثدي من النوع اللمعي—وهو نوع شائع وحسّاس عادةً للهرمونات—يُنتج XCP بكثرة ويُوجد بشكل أساسي في نواة الخلية، حيث يُحاط الحمض النووي وتُضبط نشاطات الجينات.
أين يظهر XCP في الجسم وفي الأورام
للتحقق مما إذا كان XCP مجرد أثر مخبري، مسح الباحثون العديد من الأنسجة البشرية الطبيعية. وجدوا أن lncRNA1456 وبروتينه XCP نشطان طبيعياً تقريباً فقط في الخصية والبنكرياس. بالمقابل، في عينات سرطان الثدي من مجموعات بيانات مرضى واسعة، تكون lncRNA1456 وXCP مشغلتين بشدة في الأورام لكن بالكاد تُكشف في نسيج الثدي السليم. داخل سرطانات الثدي، تظهر مستويات عالية من XCP غالباً في الأورام الأقل عدوانية والمعتمدة على مستقبلات الهرمونات (أنواع لمعية A وB ونوع معزز HER2) ونادرة في الأورام القاعدية الأكثر عدوانية. يشير هذا النمط إلى أن خلايا السرطان قد تفعّل خطأً جيناً مربوطاً بالكروموسوم X كان مقيداً بشدة في الظروف الطبيعية، محوّلةً بروتيناً مرتبطاً بالخصية إلى بروتين مرتبط بالسرطان.
كيف يوجّه XCP نمو الورم
سأل المؤلفون بعد ذلك ما الذي يفعله XCP فعلياً بخلايا السرطان. صنعوا خطوط خلايا سرطان ثدي مُعدّلة لإنتاج XCP إضافي عند الطلب وزرعوا هذه الخلايا في فئران لتشكيل أورام. في خلايا MCF-7 اللمعية، سرّعت زيادة XCP نمو الورم، مما يوحي بأن XCP يمكن أن يتصرف كجين مُسبّب للسرطان في هذا السياق. على نحو مفاجئ، عندما أُجبِر نفس البروتين على التعبير في خلايا MDA-MB-231 القاعدية، نمت الأورام ببطء أكبر، ممّا يوحي بدور كابح للورم في تلك الحالة. من خلال تحليل النشاط الجيني الكلي في الأورام الناتجة، رأى الفريق أن XCP يفعّل ويكبّت مجموعات مميزة من الجينات والمسارات في كل نوع خلوي: في الخلايا اللمعية يعزّز برامج دورة الخلية والنمو، بينما في الخلايا القاعدية يُقصّر المسارات المرتبطة بالاقتحام وإعادة تشكيل النسيج. وهكذا يمكن لبروتين صغير واحد أن يوجه السرطان في اتجاهين متعاكسين اعتماداً على البيئة الخلوية.
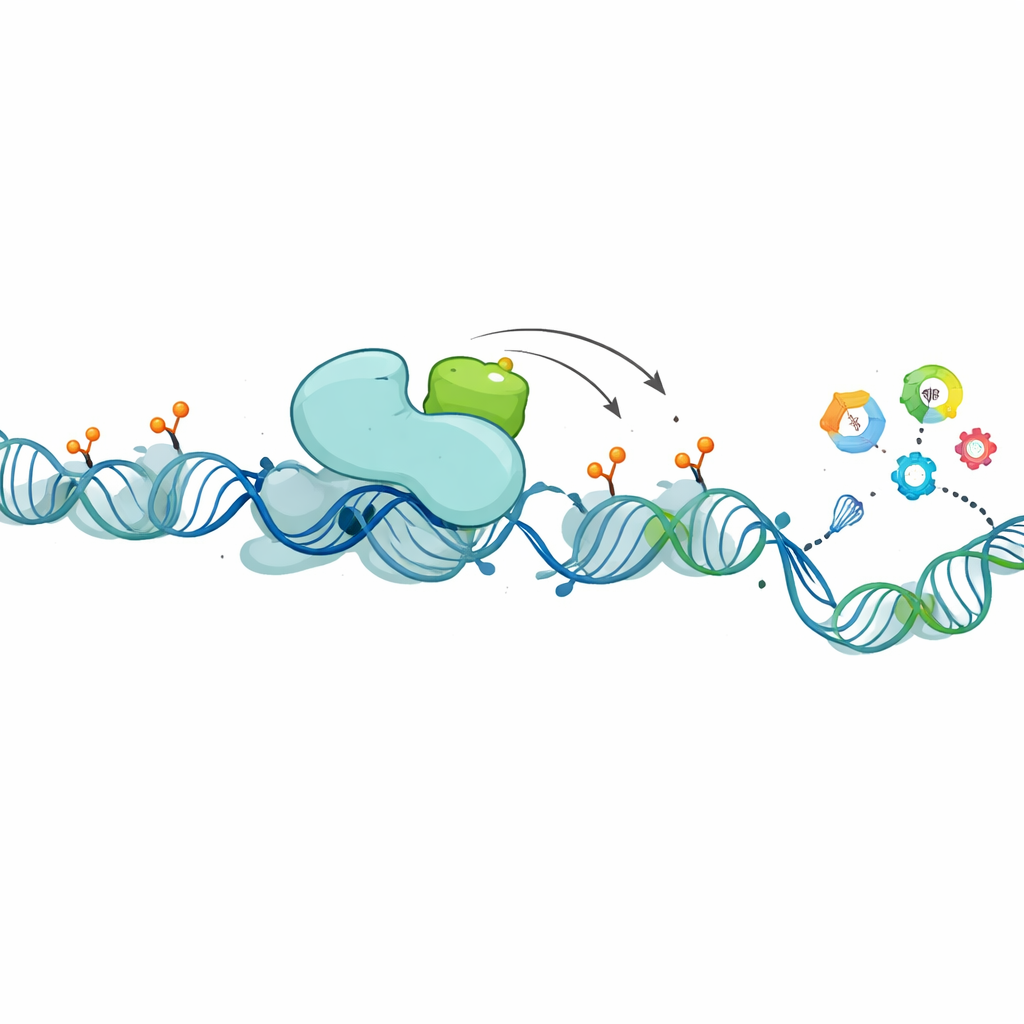
شريك جزيئي يعيد كتابة الشيفرة فوق الجينية
بتعمق أكثر، بحث الباحثون عن بروتينات ترتبط جسدياً بـ XCP في النواة. ركزوا على PHF8، وهو «ممحاة» معروفة لعلامات كيميائية معينة على بروتينات الهيستون—البكرات التي يُلف فيها الحمض النووي. تساعد هذه العلامات في تحديد ما إذا كانت الجينات المجاورة نشطة أم صامتة. PHF8، مثل XCP، مُشفّر على الكروموسوم X، ويُعبَّر عنه بدرجة عالية في الخصية، ويرتفع في سرطانات الثدي اللمعية. أظهرت التجارب أن XCP وPHF8 يرتبطان ببعضهما وغالباً ما يتواجدا في نفس الأنسجة وأنواع الأورام. عندما خفّض الفريق مستويات lncRNA1456 (وبالتالي XCP)، ضعُف تمسُّك PHF8 بالحمض النووي عند مئات مناطق التحكم الجيني، وتغير نشاط كثير من تلك الجينات. في اختبارات بيوكيميائية، أزال PHF8 وحده بشكل متواضع علامة كبح معينة من على الهيستونات، لكن بوجود XCP أصبح أكثر كفاءة بكثير، وازداد هذا التأثير المعزز بزيادة كمية XCP. في الخلايا، أدى التعبير عن نسخة طبيعية من lncRNA1456 إلى خفض هذه العلامات القمعية عبر الجينوم، في حين أن نسخة متحورة غير قادرة على إنتاج XCP لم تفعل ذلك، مما يؤكد أن البروتين—وليس فقط الرنا—هو السبب في التأثير.
لماذا تهمنا هذه الاكتشافات
تكشف هذه العمل عن أن جيناً صنف سابقاً على أنه غير مشفر ينتج فعلاً بروتيناً صغيراً لكنه مؤثر يتعاون مع إنزيم فوق جيني لإعادة تشكيل نشاط العديد من الجينات في سرطان الثدي. يساعد XCP PHF8 على الارتباط بالكروماتين ويعزز قدرته على نزع العلامات الكيميائية المانعة، مطوّراً مسارات متعلقة بالنمو بطريقة تعتمد على السياق. للقراء غير المتخصصين، الرسالة الأساسية هي أن جينومنا لا يزال يحتفظ ببروتينات مخفية ذات تأثير كبير على المرض. XCP مثال على ذلك: بروتين مرتبط بالخصية على صبغي X يمكنه، عند التعبير غير المناسب في سرطان الثدي، أن يعزّز أو يكبح نمو الورم عن طريق ضبط دقيق لكيفية قراءة كتاب تعليمات الحمض النووي. مع استمرار العلماء في استكشاف هذه البروتينات «المخفية»، قد يكتشفون مؤشرات بيولوجية وأهداف علاجية جديدة كانت غير مرئية عندما رُفضت أجزاء واسعة من الجينوم كغير مشفرة.
الاستشهاد: Gadad, S.S., Camacho, C.V., Gong, X. et al. X-linked cancer-associated polypeptide (XCP) from lncRNA1456 modulates PHF8 histone demethylase activity to regulate the epigenome, gene expression, and cellular pathways in breast cancer. Oncogene 45, 1557–1571 (2026). https://doi.org/10.1038/s41388-026-03740-w
الكلمات المفتاحية: سرطان الثدي, حمض نووي ريبوزي غير مشفر, علم فوق الجينات (الابيجينيتيكس), بروتينات صغيرة, مزيل ميثلة الهيستون