Clear Sky Science · it
Polipeptide associato al cancro legato all’X (XCP) da lncRNA1456 modula l’attività della demetilasi istonica PHF8 per regolare l’epigenoma, l’espressione genica e le vie cellulari nel cancro al seno
Messaggi nascosti nel genoma «spazzatura»
Per anni gran parte del nostro DNA è stata liquidata come «spazzatura» perché non sembrava codificare proteine. Questo studio mostra che parte di quel materiale genetico trascurato può in realtà produrre proteine potenti e finora sconosciute che influenzano la crescita dei tumori. Scoprendo una di queste proteine nei tumori mammari, gli autori mettono in luce un nuovo livello di controllo genico e indicano nuove possibilità per diagnosi e terapie.
Una piccola proteina nascosta in bella vista
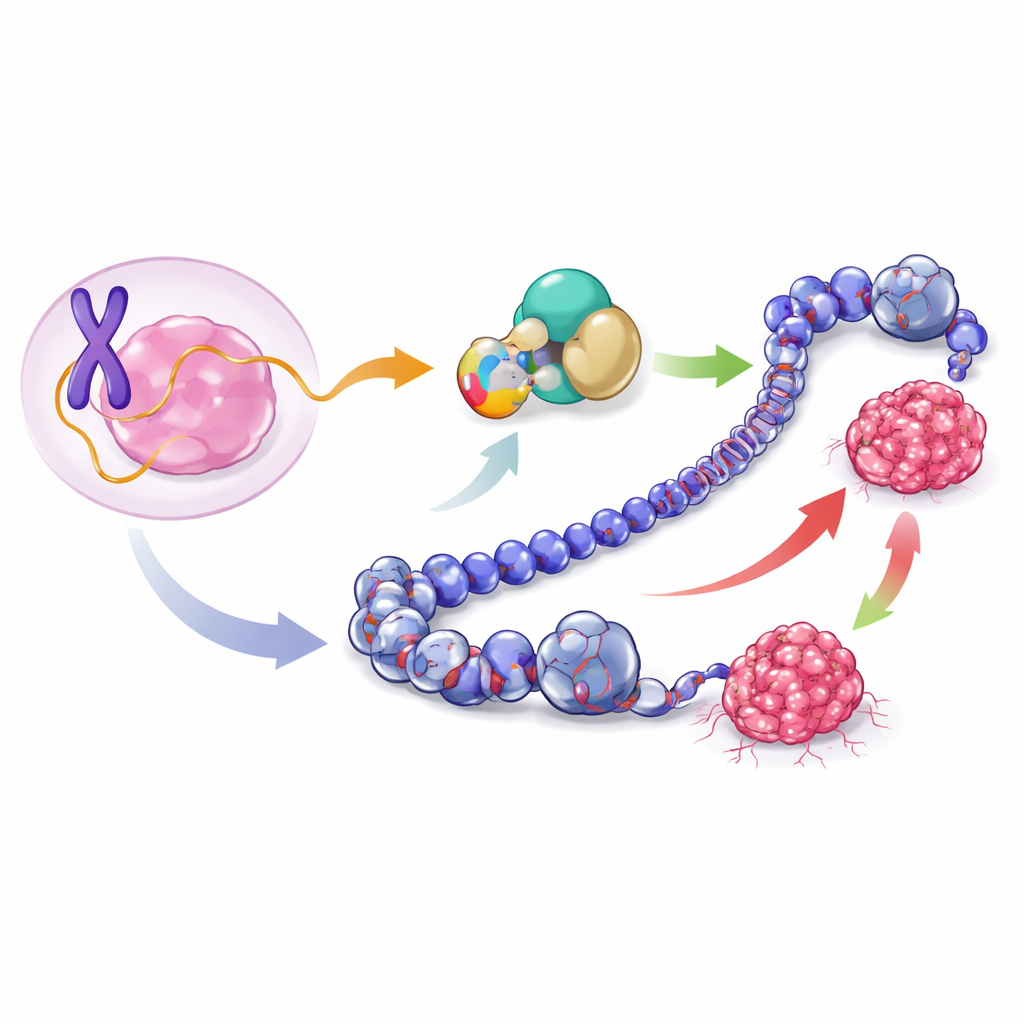
Il gruppo si è concentrato su un tratto di DNA sul cromosoma X da tempo ritenuto capace di produrre solo una molecola di RNA non codificante, chiamata lncRNA1456. Usando una combinazione di sequenziamento dell’RNA e metodi di rilevazione proteica, hanno scoperto che questo RNA in realtà contiene le istruzioni per una breve proteina di 132 amminoacidi, che hanno nominato XCP (Polipeptide associato al cancro legato all’X). XCP viene prodotta da una regione che copre i primi due segmenti, o esoni, dell’RNA. Nelle cellule di cancro al seno di tipo luminale — un sottotipo comune e tipicamente sensibile agli ormoni — XCP è abbondantemente espressa ed è localizzata principalmente nel nucleo cellulare, dove è contenuto il DNA e si controlla l’attività genica.
Dove appare XCP nel corpo e nei tumori
Per verificare se XCP fosse solo un artefatto da laboratorio, i ricercatori hanno esaminato molti tessuti umani normali. Hanno trovato che lncRNA1456 e la sua proteina XCP sono normalmente attivi quasi esclusivamente nel testicolo e nel pancreas. Al contrario, nei campioni di cancro al seno provenienti da grandi dataset di pazienti, lncRNA1456 e XCP sono fortemente attivati nei tumori ma quasi assenti nel tessuto mammario sano. All’interno dei tumori mammari, livelli elevati di XCP compaiono più spesso nei tumori meno aggressivi e positivi per recettori ormonali (tipi luminal A, luminal B e arricchiti per HER2) e sono rari nei tumori di tipo basale più aggressivi. Questo schema suggerisce che le cellule cancerose possono attivare in modo inappropriato un gene legato all’X altrimenti strettamente ristretto, trasformando una proteina tipica del testicolo in una proteina associata al cancro.
Come XCP indirizza la crescita tumorale
Gli autori si sono poi chiesti cosa faccia concretamente XCP nelle cellule tumorali. Hanno ingegnerizzato linee cellulari di cancro al seno per produrre XCP in eccesso su comando e hanno impiantato queste cellule in topi per formare tumori. Nelle cellule luminali MCF-7, l’eccesso di XCP ha accelerato la crescita tumorale, suggerendo che XCP può comportarsi come un oncogene in questo contesto. Sorprendentemente, quando la stessa proteina è stata forzata in cellule di tipo basale MDA-MB-231, i tumori sono cresciuti più lentamente, suggerendo un ruolo oncosoppressivo in quel contesto. Analizzando l’attività genica globale nei tumori risultanti, il gruppo ha osservato che XCP attiva e disattiva insiemi distinti di geni e vie in ciascun tipo cellulare: nelle cellule luminali potenzia programmi legati al ciclo cellulare e alla crescita, mentre nelle cellule basali attenua vie correlate all’invasione e al rimodellamento tissutale. Dunque una singola piccola proteina può spingere il cancro in direzioni opposte a seconda dell’ambiente cellulare.
Un partner molecolare che riscrive il codice epigenetico
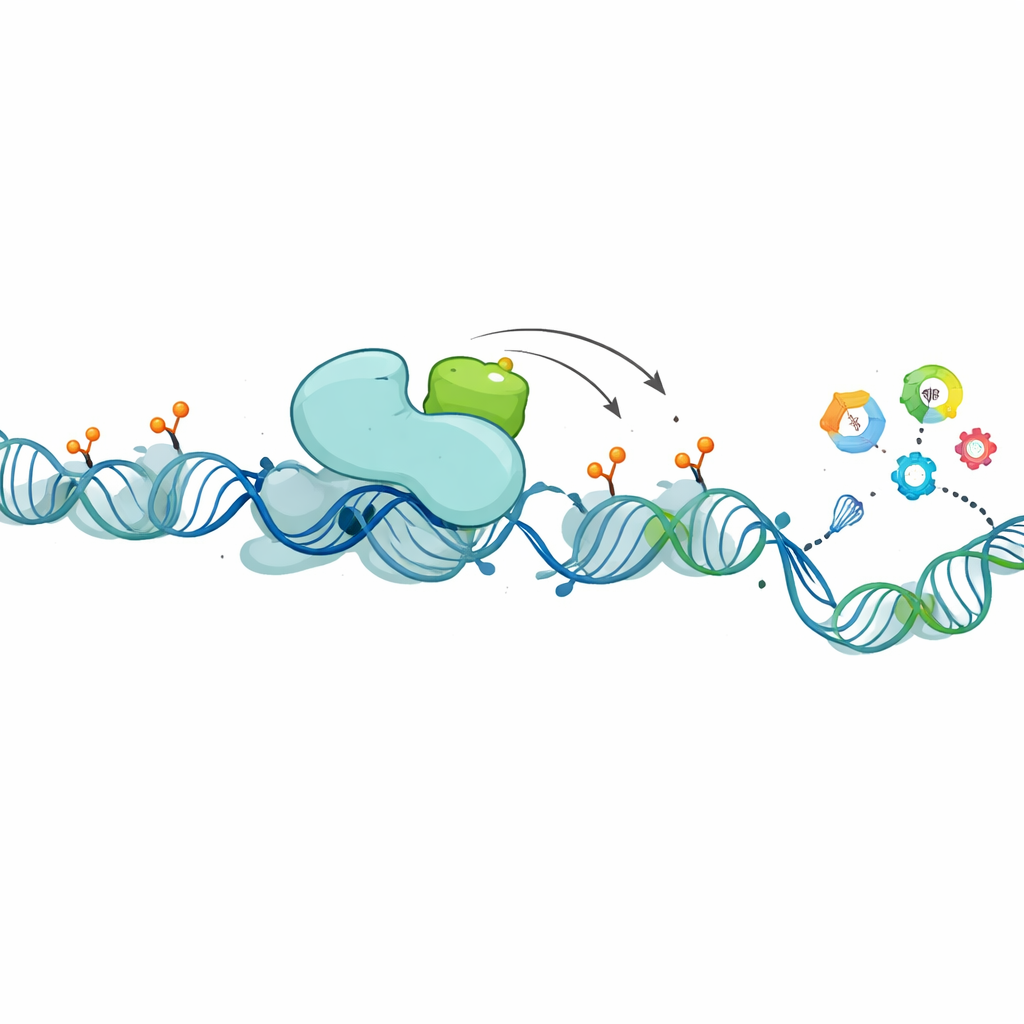
Approfondendo, i ricercatori hanno cercato proteine che si associano fisicamente a XCP nel nucleo. Si sono concentrati su PHF8, un noto «cancellatore» di alcuni marcatori chimici sugli istoni — i rocchetti attorno a cui il DNA è avvolto. Questi marcatori contribuiscono a determinare se i geni vicini sono attivi o silenti. PHF8, come XCP, è codificato sul cromosoma X, è altamente espresso nel testicolo ed è elevato nei tumori mammari luminali. Gli esperimenti hanno mostrato che XCP e PHF8 si legano tra loro e sono spesso presenti negli stessi tessuti e sottotipi tumorali. Quando il team ha ridotto i livelli di lncRNA1456 (e quindi di XCP), l’associazione di PHF8 con il DNA si è indebolita in centinaia di regioni di controllo genico, e molti di quei geni hanno modificato la loro attività. In test biochimici, PHF8 da solo rimuoveva solo modestamente un particolare marcatore repressivo dagli istoni, ma in presenza di XCP è diventato molto più efficiente, e questo effetto potenziatore aumentava con maggiori quantità di XCP. Nelle cellule, l’espressione della versione normale di lncRNA1456 ha abbassato questi marchi repressivi nel genoma, mentre una versione mutante incapace di produrre XCP non lo ha fatto, sottolineando che è la proteina — non solo l’RNA — a guidare l’effetto.
Perché questa scoperta è importante
Questo lavoro rivela che un gene un tempo etichettato come non codificante in realtà produce una piccola ma influente proteina che si allea con un enzima epigenetico per rimodellare l’attività di molti geni nel cancro al seno. XCP aiuta PHF8 a legarsi alla cromatina e ne potenzia la capacità di rimuovere marcatori chimici inibitori, modificando vie legate alla crescita in modo dipendente dal contesto. Per un pubblico generale, il messaggio chiave è che il nostro genoma nasconde ancora proteine sconosciute con un impatto sostanziale sulle malattie. XCP è un esempio: una proteina del cromosoma X legata al testicolo che, se espressa in modo anomalo nel cancro al seno, può sia alimentare sia rallentare la crescita tumorale attraverso una fine regolazione di come viene letto il libro delle istruzioni del DNA. Man mano che gli scienziati continueranno a esplorare queste proteine «nascoste», potrebbero emergere nuovi biomarcatori e bersagli farmacologici che erano invisibili quando vaste porzioni del genoma venivano considerate non codificanti.
Citazione: Gadad, S.S., Camacho, C.V., Gong, X. et al. X-linked cancer-associated polypeptide (XCP) from lncRNA1456 modulates PHF8 histone demethylase activity to regulate the epigenome, gene expression, and cellular pathways in breast cancer. Oncogene 45, 1557–1571 (2026). https://doi.org/10.1038/s41388-026-03740-w
Parole chiave: cancro al seno, RNA non codificante, epigenetica, microproteine, demetilasi istonica