Clear Sky Science · nl
Antimicrobiële resistentie, conjugatieve plasmiden en pathogeniciteit in afvalwater en oppervlaktewater Escherichia spp. in Stockholm, Zweden
Waarom water en microben ertoe doen in het dagelijks leven
De meeste mensen denken bij antibioticaresistentie aan ziekenhuizen, maar deze studie toont hoe het ook gevormd kan worden door het water dat onder onze steden stroomt en tegen onze stranden klotst. Onderzoekers in Stockholm, Zweden volgden bacteriën uit rioolwaterzuiveringsinstallaties en nabijgelegen meren en kustwateren om een eenvoudige maar urgente vraag te stellen: helpen onze afvoeren mee aan de verspreiding van moeilijk te behandelen microben terug in het milieu waar mensen zwemmen, spelen en drinkwater winnen?
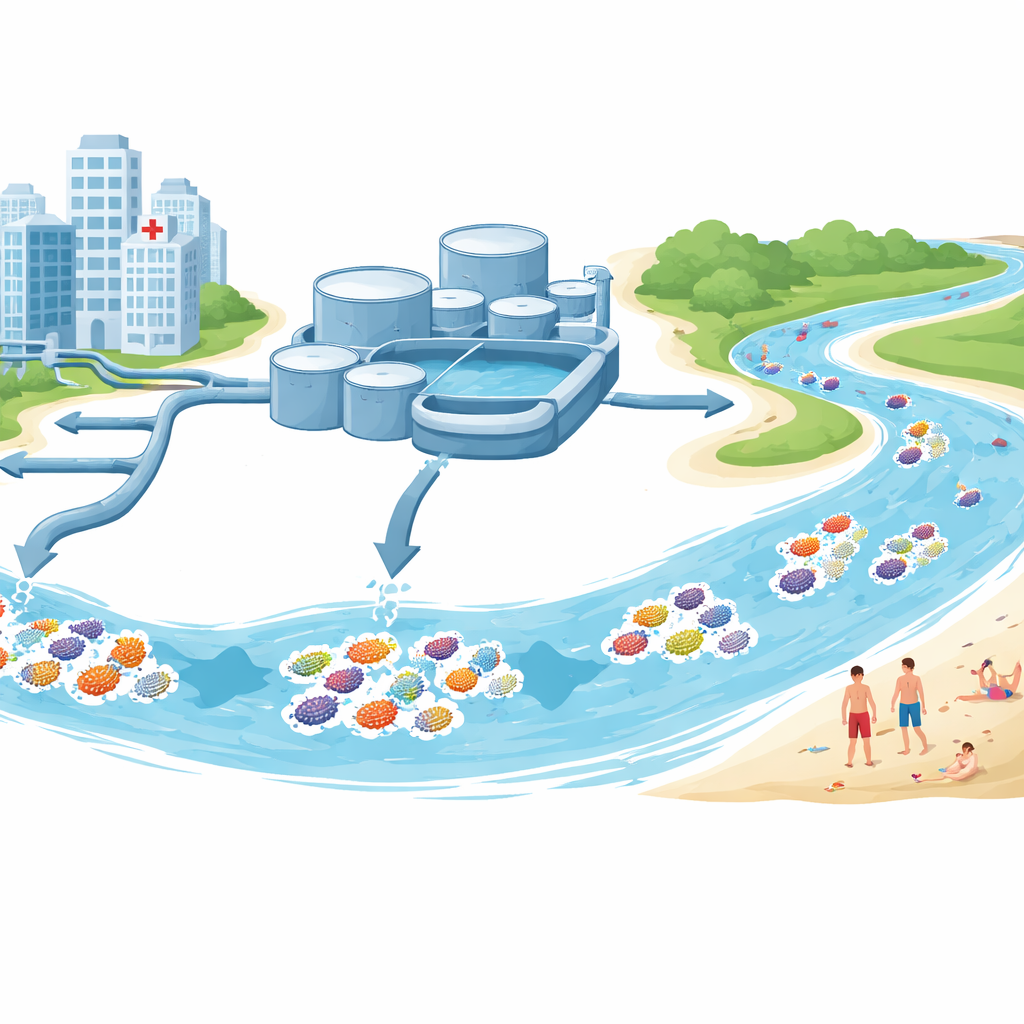
Waar de monsters vandaan kwamen
Het team verzamelde water en sediment in en rond Stockholm tijdens de zomer van 2022. Sommige monsters kwamen uit de inlaten en uitlaten van grote rioolwaterzuiveringsinstallaties die afvalwater van huizen en ziekenhuizen ontvangen. Andere werden genomen uit zoetwatermeren en brakke Baltische zee-stranden die voor recreatie worden gebruikt. Vanuit deze locaties isoleerden ze 68 stammen van Escherichia‑soorten, voornamelijk E. coli, een veelvoorkomende darmbacterie die ook als standaardindicator van fecale verontreiniging wordt gebruikt. Elke stam werd in het laboratorium getest op welke antibiotica hij kon weerstaan en vervolgens op DNA‑niveau ontleed om zijn resistentiegenen, ziekte-gerelateerde genen en de kleine DNA‑cirkelvormige plasmiden die tussen bacteriën kunnen springen, te onthullen.
Sterkere resistentie in rioolwater dan in natuurlijke wateren
Het contrast tussen rioolwater en natuurlijke wateren was opvallend. Meer dan de helft van de E. coli‑stammen uit afvalwater was resistent tegen ten minste drie klassen antibiotica, en veel droegen clusters van resistentiegenen, waaronder genen die derde‑generatie cefalosporinen uitschakelen. Met name genen uit de CTX‑M‑familie, en vooral de CTX‑M‑15‑variant, kwamen veel voor in afvalwaterstammen maar waren volledig afwezig bij stammen afkomstig uit meren en stranden. Verschillende afvalwaterbacteriën behoorden tot bekende lijnages die urineweginfecties en bloedbaaninfecties bij mensen veroorzaken, waaronder de wereldwijd problematische ST131‑groep, en deze droegen enkele van de zwaarste resistentiebelasting.
Antibioticaresten en mobiel DNA
Chemische tests van het water lieten zien dat antibioticaresten consequent hoger waren in inlaten en uitlaten van rioolwater dan op natuurlijke locaties. De concentraties van het middel ciprofloxacine bij één inlaat en één uitlaat overschreden gepubliceerde drempels waarboven resistentie naar verwachting bevorderd wordt. Dit chemische decor is belangrijk omdat veel resistentiegenen zich op conjugatieve plasmiden bevonden—mobiele DNA‑cirkels die van de ene bacterie naar de andere kunnen bewegen. In laboratorium‑kruisingsexperimenten transferreerden plasmiden van 16 stammen met succes naar een standaard ontvangerstam, waarbij ze vaak resistentie tegen meerdere middelen tegelijk meenamen. Plasmiden van bepaalde families, met name IncN en IncI, bewogen met bijzonder hoge efficiëntie, wat suggereert dat ze krachtige voertuigen zijn voor de verspreiding van resistentie in de drukbevolkte, voedingsrijke omgeving van rioolsystemen.
Ziekte‑gerelateerde eigenschappen in alledaagse wateren
Naast geneesmiddelresistentie zochten de wetenschappers in de genomen genomen naar genen die E. coli helpen ziekte te veroorzaken, zoals die voor toxines, adhesines die bacteriën laten hechten aan de darm of urinewegen, en factoren die hen in de bloedbaan beschermen. Veel afvalwaterisolaten droegen combinaties van genen die typisch zijn voor extra‑intestinale en urineweggpathogenen, een patroon dat echoot met wat in klinische infecties wordt gezien. Verrassend genoeg droeg een groot deel van de E. coli uit ogenschijnlijk schone meren en stranden ook enkele van deze virulentiegenen, hoewel ze over het algemeen minder resistentiegenen en geen genen voor uitgebreid spectrum beta‑lactamase hadden. De studie vond ook milieugerelateerde soorten zoals Escherichia marmotae die ziekte‑geassocieerde genen droegen, wat suggereert dat wilde dieren en natuurlijke wateren potentiële reservoirs van pathogenen kunnen vormen.
Wat dit betekent voor mensen en beleid
Samengevoegd schetsen de bevindingen rioolwaterzuiveringsinstallaties als belangrijke kruisplaatsen waar menselijke, dierlijke en milieu‑bacteriën mengen, worden blootgesteld aan achtergebleven antibiotica en mobiel DNA uitwisselen dat hen zowel medicijnresistenter als beter ziekteverwekkend kan maken. Hoewel zuiveringsinstallaties veel verontreinigingen verwijderen, elimineren ze niet volledig resistente of pathogene E. coli, en sommige van deze stammen en hun plasmiden worden geloosd in rivieren en kustwateren die door het publiek worden gebruikt. Voor het brede publiek is de kernboodschap dat antibioticaresistentie zich niet beperkt tot ziekenhuizen: ze wordt mede bepaald door hoe we met afvalwater omgaan en natuurlijke wateren beschermen. Het monitoren van rioolwater en nabijgelegen recreatiewateren, het verminderen van antibioticagebruik en het verbeteren van zuiveringstechnologieën kan helpen de milieu‑"recycling" van gevaarlijke microben terug naar mensen te vertragen.
Bronvermelding: Justh de Neczpal, A., Thorell, K., Tuts, L. et al. Antimicrobial resistance, conjugative plasmids and pathogenicity in wastewater and freshwater Escherichia spp. in Stockholm, Sweden. npj Antimicrob Resist 4, 32 (2026). https://doi.org/10.1038/s44259-026-00208-5
Trefwoorden: antibioticaresistentie, rioolwaterzuivering, E. coli, milieumicrobiologie, plasmidoverdracht