Clear Sky Science · de
Antimikrobielle Resistenz, konjugative Plasmide und Pathogenität von Escherichia spp. in Abwasser und Süßwasser in Stockholm, Schweden
Warum Wasser und Keime den Alltag betreffen
Die meisten Menschen verbinden Antibiotikaresistenz mit Krankenhäusern, doch diese Studie zeigt, dass sie auch durch das Wasser unter unseren Städten und an unseren Stränden geprägt werden kann. Forscher in Stockholm, Schweden, verfolgten Bakterien aus Kläranlagen sowie aus nahegelegenen Seen und Küstengewässern, um eine einfache, aber drängende Frage zu beantworten: Helfen unsere Abwasserleitungen dabei, schwer behandelbare Keime wieder in die Umwelt zu schleusen, in der Menschen baden, sich erholen und Trinkwasser entnehmen?
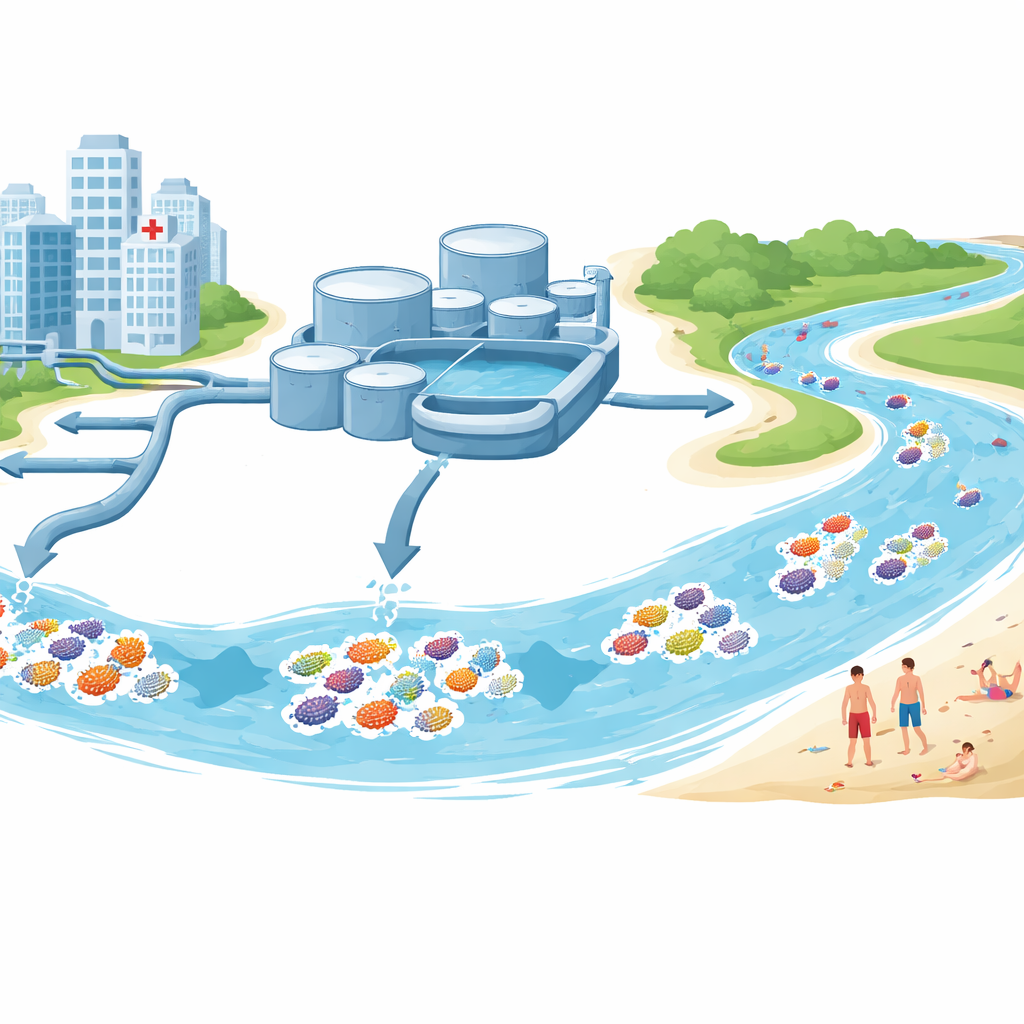
Woher die Proben stammten
Das Team sammelte im Sommer 2022 Wasser und Sediment in und um Stockholm. Einige Proben stammten aus Zuläufen und Abläufen großer Kläranlagen, die Abwässer aus Haushalten und Krankenhäusern aufnehmen. Andere wurden aus Süßwasserseen und brackigen Stränden der Ostsee entnommen, die zur Erholung genutzt werden. Von diesen Stellen isolierten sie 68 Stämme von Escherichia‑Arten, überwiegend E. coli, ein häufiges Darmbakterium und ein Standardindikator für fäkale Verunreinigung. Jeder Stamm wurde im Labor auf seine Antibiotikaresistenzen getestet und anschließend auf DNA‑Ebene entschlüsselt, um Resistenzgene, krankheitsrelevante Gene und die kleinen DNA‑Kreise namens Plasmide zu identifizieren, die zwischen Bakterien springen können.
Stärkere Resistenz im Abwasser als in natürlichen Gewässern
Der Unterschied zwischen Abwasser und natürlichen Gewässern war deutlich. Mehr als die Hälfte der E. coli‑Stämme aus dem Abwasser war gegen mindestens drei Antibiotikaklassen resistent, und viele trugen Cluster von Resistenzgenen, einschließlich solcher, die weit verbreitete Cephalosporine der dritten Generation unwirksam machen. Insbesondere Gene der CTX‑M‑Familie, vor allem die Variante CTX‑M‑15, waren in Abwasserstämmen häufig, in Stämmen aus Seen und Stränden jedoch vollständig abwesend. Mehrere Abwasserbakterien gehörten zu bekannten Linien, die Harnwegs‑ und Blutstrominfektionen beim Menschen verursachen, darunter die global problematische Gruppe ST131, und diese trugen einige der schwersten Lasten an Resistenzgenen.
Antibiotikarückstände und mobile DNA
Chemische Analysen des Wassers zeigten, dass Antibiotikarückstände in Zuläufen und Abläufen der Kläranlagen durchgängig höher waren als an natürlichen Stellen. Die Ciprofloxacin‑Konzentrationen an einem Zulauf und einem Ablauf lagen über veröffentlichten Schwellenwerten, ab denen eine Förderung von Resistenzen erwartet wird. Dieser chemische Hintergrund ist wichtig, weil viele Resistenzgene auf konjugativen Plasmiden lagen—mobilen DNA‑Kreisen, die von einem Bakterium zum anderen wandern können. In Labor‑Konjugationsexperimenten übertrugen sich Plasmide aus 16 Stämmen erfolgreich auf einen Standardempfänger, häufig begleitet von Resistenzen gegen mehrere Wirkstoffe gleichzeitig. Plasmide bestimmter Familien, insbesondere IncN und IncI, bewegten sich besonders effizient, was darauf hindeutet, dass sie leistungsfähige Vehikel für die Verbreitung von Resistenzen in der dicht besiedelten, nährstoffreichen Umgebung von Abwassersystemen sind.
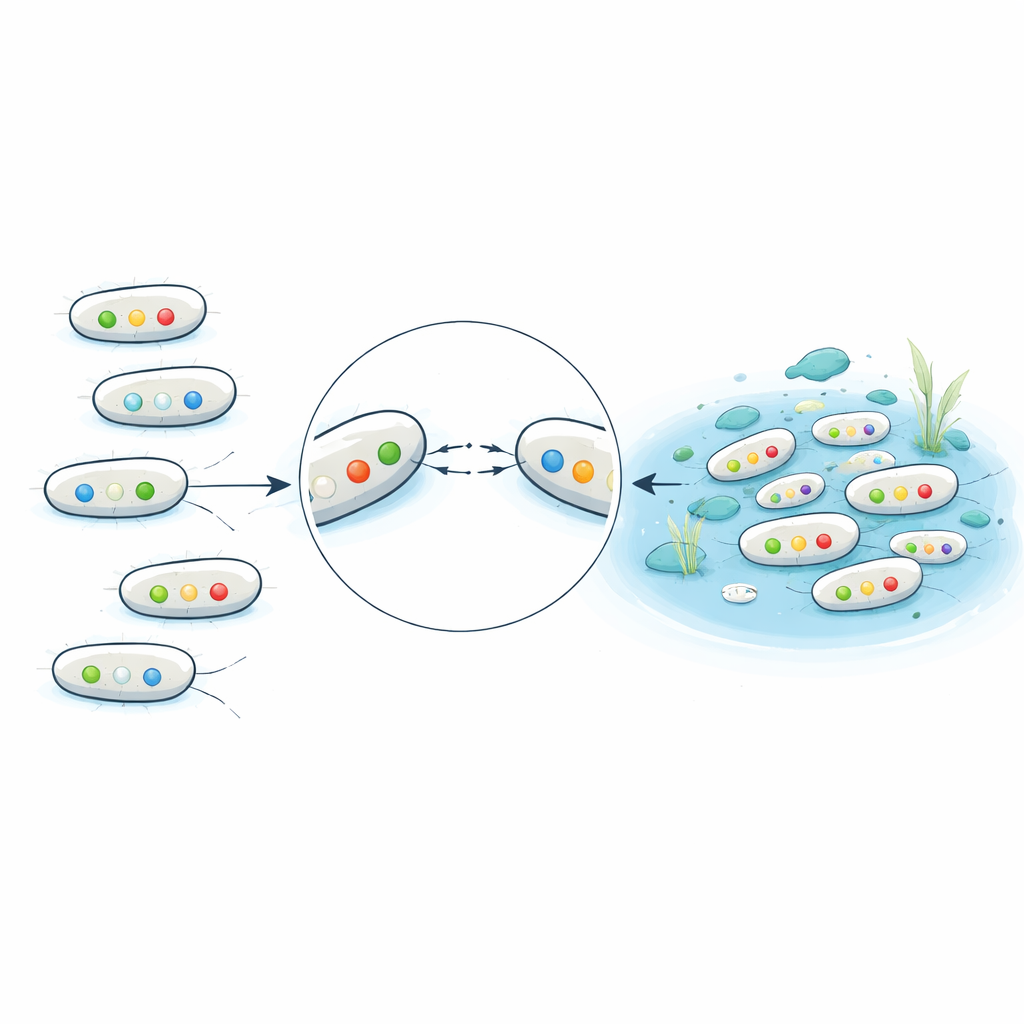
Pathogenitätsbezogene Merkmale in Alltagsgewässern
Über die Arzneimittelresistenz hinaus suchten die Wissenschaftler in den Genomen nach Genen, die E. coli bei der Krankheitsentstehung helfen, etwa für Toxine, Adhäsine, die Bakterien an Darm oder Harntrakt haften lassen, und Faktoren, die sie im Blutkreislauf schützen. Viele Abwasserisolate trugen Kombinationen von Genen, die typisch für extraintestinale und Harnwegs‑Pathogene sind und Muster widerspiegeln, die auch in klinischen Infektionen beobachtet werden. Überraschenderweise trug ein großer Anteil der E. coli aus scheinbar sauberen Seen und Stränden ebenfalls einige dieser Virulenzgene, obwohl sie allgemein weniger Resistenzgene und keine Extended‑Spectrum‑Beta‑Laktamasen aufwiesen. Die Studie fand zudem Umweltverwandte wie Escherichia marmotae, die krankheitsassoziierte Gene trugen, was darauf hindeutet, dass Wildtiere und natürliche Gewässer potenzielle Reservoirs für bereitstehende Krankheitserreger darstellen können.
Was das für Menschen und Politik bedeutet
In der Summe zeichnen die Ergebnisse Kläranlagen als wichtige Kreuzungspunkte, an denen menschliche, tierische und umweltbezogene Bakterien aufeinandertreffen, Rückständen von Antibiotika ausgesetzt sind und mobile DNA austauschen, die sie sowohl resistenter gegen Medikamente als auch fähiger macht, Krankheiten zu verursachen. Obwohl Kläranlagen viele Schadstoffe entfernen, eliminieren sie resistente oder pathogene E. coli nicht vollständig, und einige dieser Stämme und ihre Plasmide werden in Flüsse und Küstengewässer eingeleitet, die von der Öffentlichkeit genutzt werden. Für Laien lautet die Kernbotschaft: Antibiotikaresistenz ist nicht auf Krankenhäuser beschränkt; sie wird davon geprägt, wie wir Abwasser behandeln und natürliche Gewässer schützen. Die Überwachung von Abwässern und angrenzenden Freizeitgewässern, die Reduktion des Antibiotikagebrauchs und die Verbesserung der Behandlungstechnologien können alle dazu beitragen, das umweltbedingte „Recycling“ gefährlicher Keime zurück zum Menschen zu verlangsamen.
Zitation: Justh de Neczpal, A., Thorell, K., Tuts, L. et al. Antimicrobial resistance, conjugative plasmids and pathogenicity in wastewater and freshwater Escherichia spp. in Stockholm, Sweden. npj Antimicrob Resist 4, 32 (2026). https://doi.org/10.1038/s44259-026-00208-5
Schlüsselwörter: antibiotikaresistenz, abwasserbehandlung, E. coli, Umweltmikrobiologie, Plasmidtransfer