Clear Sky Science · nl
Milieudistributie van multiresistente Escherichia coli over One Health-grenzen in Mymensingh, Bangladesh
Waarom ziekteverwekkers in water iedereen aangaan
Antibioticaresistente “superbacteriën” worden vaak besproken in ziekenhuizen, maar blijven daar niet. Deze studie toont aan hoe gevaarlijke stammen van Escherichia coli, een veelvoorkomende darmbacterie, zich verspreiden via water dat door mensen, dieren en landbouw in één district van Bangladesh wordt gebruikt. Door deze microben te volgen bij ziekenhuizen, veehouderijen, vispoelen en een rivier, laten de onderzoekers zien hoe dagelijkse activiteiten geruisloos kunnen helpen resistente bacteriën het milieu in en weer terug naar mensen te brengen.
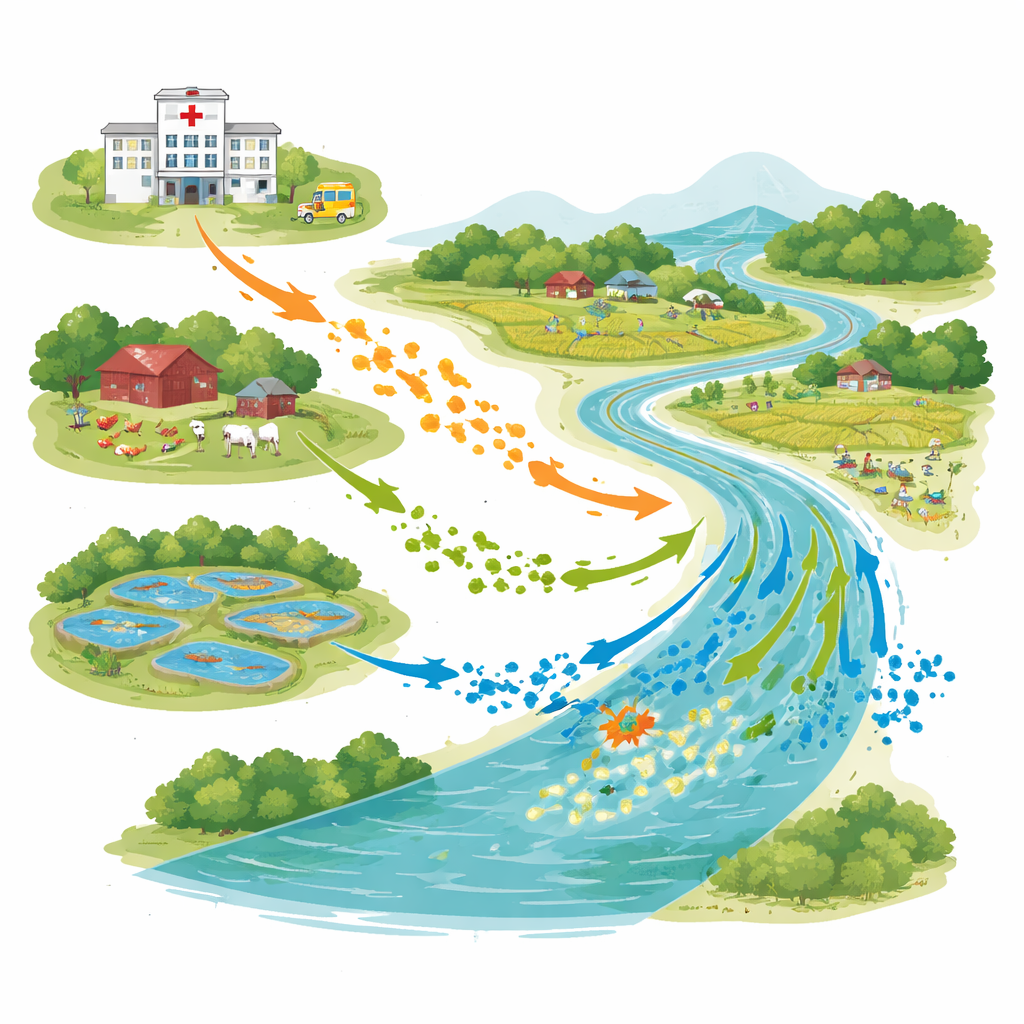
Een verbonden landschap van mensen, dieren en water
Het onderzoek vond plaats in Bhaluka Upazila, een semi-stedelijk gebied waar ziekenhuizen, pluimvee- en rundveebedrijven, aquacultuurvijvers en de Khiro-rivier in hetzelfde landschap liggen. In mei 2022 verzamelden wetenschappers 28 watermonsters van ziekenhuisafvoeren, bedrijfslozingen, visvijvers en twee punten langs de rivier, stroomopwaarts en stroomafwaarts van ziekenhuislozingen. Met een standaardprotocol van de Wereldgezondheidsorganisatie telden ze E. coli in elk monster en richtten ze zich op stammen die bestand zijn tegen krachtige antibiotica die voor ernstige infecties worden gebruikt.
Hoge niveaus van resistente bacteriën in afval en rivierwater
Het team vond E. coli in elk monster en ontdekte dat 86% stammen bevatte die resistent zijn tegen veelgebruikte ‘derde-generatie’-antibiotica. De niveaus waren het hoogst in ziekenhuisafvalwater en in lozingen van pluimvee- en rundveebedrijven, waar zowel totaal E. coli als resistente typen zeer overvloedig waren. Carbapenem-resistente stammen—bestand tegen geneesmiddelen als laatste redmiddel—waren minder vaak aanwezig maar alarmerender. Zij verschenen alleen in ziekenhuisafvoeren en in het rivierwater stroomafwaarts van ziekenhuislozingen, en ontbraken volledig in veehouderij- en aquacultuurvijvers. Visvijvers vertoonden over het algemeen veel minder verontreiniging, wat wijst op minder antibiotica-inbreng daar.
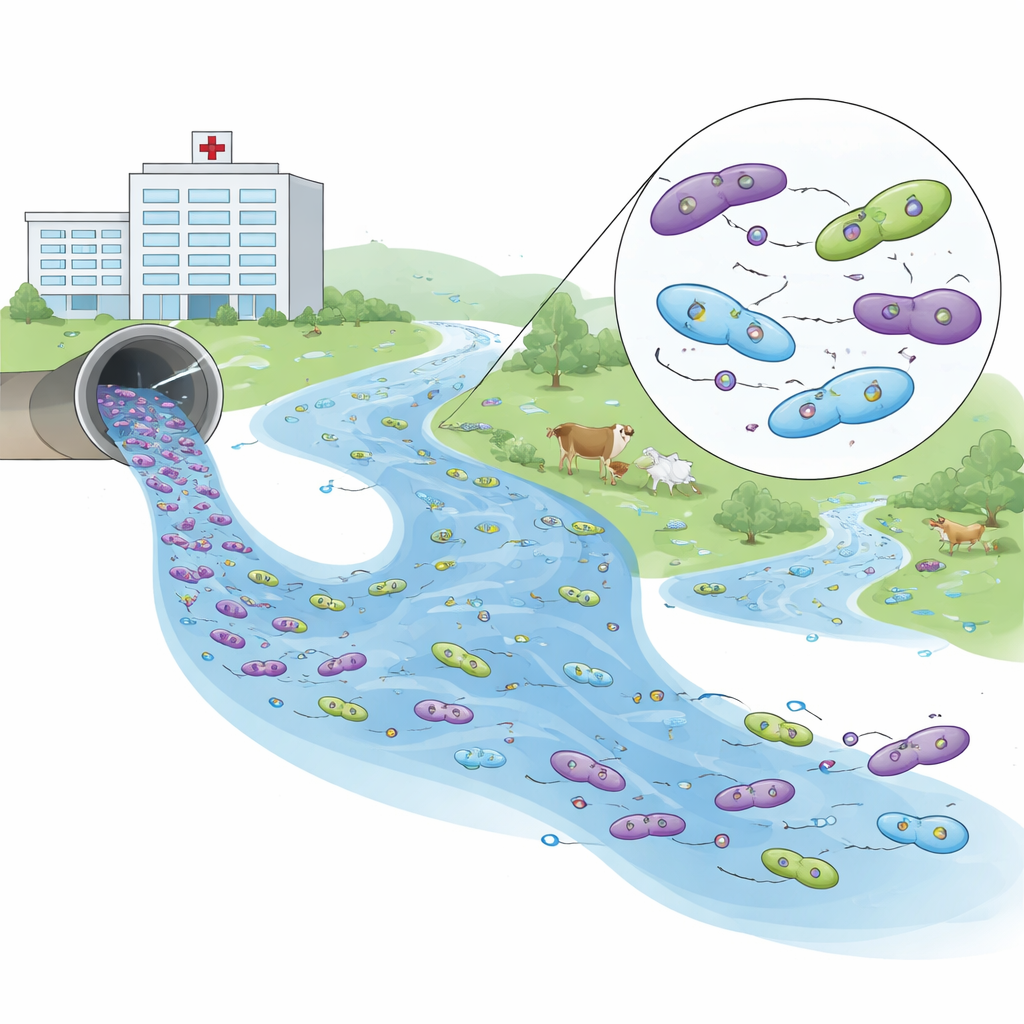
De DNA-vingerafdrukken van resistentie lezen
Om te begrijpen hoe deze bacteriën verwant zijn, sequentieerden de onderzoekers de genomen van 26 representatieve isolaten. Ze ontdekten 93 verschillende resistentiegenen, waarvan een paar herhaaldelijk optraden op meerdere locaties. Één genfamilie, bekend als blaCTX-M-15, die veel belangrijke bèta-lactamantibiotica onwerkzaam maakt, domineerde in alle omgevingen. Een ander gen, blaNDM-5, verleent resistentie tegen carbapenems, enkele van de krachtigste geneesmiddelen in de moderne geneeskunde. Dit gen kwam voor in ziekenhuismonsters en in een isolaat uit de rivier stroomafwaarts, gekoppeld aan kleine, mobiele DNA-lusjes die plasmiden worden genoemd en zich tussen bacteriën kunnen verplaatsen.
Genetische verbanden tussen ziekenhuisafvoeren en de rivier
Door kleine DNA-verschillen te vergelijken—éénletterwijzigingen in het genoom—bouwden de wetenschappers een stamboom van de verzamelde E. coli. De meeste bacteriën clusterden naar herkomst: pluimvee-isolaten groepeerden samen, rundveerisolaten vormden een eigen tak, en aquacultuurstammen stonden apart met minder resistentie-eigenschappen. Ziekenhuisisolaten waren diverser maar, cruciaal, deelden één ziekenhuisstam en een stroomafwaarts rivierisolaat een vrijwel identieke genetische kern, zonder verschillen in het core-genoom. Hoewel ze als licht verschillende sequentietypes werden geclassificeerd, wijst deze bijna perfecte overeenkomst, gecombineerd met de aanwezigheid van hetzelfde carbapenem-resistentiegen op plasmiden, sterk op recente verspreiding van ziekenhuislozingen naar de rivier.
Wat dit betekent voor gezondheid en beleid
Dit werk biedt een close-up van hoe resistente bacteriën bewegen over de ‘One Health’-interface die mensen, dieren en het milieu verbindt. Het toont aan dat ziekenhuisafvalwater een belangrijk knooppunt is dat sterk resistente E. coli in een rivier loost waarop lokale gemeenschappen vertrouwen. Veehouderijsystemen leveren ook grote aantallen resistente stammen, al nog niet van die tegen middelen als laatste redmiddel. Zelfs met een beperkt aantal monsters dat in één maand is genomen, ondersteunen de bevindingen dringende actie: betere behandeling van ziekenhuisafvalwater, voorzichtiger gebruik van antibiotica op boerderijen en in klinieken, en routinematige bewaking van rivieren en andere gedeelde waterbronnen. Voor niet-specialisten is de kernboodschap dat keuzes over antibioticagebruik en afvalbeheer niet alleen ziekenhuispatiënten raken—ze bepalen de onzichtbare stroom van superbacteriën door het milieu dat we allemaal delen.
Bronvermelding: Rahman, A., Roy, S., Afreen, N. et al. Environmental dissemination of multidrug-resistant Escherichia coli across one health interfaces in Mymensingh, Bangladesh. npj Antimicrob Resist 4, 27 (2026). https://doi.org/10.1038/s44259-026-00202-x
Trefwoorden: antimicrobiële resistentie, milieuverontreiniging, afvalwater, Escherichia coli, One Health