Clear Sky Science · de
Umweltverbreitung multiresistenter Escherichia coli an One‑Health‑Schnittstellen in Mymensingh, Bangladesch
Warum Keime im Wasser uns alle betreffen
Antibiotikaresistente „Superkeime“ werden häufig im Zusammenhang mit Krankenhäusern diskutiert, bleiben dort aber nicht. Diese Studie zeigt, wie gefährliche Stämme von Escherichia coli, einem häufigen Darmbakterium, sich über Wasser verbreiten, das von Menschen, Tieren und landwirtschaftlichen Betrieben in einem Distrikt Bangladeschs genutzt wird. Indem die Forschenden diese Mikroben in Krankenhäusern, Tierhaltungen, Fischteichen und einem Fluss nachverfolgen, machen sie deutlich, wie alltägliche Aktivitäten widerstandsfähige Keime unbemerkt in die Umwelt und zurück zum Menschen bringen können.
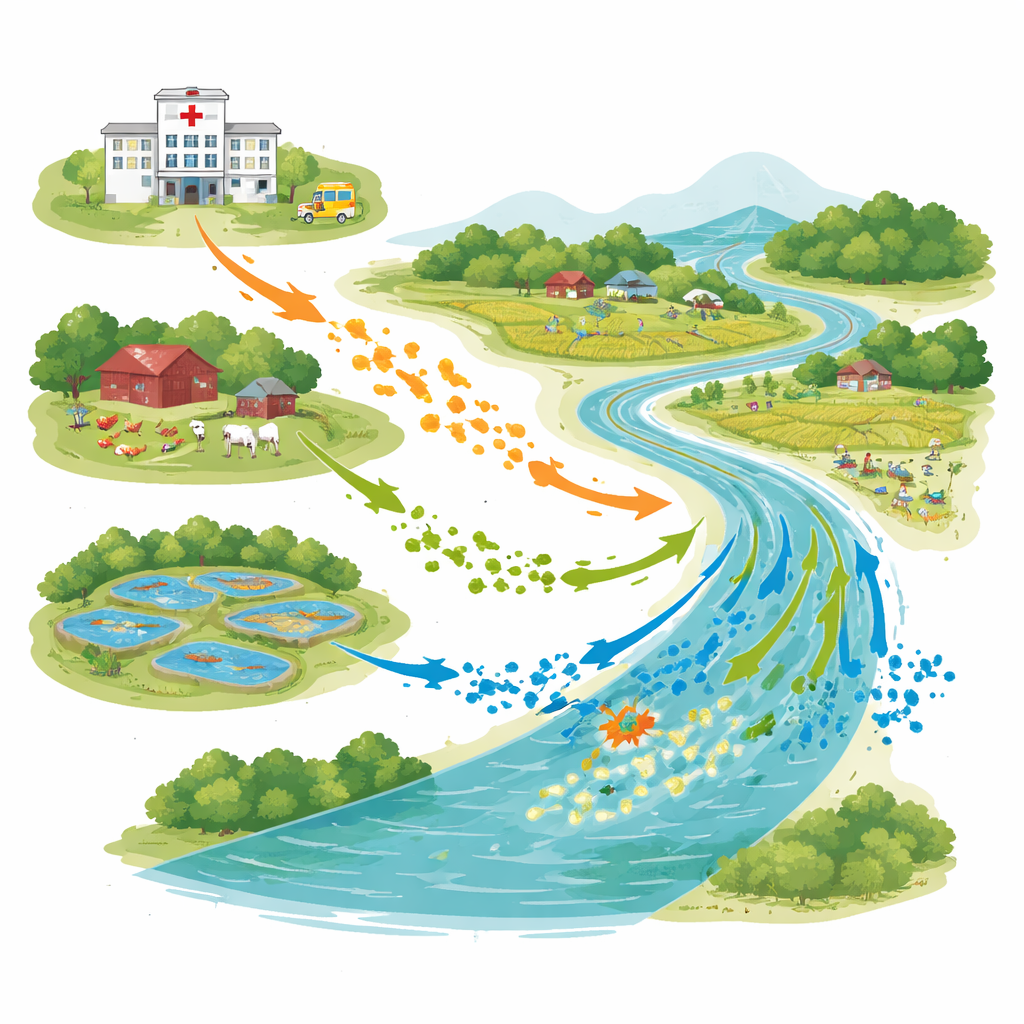
Eine vernetzte Landschaft aus Menschen, Tieren und Wasser
Die Untersuchung fand in Bhaluka Upazila statt, einem halb‑urbanen Gebiet, in dem Krankenhäuser, Geflügel‑ und Rinderbetriebe, Aquakulturteiche und der Khiro‑Fluss räumlich nahe beieinander liegen. Im Mai 2022 sammelten die Wissenschaftler 28 Wasserproben aus Krankenhausabflüssen, Betriebsabwässern, Fischteichen sowie an zwei Stellen des Flusses – oberhalb und unterhalb der Krankenhausablässe. Nach einem Standard‑Protokoll der Weltgesundheitsorganisation zählten sie die E. coli in jeder Probe und konzentrierten sich auf Stämme, die mächtige Antibiotika für schwere Infektionen umgehen können.
Hohe Anteile resistenter Bakterien in Abwässern und Flusswasser
Das Team fand E. coli in jeder Probe und stellte fest, dass 86 % Stämme enthielten, die gegen weit verbreitete „Dritt‑Generations“‑Antibiotika resistent sind. Die höchsten Konzentrationen fanden sich in Krankenhausabwässern sowie in Abwässern aus Geflügel‑ und Rinderbetrieben, wo sowohl die Gesamtzahl an E. coli als auch die resistenten Typen sehr hoch waren. Carbapenemresistente Stämme – die gegen Reservemedikamente resistent sind – waren seltener, aber besorgniserregender. Sie traten nur in Krankenhauskanälen und im Flusswasser unterhalb der Krankenhausablässe auf und fehlten vollständig in den Tierhaltungs‑ und Aquakulturteichen. Fischteiche zeigten insgesamt deutlich geringere Kontamination, was auf weniger Antibiotikaeinträge dort hindeutet.
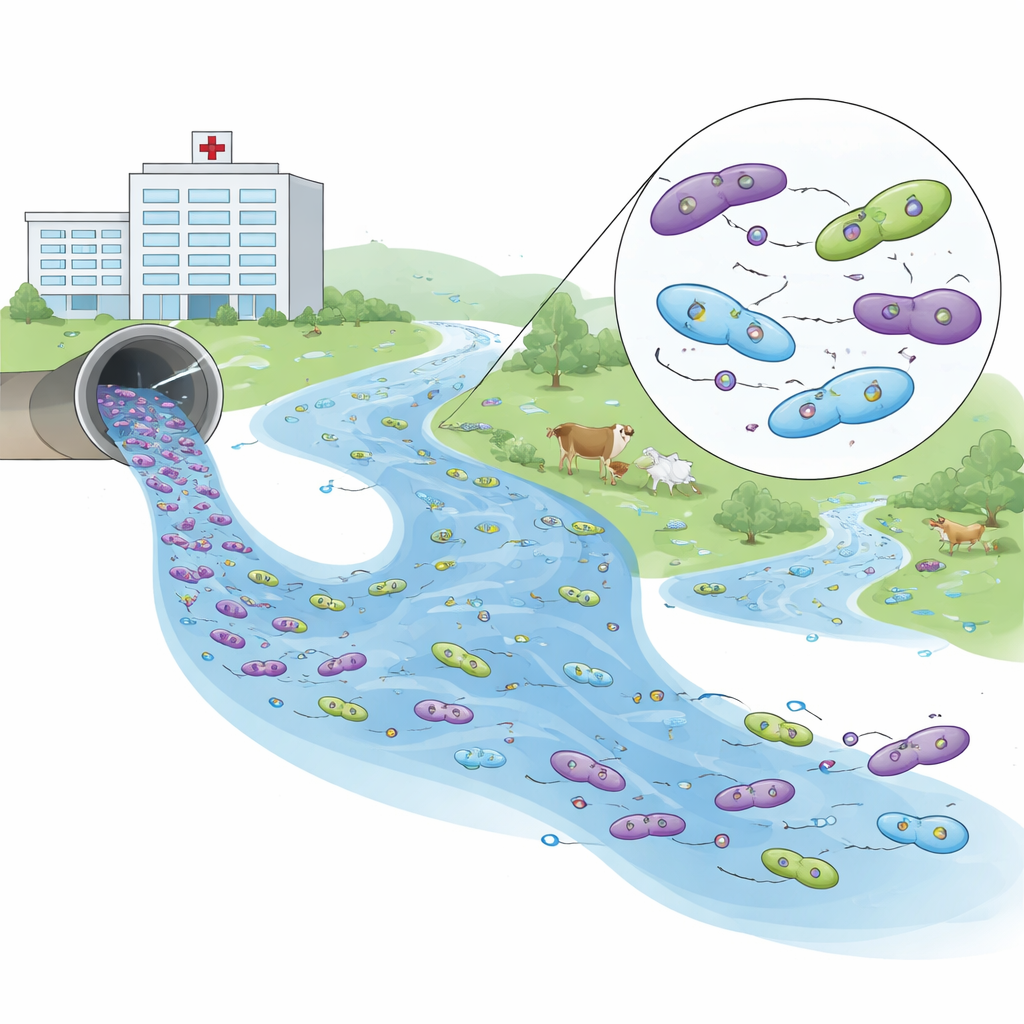
Die DNA‑Fingerabdrücke der Resistenz lesen
Um zu verstehen, wie diese Bakterien miteinander verwandt sind, sequenzierten die Forschenden die Genome von 26 repräsentativen Isolaten. Sie entdeckten 93 verschiedene Resistenzgene, wobei einige wenige immer wieder an verschiedenen Probenorten auftauchten. Eine Genfamilie, bekannt als blaCTX‑M‑15, die viele wichtige Beta‑Laktam‑Antibiotika außer Kraft setzt, dominierte in allen Umgebungen. Ein anderes Gen, blaNDM‑5, vermittelt Carbapenemresistenz, also Resistenz gegen einige der stärksten Medikamente der modernen Medizin. Dieses Gen fand sich in Krankenhausproben und in einem Flussisolat stromabwärts, gekoppelt an kleine, bewegliche DNA‑Ringe (Plasmide), die zwischen Bakterien übertragen werden können.
Genetische Verbindungen zwischen Krankenhausabläufen und dem Fluss
Durch den Vergleich winziger DNA‑Unterschiede – einzelner Buchstabenänderungen im Genom – bauten die Wissenschaftler einen Stammbaum der gesammelten E. coli. Die meisten Bakterien gruppierten sich nach Quelle: Geflügelisolaten bildeten eine Gruppe, Rinderisolaten bildeten einen eigenen Ast, und Aquakulturstämme lagen getrennt und wiesen weniger Resistenzmerkmale auf. Krankenhausisolate waren vielfältiger, doch entscheidend ist: Ein Krankenhausstamm und ein stromabwärts entnommenes Flussisolat teilten nahezu identische genetische Grundstrukturen, ohne Unterschiede im Kern ihres Genoms. Obwohl sie formal leicht unterschiedliche Sequenztypen hatten, deutet diese fast perfekte Übereinstimmung, kombiniert mit dem Vorhandensein desselben Carbapenemresistenzgens auf Plasmiden, stark auf eine aktuelle Ausbreitung von Krankenhausabwässern in den Fluss hin.
Was das für Gesundheit und Politik bedeutet
Diese Arbeit liefert eine anschauliche Momentaufnahme, wie resistente Bakterien über die One‑Health‑Schnittstelle zwischen Menschen, Tieren und Umwelt wandern. Sie zeigt, dass Krankenhausabwasser ein wichtiger Hotspot ist, der hochresistente E. coli in einen Fluss freisetzt, von dem lokale Gemeinschaften abhängig sind. Tierhaltungssysteme tragen ebenfalls große Mengen resistenter Stämme bei, wenn auch bislang nicht solche gegen Reservemedikamente. Trotz einer nur moderaten Stichprobenzahl in einem Monat unterstützen die Ergebnisse dringendes Handeln: bessere Behandlung von Krankenhausabwässern, vorsichtigere Antibiotikaanwendung in Betrieben und Kliniken sowie routinemäßige Überwachung von Flüssen und anderen gemeinsam genutzten Wasserquellen. Für Laien lautet die Kernbotschaft: Entscheidungen zu Antibiotikagebrauch und Abfallmanagement betreffen nicht nur Patientinnen und Patienten im Krankenhaus – sie bestimmen den unsichtbaren Fluss von Superkeimen durch die Umwelt, die wir alle teilen.
Zitation: Rahman, A., Roy, S., Afreen, N. et al. Environmental dissemination of multidrug-resistant Escherichia coli across one health interfaces in Mymensingh, Bangladesh. npj Antimicrob Resist 4, 27 (2026). https://doi.org/10.1038/s44259-026-00202-x
Schlüsselwörter: antimikrobielle Resistenz, Umweltkontamination, Abwasser, Escherichia coli, One Health