Clear Sky Science · he
SIRT1 מעורר פיתוח של FOXO1/אוטופאגיה/NCOA4-תלוית פרופתוזיס ומאיץ את התקדמות האוטם המוחי על ידי עיכוב מסלול האיתות E2F1/NOTCH-1/YAP
מדוע המחקר הזה על שבץ חשוב
אוטם מוחי, צורה שכיחה של שבץ, נשאר סיבה מובילה לתמותה ולנכות ברחבי העולם. לעתים רופאים מצליחים לפתוח כלי דם חסומים, אך רבים מהמטופלים נותרים עם נזק מוחי מתמשך. מחקר זה בוחן מה קורה בתוך תאי המוח כדי לגלות כיצד חלבון בקרה מרכזי, SIRT1, עלול למעשה להחמיר את הפגיעה לאחר שבץ על ידי דחיפת תאים לצורת מוות הרסנית התלויה בברזל. הבנת המסלול החבוי הזה עשויה לפתוח פתח לטיפולים חדשים שישמרו על המוח כשכל דקה חשובה.
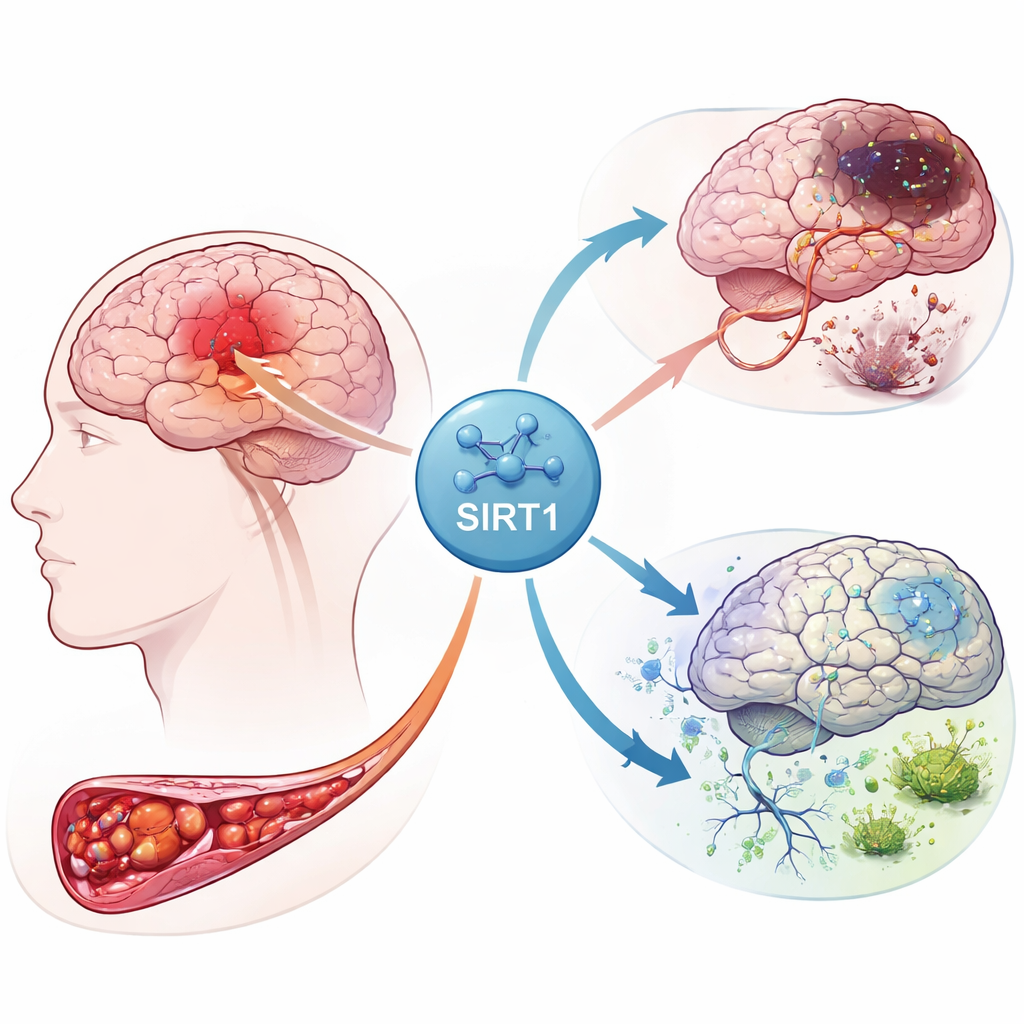
תגובות שרשרת בתוך מוח שנפגע
כשזרימת הדם לחלק מהמוח נמנעת, תאי העצב נאלצים להתמודד עם חוסר חמצן ואנרגיה. המשבר הזה מצית סערת אותות בתוך סוגי תאים רבים, כולל תאים תומכים הנקראים אסטרוציטים. החוקרים התרכזו בחלבון בשם SIRT1, רגולטור ראשי המגיב למתח אנרגטי. באמצעות נתוני ביטוי גנים ממטופלי שבץ הם מצאו כי SIRT1 קשור קשר חזק לגנים המעורבים בטיפול בברזל, בהישרדות התאים ובצורת מוות חדשה שהתגלתה בשם פרופתוזיס. הניתוח שלהם גם הדגיש קשרים בין SIRT1 לבין כמה מסלולי איתות המוכרים כבעלי תפקיד בשליטה על גדילה תאית ותהליכי ניקוי עצמי.
מנתונים גדולים למוחות של בעלי חיים ולצלחות תרבית
כדי לבדוק כיצד הרמזים האלה מתנהגים ברקמה חיה, הצוות יצר מודל חולדה לאוטם מוחי על ידי חסימת עורק מוחי מרכזי לזמן קצר ואז החזרת זרימת הדם. חלק מהחולדות קיבלו תרופה המפעילה את SIRT1, בעוד שאחרות קיבלו וירוס שהגביר רכיב אחר של המסלול, Notch-1. חתכי מוח הראו כי פעילות SIRT1 עלתה באופן חזק לאחר השבץ וכי הגברת SIRT1 הגדילה את אזור הרקמה המת ואת חומרת הפגיעה בעצבים. לעומת זאת, הגברת רמות Notch-1 צמצמה את הנזק. בדיקות חלבון אישרו את הדפוס הזה: כאשר SIRT1 היה גבוה, גורמי הגנה הקשורים ל-Notch-1 ולחלבון שותף, YAP, ירדו, בעוד פגיעת השבץ התרחבה.
כיצד ברזל ואכילה עצמית דוחפים מוות תאי
החוקרים המשיכו לתרביות אסטרוציטים שנחשפו לחמצן נמוך, תזונה דלה ותוספת ברזל כדי לדמות תנאי שבץ. על ידי הוספה מדודה של מעכבים או מגברים של SIRT1, E2F1, Notch-1, YAP ופרופתוזיס, הם מיפו שרשרת אירועים מפורטת. SIRT1 גבוה כיבה את E2F1 הגרעיני, Notch-1 ו-YAP, אך הגדיל רגולטור אחר בשם FOXO1, יחד עם חלבונים המסמנים עלייה באוטופאגיה ומתווך מטען הנקרא NCOA4. שילוב זה הטה לטובת סוג מיוחד של אוטופאגיה המפרקת קומפלקסים האחסון של הברזל, ושיחרר ברזל חופשי לתוך התאים. בזמן זה, סמני מערכות ההגנה נגד חמצון השתנו ומספר המוות התאי עלה משמעותית, בהתאמה לחתימת הביוכימית של פרופתוזיס. חסימת הפרופתוזיס או שיקום חלקי של ציר Notch-1/YAP הפחיתו את השינויים הפוגעים הללו.
מפסק מאסטר חדש למסלולי הפגיעה
בהרכבת הממצאים מציע המחקר כי SIRT1 פועל כמפסק מאסטר לאחר שבץ, יושב בצומת של חישת אנרגיה, ויסות גנטי וחילוף חומרים של ברזל. כאשר SIRT1 מופעל בעוצמה, הוא מדכא את ציר E2F1/Notch-1/YAP, שבמצבו התקין מסייע לשמור על פעולת גנים שורדים ומערכות אנטי-חמצון. במקביל, SIRT1 מגביר את FOXO1 ותוכנית אוטופאגיה שמגייסת את NCOA4 כדי לפרק חלבוני אחסון ברזל. עודף הברזל שנוצר, בשילוב עם הגנה כימית מוחלשת, גורם לנזק לשומנים בממברנות התאים ודוחף את התאים לפרופתוזיס.
מסקנות לגבי טיפול עתידי בשבץ
ללא רקע מקצועי, המסר המרכזי הוא שלא כל המוות התאי לאחר שבץ זהה, וחלקו עשוי להיות ניתן למניעה. העבודה הזו מציעה כי במוח תחת מתח SIRT1 יכול להזיז את המאזן לעבר מסלול מוות תלוי-ברזל הרסני במקום הגנה. מטרה של SIRT1 עצמו, או של שלבי המורד המעורבים ב-Notch-1, YAP, FOXO1, אוטופאגיה ו-NCOA4, יכולה להציע דרכים חדשות לצמצום נזק מוחי מעבר לפשוט פתיחת כלי דם חסומים. אם כי נדרשים עוד מחקרים ברקמות אנושיות, המסלול המתואר כאן מספק מפת דרכים לעיצוב תרופות שיכבו את האש התלויה בברזל בתוך תאי המוח ועשויות לשפר את ההחלמה לאחר אוטם מוחי.
ציטוט: Wang, G., Ma, S., Qi, L. et al. SIRT1 induces FOXO1/autophagy/NCOA4-induced ferroptosis and accelerates the progression of cerebral infarction by inhibiting the E2F1/NOTCH-1/YAP signaling pathway. Sci Rep 16, 13946 (2026). https://doi.org/10.1038/s41598-026-44355-1
מילות מפתח: אוטם מוחי, פרופתוזיס, SIRT1, אוטופאגיה, מנגנוני שבץ