Clear Sky Science · he
פולימורפיזם ב‑MTHFR קשור לעלייה בתופעות לוואי ותוצאות קליניות גרועות בחולי סרטן קיבה המטופלים בכימותרפיית S-1 משלימה
מדוע חלק מהאנשים מתקשים יותר עם אותו גלולה נגד סרטן
שני מטופלים יכולים ליטול את אותה גלולה כימותרפית ולחוות חוויות שונות לחלוטין: אחד יסיים את הטיפול עם אי נוחות קלה בלבד, בעוד שאחר יתמודד עם תופעות לוואי קשות וסיכון גבוה יותר לשארת המחלה. המחקר הזה שואל שאלה פשוטה אך קריטית לחולי סרטן קיבה: האם הבדלים תורשתיים שכיחים ב‑DNA שלנו יכולים להסביר מי מסתדר טוב ומי מסתדר פחות עם תרופה אורלית נפוצה בשם S-1?
גלולה שעוצבה כדי להקל על טיפול קשה
S-1 היא צורה אורלית של כימותרפיה הניתנת לאחר ניתוח לסרטן הקיבה, במיוחד במזרח אסיה. במקום להזדקק למתן בזרם רצוף בבית החולים, S-1 נלקחת כגלולות למשך שנה, מה שמקל על חיי המטופלים. התרופה מבוססת על סוכן אנטי‑סרטן ישן יותר, 5‑פלואורואורציל, אך מוסיפה שני מרכיבים מסייעים שמשנים את האופן שבו הטיפול מעובד בגוף. ניסויים קליניים גדולים כבר הראו ששנה של S-1 לאחר ניתוח מפחיתה את הסיכון לחזרת המחלה ועשויה להאריך את תוחלת החיים. אך לא כולם יכולים לסבול טיפול בן שנה במלואו, ורופאים שמו לב שתופעות הלוואי והתועלות משתנות במידה ניכרת מאדם לאדם.
בחינת רמזי DNA במטופלים שטופלו
החוקרים בדקו 334 אנשים עם סרטן קיבה בשלב II או III שעברו כריתה של הגידול ולאחר מכן קיבלו טיפול משלימתי (אחרי־ניתוח) ב‑S-1. לכל המשתתפים הייתה תפקודיות איברים טובה בתחילת הטיפול, ונלקחה דגימת דם לפני הכימותרפיה כדי לבדוק הבדלים זעירים ושכיחים ב‑DNA המכונים פולימורפיזמים של נוקלאוטיד יחיד (SNPs). הצוות התמקד ב‑46 SNPs בשישה גנים שמעורבים בעיבוד 5‑פלואורואורציל ותרופות קרובות לו. אחר כך עקבו אחר המטופלים במשך חציון של יותר משבע שנים, ורשמו בקפידה את תופעות הלוואי הטיפוליות, כמה תרופה קיבל כל מטופל בפועל לאורך זמן, כמה זמן נשארו חופשיים ממחלה וכמה זמן שרדו באופן כללי.
משתנה DNA שכיח בולט
מבין כל הסמנים הגנטיים, שינוי ספציפי אחד בגן הקרוי MTHFR בלט כחשוב במיוחד. וריאנט זה, המכונה rs1801133, משפיע על אנזים שמנהל את מטבוליזם החומצה הפולית, ויטמין הקשור קרוב לבניין ותיקון DNA. אנשים שירשו שתי עותקים של הגרסה המסכנת היו בסבירות גבוהה בערך פי שלוש לפתח תופעות לוואי הקשורות לדם כגון אנמיה או ספירה נמוכה של תאי דם לבנים. כאשר החוקרים הסתכלו על התוצאות לטווח הארוך, מטופלים שהחזיקו לפחות עותק אחד של הגרסה המסכנת חוו פרקי זמן קצרים יותר ללא חזרת המחלה ותוחלת הישרדות כוללת קצרה יותר בהשוואה לאלה עם הגרסה הטיפוסית. גן נוסף המעורב בפירוק התרופה, CYP2A6, הראה גם הוא קשר להישרדות חופשית ממחלה גרועה יותר, אך השפעתו הייתה חלשה ופחות עקבית.
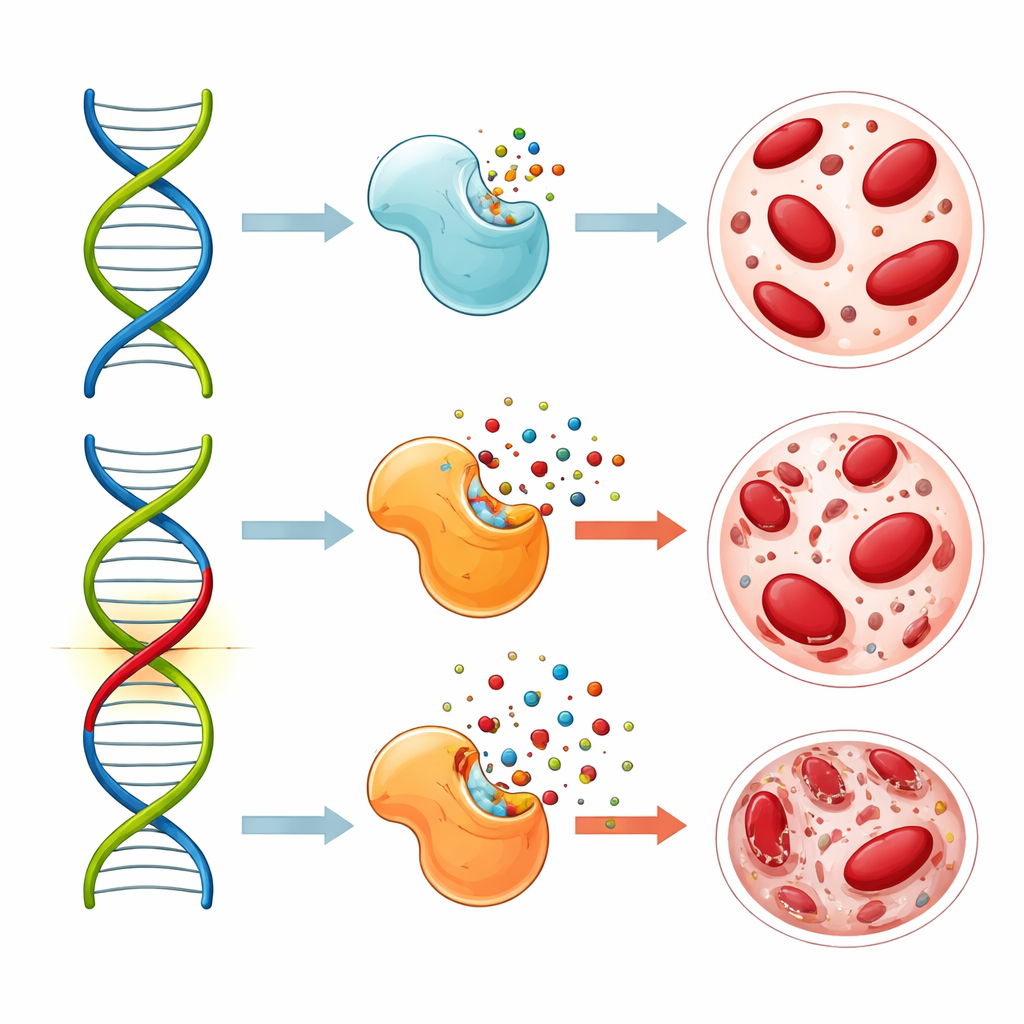
מדוע שינוי זה ב‑DNA עלול להחמיר תופעות לוואי ותוצאות
עבודות מעבדה ממחקרים אחרים הראו שהוריאנט ב‑MTHFR מפחית את פעילות האנזים, ומעביר את מאזן החומצה הפולית בתוך התאים. שינוי זה יכול להפוך את 5‑פלואורואורציל ליעיל יותר בחסימת האנזימים שהתאים הסרטניים משתמשים בהם לשכפול ה‑DNA. בתיאוריה, זה עשוי להישמע כמשהו חיובי, כי פעולה חזקה יותר של התרופה יכולה להיעשות כהתקפה יעילה יותר על הסרטן. אבל אותה השפעה מחמירה פוגעת גם בתאים בריאים המתפתחים במהירות, ובמיוחד במח העצם שבו מיוצרים תאי הדם. במחקר זה, מטופלים עם הווריאנט המסכן אכן חוו בעיות דמיות חמורות יותר ולא קיבלו שליטה טובה יותר על המחלה; להיפך, נטו להציג תוצאות גרועות יותר בטווח הארוך. המחברים מציעים כי אינטראקציות מורכבות בין החשיפה ממושכת לתרופה מ‑S-1 לבין מסלול החומצה הפולית המושפע עשויות לפגוע ברקמות בריאות ללא תוספת תועלת נגד הגידול.
מה עשוי הדבר לשנות בטיפול בעתיד
הממצאים מצביעים על וריאנט rs1801133 ב‑MTHFR כביו‑מרקר פוטנציאלי — רמז תורשתי שיוכל לסמן מטופלים שסביר שיסבלו מרעילות דמית ותוצאות גרועות יותר בטיפול הסטנדרטי ב‑S-1. המחקר עדיין אינו מוכיח שיש לשנות את הטיפול על סמך בדיקת DNA בודדת זו, אך הוא מעלה את האפשרות שבעתיד סקר גנטי יוכל לסייע לרופאים להתאים מינונים, להגביר מעקב או לשקול שיטות טיפול חלופיות למטופלים בסיכון גבוה יותר. במונחים פשוטים, העבודה מקרבת את הטיפול בסרטן צעד אחד לעולם שבו בחירת גלולה לא נקבעת רק על פי שלב הגידול, אלא גם על פי האופן שבו הגנים של כל אדם מעבדים את התרופה.
ציטוט: Kang, M., Kim, J.W., Lee, J.H. et al. MTHFR polymorphism is associated with increased adverse events and poor clinical outcomes in gastric cancer patients with adjuvant S-1 chemotherapy. Sci Rep 16, 14196 (2026). https://doi.org/10.1038/s41598-026-38429-3
מילות מפתח: סרטן הקיבה, כימותרפיית S-1, פראמקוגנומיקה, פולימורפיזם ב‑MTHFR, רעילות טיפולית