Clear Sky Science · ar
تغاير MTHFR مرتبط بزيادة الأحداث الضارة ونتائج سريرية أسوأ لدى مرضى سرطان المعدة الخاضعين للعلاج التكميلي S-1
لماذا يواجه بعض الناس صعوبة أكبر مع نفس حبة السرطان
قد يتناول مريضان نفس الحبة الكيميائية ويختبران نتائجٍ مختلفة تمامًا: ينهي أحدهما العلاج مع انزعاج طفيف فقط، بينما يواجه الآخر آثارًا جانبية شديدة وفرصة أكبر لعودة السرطان. تطرح هذه الدراسة سؤالًا بسيطًا لكنه حاسم لمرضى سرطان المعدة: هل يمكن للاختلافات الوراثية الشائعة في حمضنا النووي أن تفسر من ينجح ومن يتعرض لنتائج أسوأ عند استخدام دواء فموي شائع يسمى S-1؟
حبة صممت لتسهيل علاج قاسٍ
S-1 هو شكل فموي من العلاج الكيميائي يُستخدم بعد الجراحة لعلاج سرطان المعدة، خصوصًا في شرق آسيا. بدلًا من الحاجة لتسريب مستمر في المستشفى، يُؤخذ S-1 على هيئة حبوب لمدة عام، مما يجعل حياة المرضى أسهل. يعتمد الدواء على عامل مضاد للسرطان أقدم، 5-فلورويوراسيل، لكنه يضيف مكوّنين مساعدين يغيّران كيفية معالجته في الجسم. أظهرت تجارب سريرية كبيرة أن عامًا من S-1 بعد الجراحة يمكن أن يقلل من خطر عودة السرطان ويساعد المرضى على العيش لفترة أطول. لكن ليس الجميع يمكنهم تحمّل عام كامل من العلاج، وقد لاحظ الأطباء أن الآثار الجانبية والفوائد تختلف على نطاق واسع بين الأفراد.
البحث عن دلائل في الحمض النووي لدى المرضى المعالجين
درس الباحثون 334 شخصًا مصابًا بسرطان المعدة المرحلة الثانية أو الثالثة أُزيلت أورامهم جراحيًا ثم تناولوا S-1 كعلاج تكميلي (بعد الجراحة). كان لدى كل المشاركين وظائف أعضاء جيدة في البداية، وسُحِبَت عينات دم قبل العلاج الكيميائي للبحث عن اختلافات صغيرة وشائعة في الحمض النووي تُعرف بتبدلات النوكليوتيد المفردة (SNPs). ركز الفريق على 46 من هذه التبدلات في ستة جينات تساعد على معالجة 5-فلورويوراسيل والأدوية ذات الصلة. تبع الباحثون المرضى لفترة وسطية تزيد عن سبع سنوات، وسجلوا بدقة الآثار الجانبية للعلاج، وكمية الدواء التي تلقاها كل شخص على مدار الوقت، ومدة خلو المريض من السرطان، والبقاء الكلي على قيد الحياة.
متغير واحد شائع يبرز
من بين جميع العلامات الجينية، برز تغير واحد في جين يُدعى MTHFR كأهم علامة. يؤثر هذا المتغير، المسمى rs1801133، على إنزيم يدير مسار الفولات، وهو فيتامين مرتبط ارتباطًا وثيقًا ببناء وإصلاح الحمض النووي. كان الأشخاص الحاملون لنسختين من الشكل العرضي أكثر عرضة بحوالي ثلاثة أضعاف للإصابة بآثار جانبية دموية مثل فقر الدم أو انخفاض أعداد خلايا الدم البيضاء. وعند فحص النتائج طويلة الأمد، كان لدى المرضى الحاملين لنسخة عرضية واحدة على الأقل فترات أقصر من الخلو من السرطان وبقاء إجمالي أقصر مقارنة بمن يحملون النسخة النموذجية. كما أبدى جين آخر مشارك في تكسير الدواء، CYP2A6، ارتباطًا ببقاء خالٍ من السرطان أسوأ، لكن أثره كان أضعف وأقل اتساقًا.
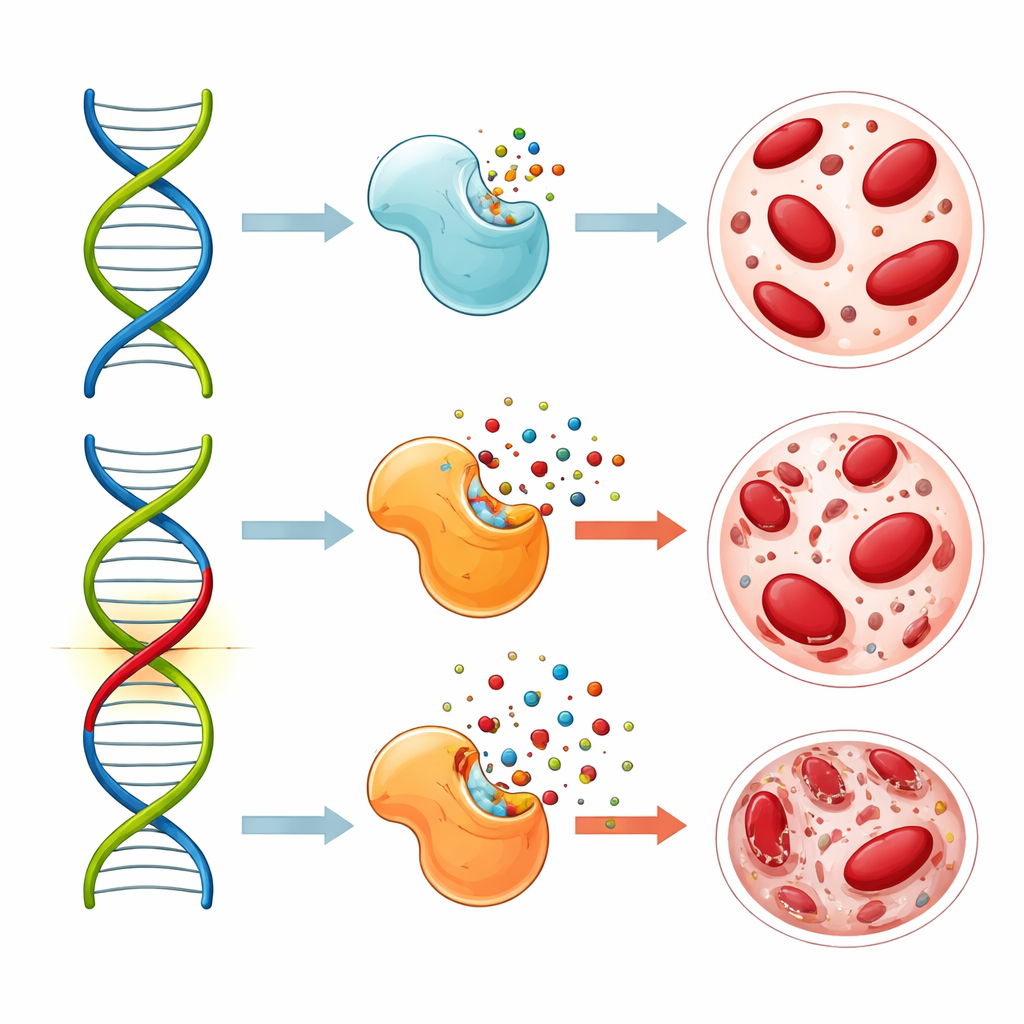
لماذا قد يزيد هذا التغير الجيني من الآثار الجانبية والنتائج
أظهرت أعمال مخبرية من دراسات أخرى أن متغير MTHFR يقلل نشاط إنزيمه، ما يغير توازن الفولات داخل الخلايا. يمكن لهذا التحول أن يجعل 5-فلورويوراسيل أكثر فاعلية في كبح الإنزيمات التي تستخدمها الخلايا السرطانية لنسخ حمضها النووي. من الناحية النظرية، قد يبدو ذلك أمرًا جيدًا، لأن تأثيرًا دوائيًا أقوى قد يعني هجومًا أقوى على السرطان. لكن التأثير المعزّز نفسه يصيب أيضًا الخلايا السريعة النمو في الأنسجة السليمة، خصوصًا نخاع العظم حيث تتكوّن خلايا الدم. في هذه الدراسة، أظهر المرضى الحاملون للنسخة العرضية مشاكل دموية أكثر خطورة ولم يحصلوا بشكل غير متوقع على تحكم أفضل في السرطان؛ بل مالوا إلى نتائج أسوأ على المدى الطويل. يقترح المؤلفون أن تداخلات معقدة بين التعرض المطوّل للدواء عبر S-1 ومسار الفولات المعدّل قد تضر بالأنسجة السليمة دون أن توفر فوائد إضافية ضد الورم.
ماذا قد يعني هذا لرعاية السرطان في المستقبل
تشير النتائج إلى متغير MTHFR rs1801133 كعلامة حيوية محتملة — دليل وراثي قد ينبه إلى المرضى الأكثر عرضة لسمية دموية وذوي النتائج الأسوأ على العلاج القياسي S-1. لا تثبت الدراسة بعد أن العلاج يجب أن يتغير بناءً على اختبار وراثي واحد، لكنها تفتح احتمال أن يساعد الفحص الجيني مستقبلًا الأطباء على تعديل الجرعات، زيادة المتابعة، أو النظر في نظم علاجية بديلة للمرضى ذوي الخطر الأعلى. ببساطة، تحرك هذه النتائج رعاية السرطان خطوة أقرب إلى عالم تُختار فيه الحبة ليس فقط حسب مرحلة الورم، بل أيضًا حسب كيفية تعامل جينات كل شخص مع الدواء.
الاستشهاد: Kang, M., Kim, J.W., Lee, J.H. et al. MTHFR polymorphism is associated with increased adverse events and poor clinical outcomes in gastric cancer patients with adjuvant S-1 chemotherapy. Sci Rep 16, 14196 (2026). https://doi.org/10.1038/s41598-026-38429-3
الكلمات المفتاحية: سرطان المعدة, العلاج الكيميائي S-1, علم الجينات الدوائي, تغاير MTHFR, سمية العلاج