Clear Sky Science · fr
ARN intron mobile d’un prédateur bactérien s’accumule dans des cellules archées mortes
Petits prédateurs et messages cachés
Dans les recoins sombres et privés d’oxygène de notre planète, des prédateurs microscopiques chassent d’autres microbes dans des batailles au ralenti qui façonnent le recyclage du carbone et la production de méthane. Cette étude examine un voyageur inattendu présent lors de ces rencontres : un fragment d’ARN génétique d’un prédateur bactérien qui finit à l’intérieur de cellules mortes d’un autre domaine de la vie, les archées. Ce travail offre un rare aperçu en temps réel de la manière dont des éléments génétiques peuvent sauter entre des branches éloignées de l’arbre du vivant, étayant des idées anciennes sur le transfert horizontal de gènes et le monde primitif de l’ARN.
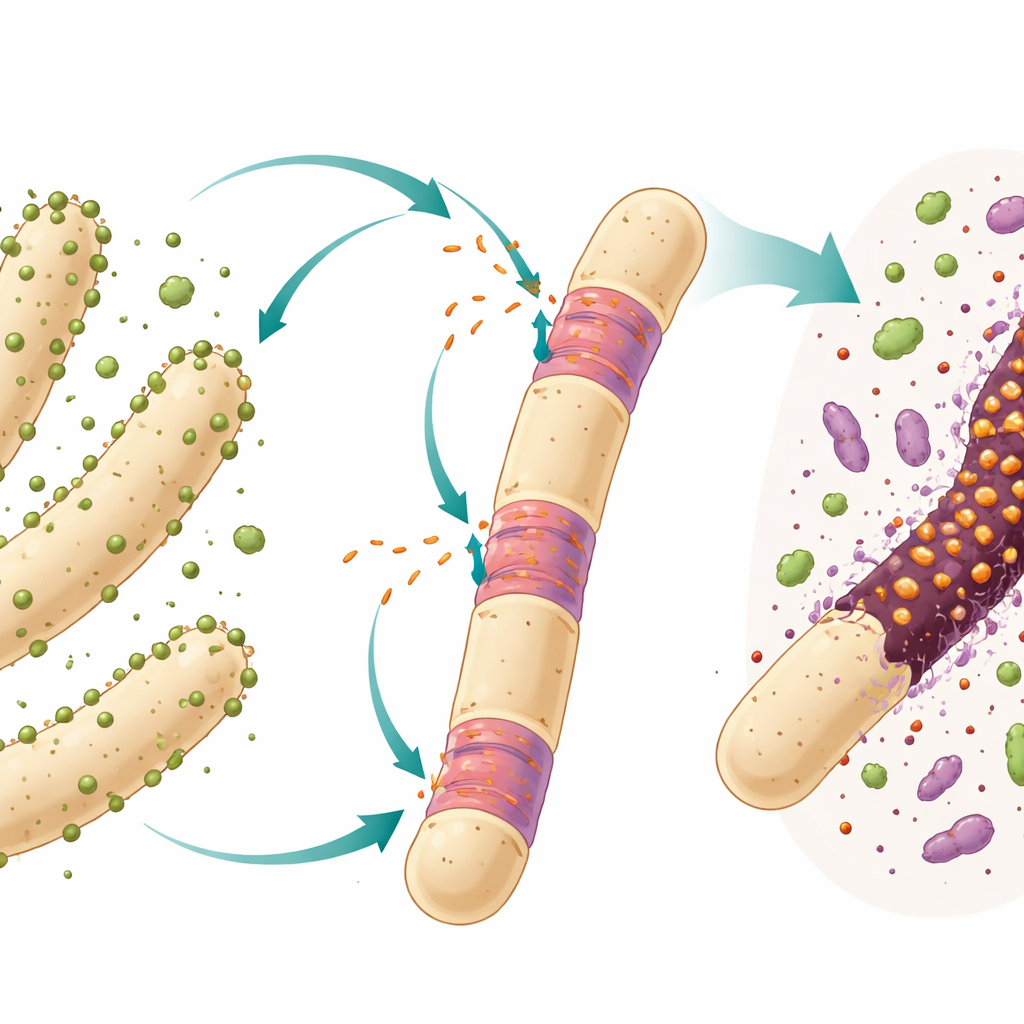
Gènes sauteurs chez les cellules simples
De nombreuses bactéries et archées portent des passagers génétiques appelés introns, des segments d’ADN copiés en ARN puis excisés avant d’obtenir un ARN fonctionnel. Chez les organismes complexes, les introns sont des caractéristiques usuelles des gènes, mais dans les cellules simples ils sont plus rares et se comportent souvent comme des éléments mobiles qui peuvent se déplacer et envahir de nouveaux emplacements du génome. L’étude se concentre ici sur un intron particulier de type « groupe I » situé dans le gène de l’ARN ribosomal 23S d’un prédateur bactérien ultraminuscule nommé Candidatus Velamenicoccus archaeovorus. Cette bactérie vit attachée à des cellules archées filamentaires dans une culture de laboratoire de longue date qui dégrade le composé végétal limonène et produit lentement du méthane.
Un monde microbien lent et confiné
Les chercheurs ont travaillé sur une culture d’enrichissement anaérobie maintenue depuis plus de vingt ans sur du limonène avec un seul transfert par an. Dans ce système fermé, différents microbes coopèrent et rivalisent. Un partenaire bactérien dégrade le limonène en composés plus petits, et plusieurs archées méthanogènes, dont l’espèce filamenteuse Methanothrix soehngenii, transforment ces produits en méthane. L’ultramicrobactérie Ca. Velamenicoccus archaeovorus vit en épibionte, attachée à la surface de ces filaments. Des travaux antérieurs ont suggéré qu’elle agit comme un prédateur : certaines cellules filamenteuses semblent mortes mais contiennent encore de l’ADN et des lipides, ce qui suggère que le prédateur extrait des composants cellulaires essentiels tout en laissant derrière lui une coque partielle.
Voir de l’ARN étranger à l’intérieur de cellules mortes
Pour tester si le prédateur envoie son ARN intron dans ses victimes archées, l’équipe a utilisé une technique d’imagerie sensible appelée CARD‑FISH, qui emploie de courtes sondes d’ADN marquées pour illuminer les molécules d’ARN correspondantes à l’intérieur de cellules fixées. Ils ont conçu trois sondes reconnaissant l’ARN de l’intron et les ont combinées avec des sondes pour l’ARN ribosomal du prédateur et un marquage de l’ADN. Au microscope, le signal de l’intron est apparu à la fois dans les petites cellules sphériques du prédateur et, surtout, à l’intérieur de certains segments des longs filaments de Methanothrix. Ces cellules filamenteuses montrant le signal de l’intron avaient perdu leur propre ARN ribosomal, un signe de mort, mais contenaient encore de l’ADN, confirmant qu’elles étaient mortes mais pas encore entièrement décomposées. Des sondes témoins aux séquences inversées n’ont pas produit de signal, ce qui indique que le marquage était spécifique de l’intron.
Compter ces rares voyageurs d’ARN
Pour compléter l’imagerie, les auteurs ont réexaminé un important jeu de données de séquençage d’ARN précédemment généré à partir de la même culture. Comme l’ARN ribosomal n’avait pas été retiré de cet échantillon, ils ont pu comparer directement la fréquence d’apparition de la séquence de l’intron par rapport à l’ARN 23S mature et pleinement traité. Ils ont constaté que les lectures correspondant à l’intron représentaient environ 1 sur 20 000 par rapport à l’ARN 23S mature, ce qui signifie que la plupart des copies d’intron sont effectivement excisées du transcrit primaire. Quelques lectures franchissaient les jonctions entre l’intron et la séquence voisine, indiquant qu’une très petite fraction des transcrits restait non épissée. Conjuguées à l’imagerie, ces données montrent que des molécules d’intron excisées existent dans la culture et peuvent se trouver en dehors de leur cellule hôte d’origine.
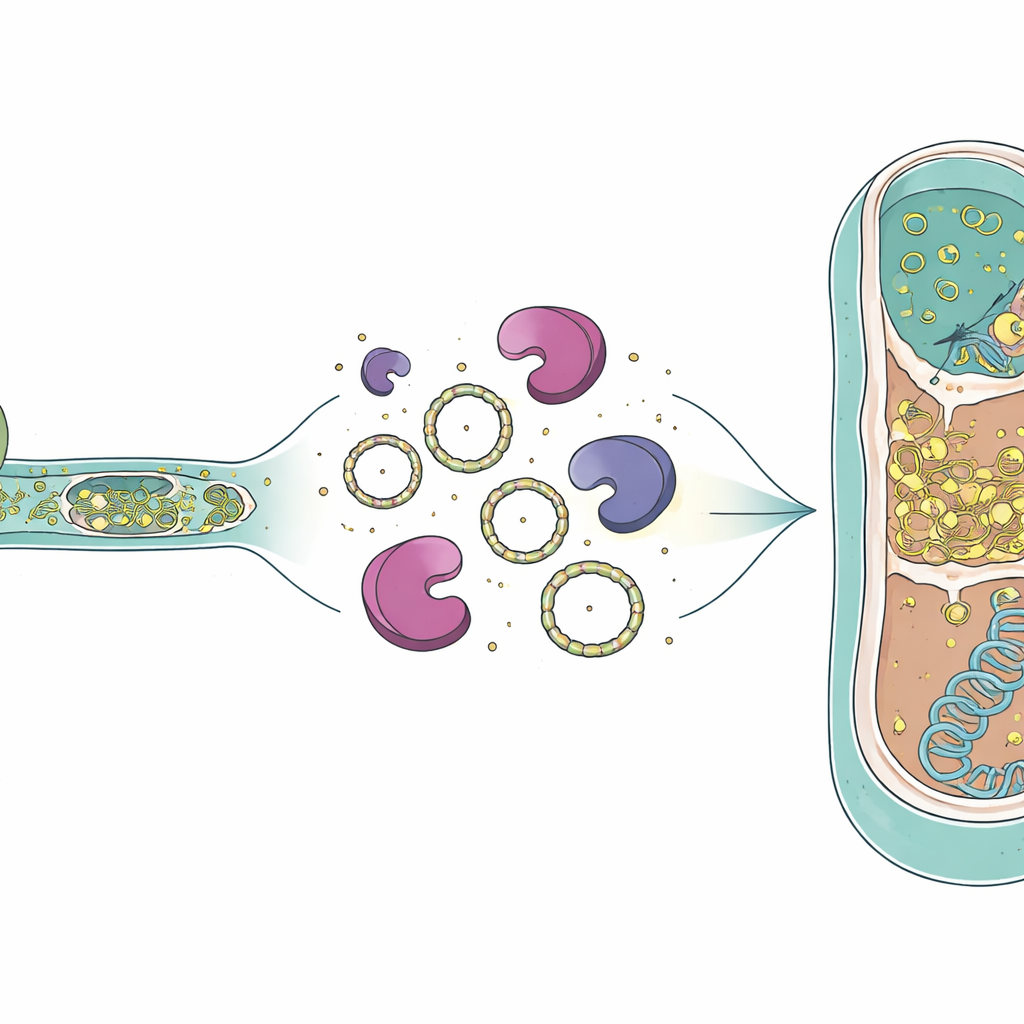
Comment l’ARN peut survivre et se propager
La présence d’ARN d’intron à l’intérieur de cellules archées mortes soulève la question de la durée de vie de ces molécules. Des travaux antérieurs ont montré que les introns de groupe I peuvent former des anneaux d’ARN circulaires après l’épissage, et ces cercles résistent mieux aux enzymes qui dégradent l’ARN. Le génome du prédateur code aussi pour une transcriptase inverse spéciale — une enzyme capable de copier l’ARN en ADN — qui avait été détectée auparavant comme protéine dans la même culture. Des images en microscopie électronique d’études antérieures montraient des contacts cytoplasmiques ouverts entre prédateur et victime, suggérant que non seulement de l’ARN mais possiblement cette enzyme pourraient passer dans la cellule archée. Si l’ARN intron circulaire et une transcriptase inverse entrent ensemble dans une cellule victime, ils pourraient en principe être copiés en ADN et insérés dans le génome archéen, créant un nouvel intron chez un nouvel hôte.
Pourquoi cela compte pour le trafic génétique de la vie
Pour les non‑spécialistes, la conclusion principale est que cette étude apporte une preuve directe et microscopique qu’un fragment mobile d’ARN bactérien peut quitter sa cellule d’origine et s’accumuler dans les restes morts d’un microbe très différent. Ce mouvement constitue une étape clé du transfert horizontal de gènes, le processus par lequel des gènes et des éléments génétiques se propagent entre espèces. Le travail élargit aussi les rôles connus de l’ARN extracellulaire, qui incluent déjà la signalisation et l’inhibition de la croissance, en y ajoutant les introns mobiles. À plus grande échelle, ces ARN mobiles et leurs enzymes associées aident à expliquer comment des innovations génétiques ont été redistribuées au sein des communautés microbiennes au cours de l’évolution, brouillant les frontières entre des branches séparées du vivant.
Citation: Kizina, J., Lonsing, A. & Harder, J. Mobile intron RNA from a bacterial predator accumulates in dead archaeal cells. Sci Rep 16, 14654 (2026). https://doi.org/10.1038/s41598-026-51721-6
Mots-clés: introns mobiles, ARN extracellulaire, prédation microbienne, transfert horizontal de gènes, archées méthanogènes