Clear Sky Science · es
Segmentación automatizada de cálculos renales en videos de ureteroscopia flexible mediante un modelo U‑Net: un estudio preliminar de viabilidad
Ayudando a los cirujanos a ver cálculos renales ocultos
Los cálculos renales son un problema doloroso y cada vez más frecuente, y una de las principales formas de tratarlos consiste en introducir una cámara diminuta en el riñón y fragmentar las piedras con un láser. Pero dentro del cuerpo la vista puede ser confusa: sangre, polvo de la piedra fracturada y el movimiento por la respiración dificultan que los cirujanos vean con claridad. Este estudio explora si la inteligencia artificial (IA) puede funcionar como un resaltador en tiempo real para los cálculos durante la cirugía, haciendo que se distingan mejor en la pantalla y potencialmente agilizando y haciendo más segura la intervención.
Por qué es difícil tratar los cálculos renales
Los cálculos renales afectan a una gran proporción de adultos en todo el mundo y pueden causar dolor intenso, infecciones e incluso insuficiencia renal. El tratamiento moderno emplea a menudo la ureteroscopia flexible, en la que los médicos guían un endoscopio flexible con cámara por las vías urinarias hasta el riñón. Una vez allí, usan un láser para fragmentar las piedras en pedazos más pequeños. Sin embargo, la imagen de la cámara está lejos de ser perfecta. Hemorragias repentinas, nubes de polvo producidas por el láser, cambios de iluminación y movimientos rápidos pueden emborronar la vista. Los cirujanos deben decidir continuamente dónde termina la piedra y dónde comienza el tejido circundante. Si pasan por alto fragmentos, los pacientes pueden necesitar procedimientos repetidos; si interpretan mal el campo, aumenta el riesgo de complicaciones.
Enseñar a un ordenador a detectar piedras
Para abordar este reto, los investigadores entrenaron un programa informático para delimitar automáticamente los cálculos en la secuencia de vídeo del endoscopio. Reunieron 12 grabaciones completas de cirugías de distintos pacientes, que sumaban alrededor de 11 horas de metraje del mundo real. A partir de estos vídeos extrajeron miles de fotogramas individuales y diseñaron un sistema semiautomático para marcar dónde estaban las piedras. Primero, revisores humanos trazaron recuadros sencillos alrededor de las piedras visibles. Luego, una herramienta separada generó formas más precisas dentro de esos recuadros y expertos médicos comprobaron que coincidían con las áreas reales de la piedra. Estas imágenes y contornos emparejados se emplearon para entrenar un modelo de aprendizaje profundo basado en la arquitectura U‑Net, un tipo de red popular para segmentación de imágenes que puede indicar exactamente qué píxeles pertenecen a la piedra.
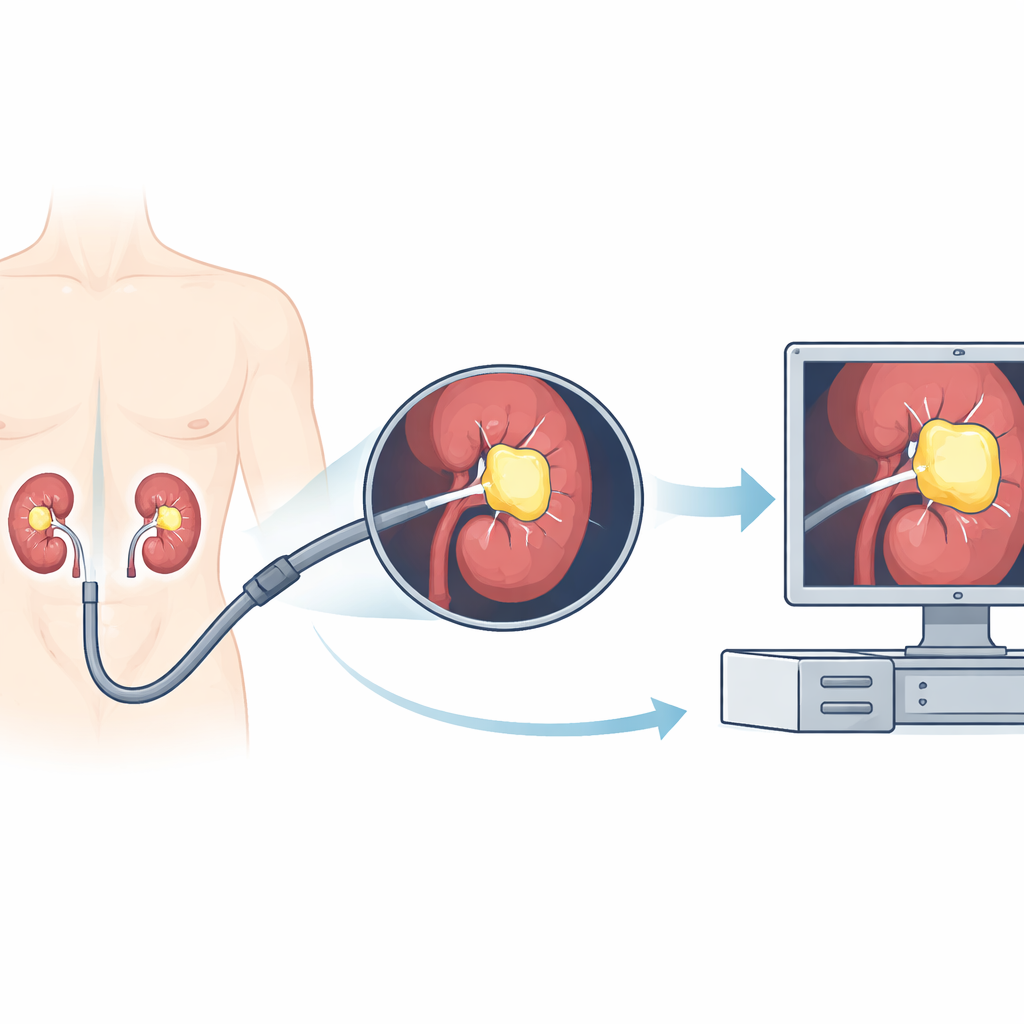
Cómo se comportó el modelo de IA
El equipo dividió cuidadosamente sus datos de modo que algunas cirugías sirviesen para enseñar al modelo, otras para afinarlo y otras se mantuvieran completamente separadas para probar su rendimiento en operaciones nuevas, no vistas. En estos vídeos retenidos, la IA clasificó correctamente la mayoría de los píxeles en cada fotograma y mostró una fuerte superposición entre sus contornos de la piedra y las marcas de los expertos. En términos sencillos, cuando la piedra era claramente visible y la imagen de la cámara estaba nítida, el sistema trazaba un límite ceñido y preciso a su alrededor. El modelo también fue rápido: en una tarjeta gráfica estándar procesó alrededor de 30 fotogramas por segundo, similar a la velocidad de un flujo de vídeo en directo, lo que sugiere que su uso en tiempo real en el quirófano es técnicamente factible.
Cuando la imagen se vuelve confusa
El rendimiento cayó cuando el vídeo se parecía más a una tormenta de nieve que a una imagen clara. En fotogramas con sangrado abundante, densas nubes de polvo provocadas por el láser o fuerte desenfoque por movimiento, el modelo a veces confundía restos brillantes con piedra real o no detectaba partes de la piedra. Un análisis más detallado comparó fotogramas "claros", con mínimo ruido, con fotogramas "borrosos" llenos de artefactos. La IA se comportó notablemente mejor en el grupo claro, lo que confirma que la mala visibilidad dificulta la delimitación precisa incluso para un algoritmo entrenado. Dado que el modelo analiza cada fotograma por separado, aún no puede aprovechar el movimiento a lo largo del tiempo para distinguir una piedra estable de polvo o trazas de sangre pasajeras.
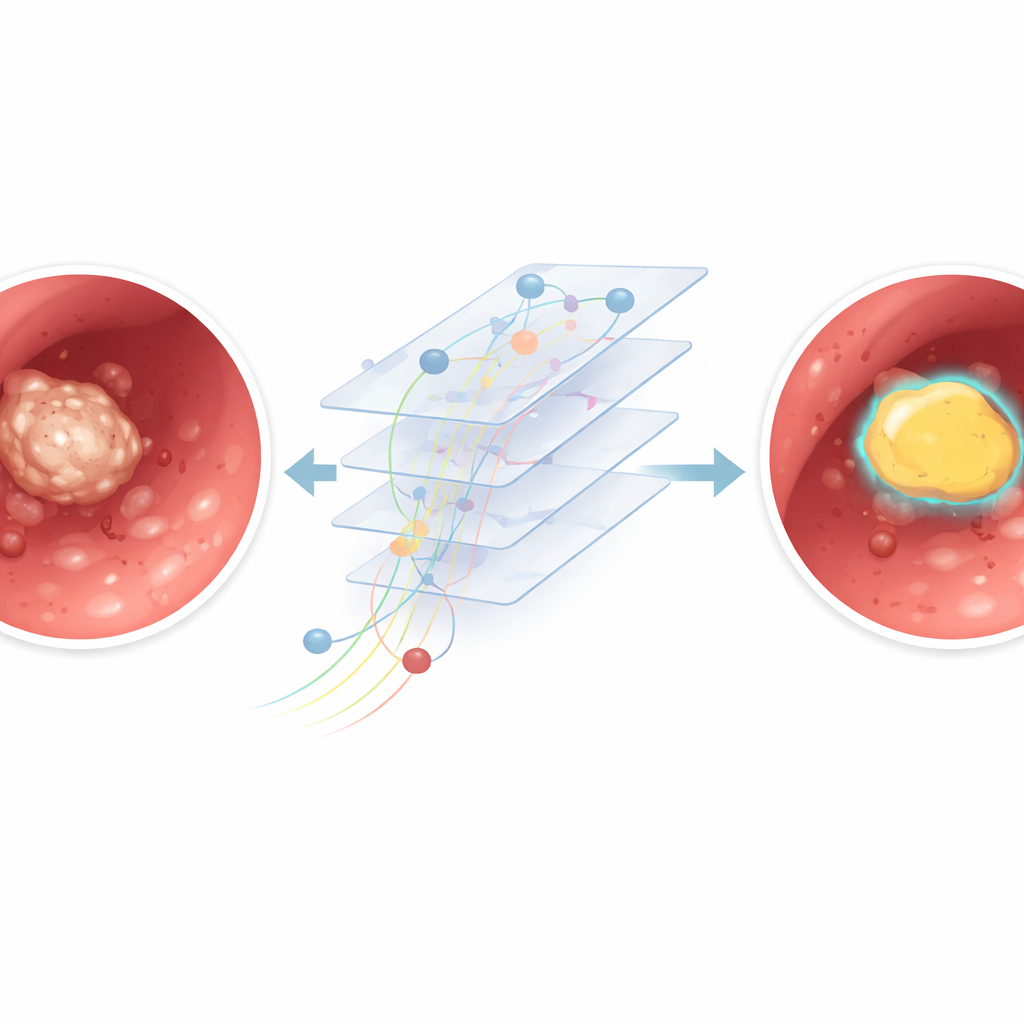
Qué podría significar esto para futuras cirugías
Este trabajo es un paso inicial más que una herramienta lista para usar en hospitales. El estudio empleó un número moderado de vídeos de un único centro, con un conjunto limitado de tipos de cámara, y el proceso de anotación puede seguir conteniendo imperfecciones humanas y algorítmicas. El sistema aún no se ha integrado en un flujo de trabajo quirúrgico completo, donde la fiabilidad, las comprobaciones de seguridad y las limitaciones de hardware son cuestiones clave. Aun así, los resultados muestran que un modelo de IA puede aprender a localizar y delinear cálculos renales directamente a partir de vídeos quirúrgicos reales y mantener el ritmo de la velocidad en directo. Con conjuntos de datos más amplios y diversos, un uso más inteligente de la información entre fotogramas consecutivos y pruebas cuidadosas en quirófanos reales, sistemas similares podrían acabar ayudando a los cirujanos a que las piedras ocultas destaquen con mayor claridad, reduciendo fragmentos pasados por alto y mejorando la atención al paciente.
Cita: El Hajj, A., Bou Mrad, A., Malik, E. et al. Automated kidney stone segmentation from flexible ureteroscopy videos using a U-net model: A preliminary feasibility study. Sci Rep 16, 14542 (2026). https://doi.org/10.1038/s41598-026-45143-7
Palabras clave: cálculos renales, IA quirúrgica, video endoscópico, imágenes médicas, aprendizaje profundo