Clear Sky Science · zh
解析癌症与细菌组相互作用的意义与挑战
为什么微小住客对癌症至关重要
每个人体内都带有数万亿细菌,它们默默地与我们共居,在皮肤、口腔、肺部,尤其是在肠道中形成丰富的群落。本文探讨了一个挑衅性的观点:这些微生物邻居既可能促成癌症,也可能在重要程度上抑制癌症。通过检视整套细菌群落如何与肿瘤相互作用——以及为何研究它们在技术上如此困难——作者认为理解这一隐秘生态系统可能为癌症的早期发现和治疗开辟新路径。
我们体内的隐秘世界
人体是一个巨大的“细菌组”之家,包含数千种细菌,其总体细胞数可与我们自身细胞相媲美。不同器官拥有不同的细菌组合,这些组合随时间和个体而变化。研究人员现已发现,某些细菌种类可通过损伤DNA、引发长期炎症或阻断机体对失控生长的内在制动,推动健康细胞走向癌变。另一些细菌则似乎相反,能够动员免疫细胞攻击肿瘤或改变肿瘤环境以减缓癌症发展。然而,我们的大多数常驻细菌从未被测试其对癌症的影响,留下了一个巨大而未知的潜在帮手与罪魁祸首的景观。
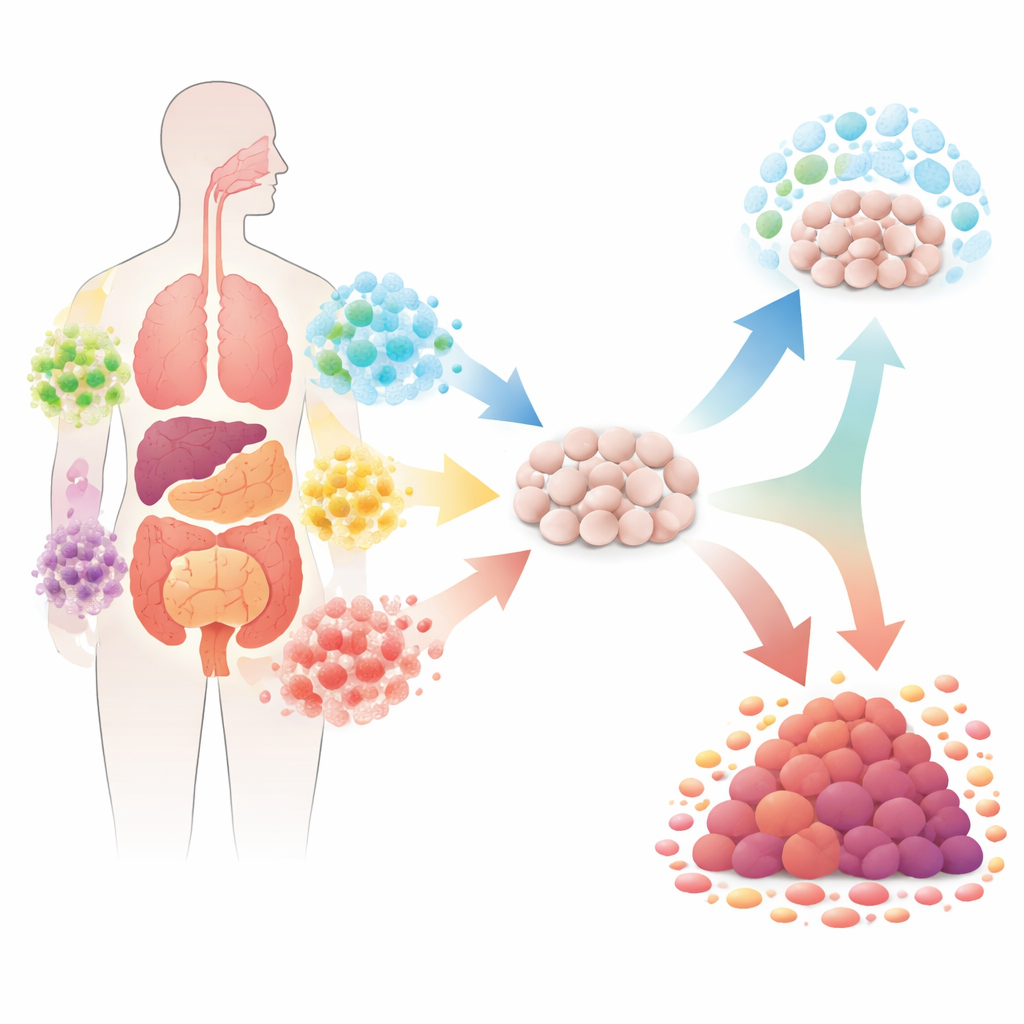
细菌如何推动细胞走向肿瘤
文章回顾了若干研究充分的例子,展示细菌如何促发或助长肿瘤。在胃内,幽门螺杆菌会引发免疫细胞的大规模反应,这些免疫细胞释放反应性分子,损伤DNA并促进可导致癌变的长期炎症。某些大肠杆菌菌株产生一种名为colibactin的小而不稳定的化学物质,直接损害DNA,增加邻近细胞的突变率。在结肠中,核梭杆菌(Fusobacterium nucleatum)和脆弱拟杆菌(Bacteroides fragilis)都可以扰乱控制细胞增殖与凋亡的关键信号通路。这些案例共同揭示了一个常见模式:细菌通过多年反复造成组织DNA、免疫平衡与生长控制的应激,从而塑造癌症风险。
从相关性走向因果
迄今为止,许多研究通过比较有无癌症者的微生物组,使用DNA测序来记录哪些细菌存在。这类工作已将特定物种和更广泛的细菌群落与肠道、口腔、肺、肝、皮肤及其他器官的癌症联系起来。但此类快照式研究有其局限:它们能显示关联,却无法证明某一微生物导致疾病。它们遗漏了仅在特定组合中危险的细菌,并且难以识别那些悄然保护免于癌变的微生物。作者概述了几种概念性策略——从逐一研究单一物种,到比较大规模患者群体,再到追踪癌细胞与复杂细菌混合群的共同演化——这些方法各自捕捉到图景的一部分,但都不足以全面绘制细菌组如何塑造肿瘤的全貌。
将癌症实验缩小到微小液滴中
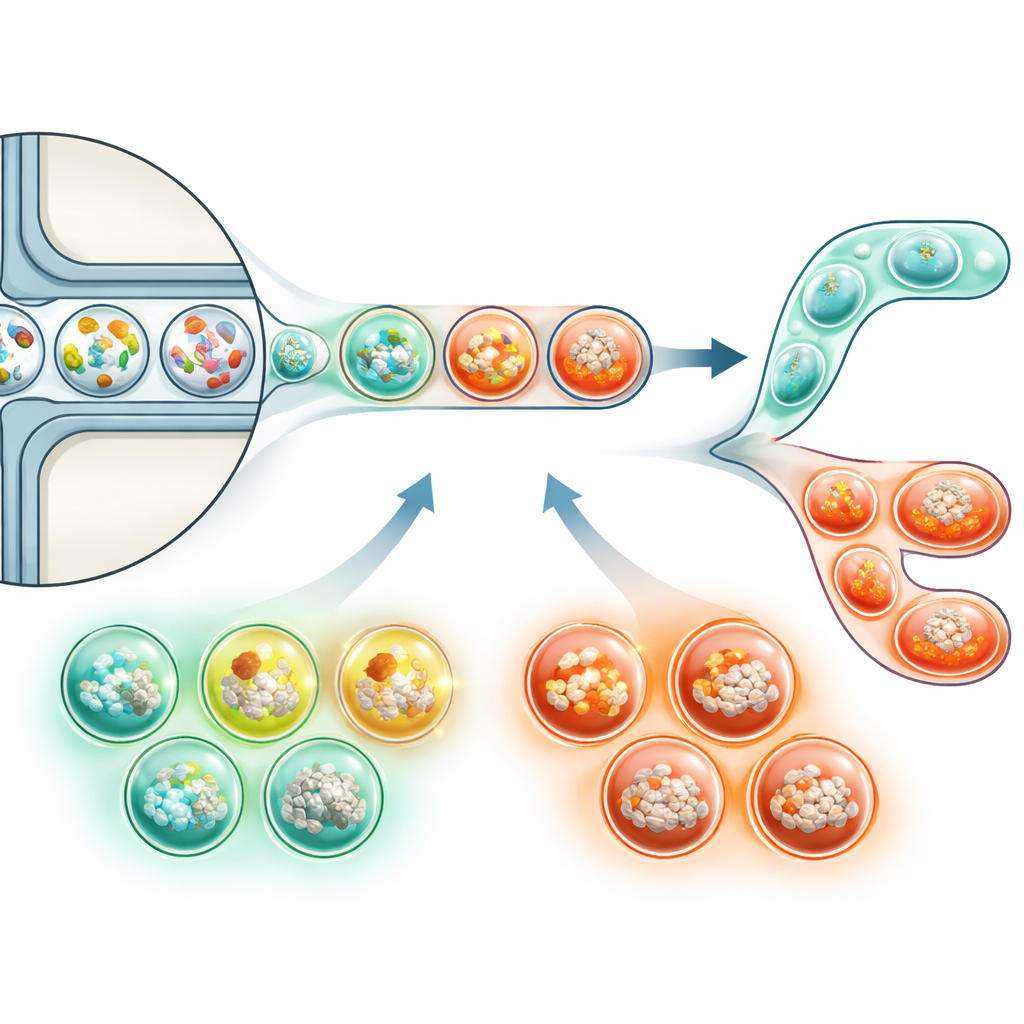
为弥补这些空白,文章重点介绍了将实验缩小到数百万微小液滴的微流控技术。每个液滴都可作为一个微小试管,承载独特的细菌与人类细胞混合物。借助巧妙的芯片设计,研究者可以快速生成、培养并根据简单信号(例如报告癌细胞生长的荧光)对液滴进行分拣。液滴内的DNA“条形码”使得随后可以对所有遗传物质进行批量测序,同时仍能追踪哪些细菌和细胞来自哪个液滴。结合强大的测序方法,这一方法最终可让科学家并行测试成千上万种不同的微型细菌群落对癌细胞的影响,揭示既促癌又抑癌的组合。
理解数据洪流
这种高通量实验会产生巨大且复杂的数据集。作者描述了统计工具、降维技术、网络分析和现代人工智能如何帮助梳理这一洪流。这些方法可以突出模式,例如在侵袭性肿瘤或显然受保护的组织中倾向于共同出现的细菌群,并能提出可检验的假设,说明不同微生物彼此以及与肿瘤如何相互作用。重要的是,基于生物学的计算模型可将这些模式转化为关于因果机制的可操作想法,指导下一轮实验。
将微生物生态学转化为医学
最终,文章认为仅关注人类基因与细胞不足以全面理解癌症。我们的常驻细菌形成了一个生态背景,能将平衡倾向于疾病或健康。通过开发研究整套细菌群落与癌细胞并行的方法——并将这些实验与先进的数据分析工具配对——研究人员希望从仅识别危险微生物,转向有意重塑细菌组。长期愿景大胆:不仅直接靶向肿瘤来预防或治疗癌症,还要工程化我们体内的微生物生态系统,以达到治疗效果。
引用: Alshareedah, I., Brunner, J.D., Chain, P.S.G. et al. Significance and challenges in dissecting cancer-bacteriome interactions. BJC Rep 4, 22 (2026). https://doi.org/10.1038/s44276-026-00229-7
关键词: 癌症微生物组, 细菌组, 肿瘤微环境, 微流控, 微生物治疗