Clear Sky Science · ar
أهمية وتحديات تفكيك تفاعلات السرطان مع البكتريوم
لماذا تهمّ القاطنون الصغار في السرطان
يحمل كل إنسان تريليونات من البكتيريا التي تتشارك أجسامنا بهدوء، مكونة مجتمعات غنية على الجلد، وفي الفم والرئتين، وخاصة في الأمعاء. تستعرض هذه المقالة فكرة مثيرة: أن هؤلاء الجيران الميكروبيين قد يساهمون في دفع تطور السرطانات أو، وبقدر الأهمية، قد يساعدون في كبحها. من خلال فحص كيفية تفاعل مجتمعات البكتيريا بأكملها مع الأورام — ولماذا من الصعب تقنياً دراستها — يجادل المؤلفون بأن فهم هذا النظام البيئي المخفي قد يفتح طرقًا جديدة لاكتشاف السرطان مبكراً وعلاجه.
العالم الخفي بداخلنا
يحتضن الجسم البشري «بكتريوماً» هائلاً، آلاف الأنواع البكتيرية التي يصل مجموع خلاياها إلى حد ينافس خلايانا. تستضيف أعضاء مختلفة مزيجاً مميزاً من البكتيريا، وتتبدل هذه التراكيب مع الزمن ومن شخص لآخر. يعرف الباحثون الآن أن بعض الأنواع البكتيرية يمكن أن تدفع الخلايا السليمة نحو السرطان عن طريق تلف الحمض النووي، أو إشعال التهاب طويل الأمد، أو تعطيل آليات الجسم المانعة للنمو غير المنضبط. في المقابل، تبدو أنواع أخرى قادرة على العكس، بجذب خلايا المناعة لمهاجمة الأورام أو تغيير بيئة الورم بطرق تبطئ السرطان. ومع ذلك، لم تُختبر معظم بكتيراتنا المقيِّمة تأثيراتها على السرطان، تاركة مشهداً واسعاً من المجهول لِمَن قد يكون مساعداً أو مُضرّاً.
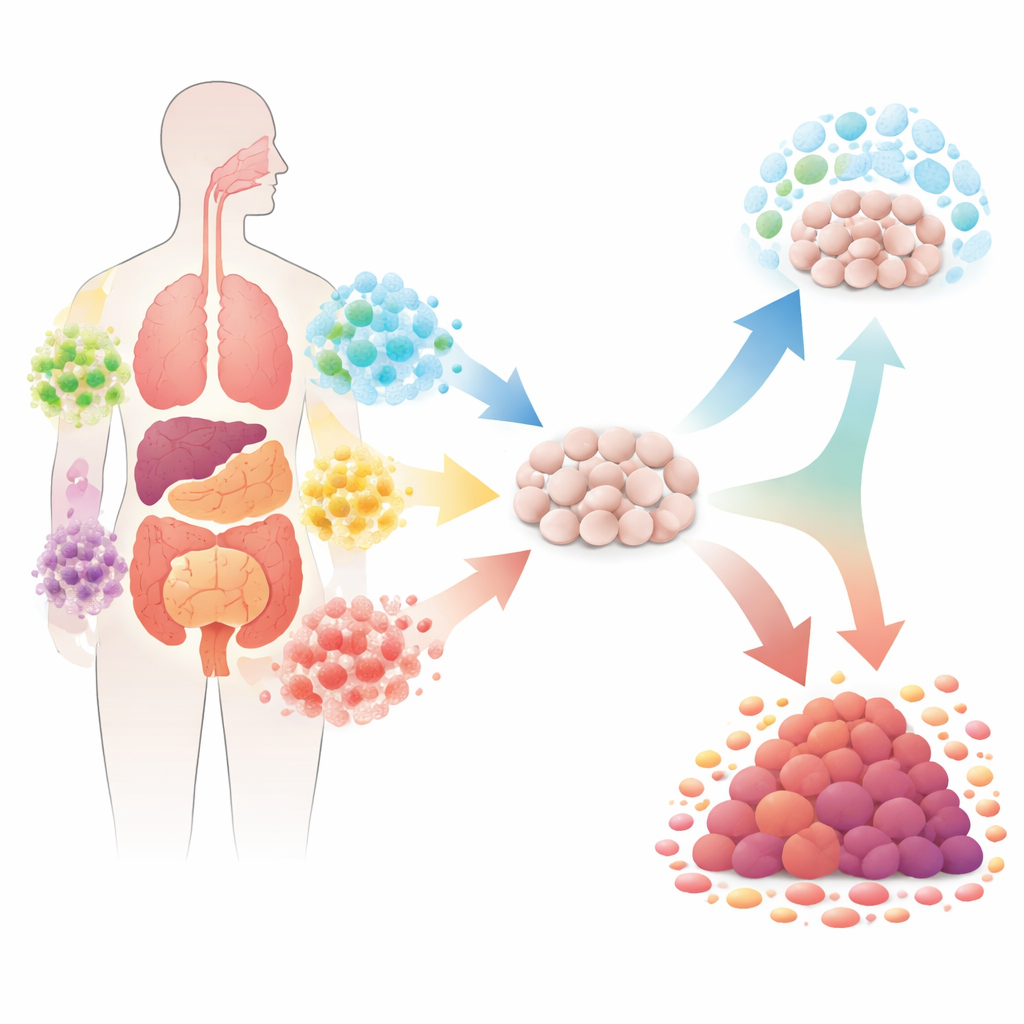
كيف يمكن للبكتيريا دفع الخلايا نحو الأورام
تستعرض المقالة عدة أمثلة مدروسة جيداً توضح كيف يمكن للبكتيريا أن تساهم في إشعال أو تغذية الأورام. في المعدة، يثير الهيليكوباكتر بيلوري موجات من الخلايا المناعية التي تطلق جزيئات تفاعلية تضرّ الحمض النووي وتؤدي إلى التهاب مزمن قد يتطور إلى سرطان. بعض سلالات الإشريكية القولونية تصنع مركباً صغيراً وغير مستقر يُدعى كوليبكتين يضرّ بالحمض النووي مباشرةً، ما يزيد من معدلات الطفرات في الخلايا المجاورة. في القولون، يمكن لكل من الفوسفوريبكتريوم نُكليتبوم والبطريودس فراجيليس أن يعطّلا مسارات إشارة رئيسية تتحكم بسرعة انقسام الخلايا ومواعيد موتها. تكشف هذه الحالات مجتمعة عن نمط شائع: يمكن للبكتيريا أن تشكل خطر الإصابة بالسرطان عبر إجهاد الحمض النووي وتوازن المناعة وآليات النمو في الأنسجة على مدى سنوات عديدة.
من الارتباط إلى السببية
قارن العديد من الدراسات حتى الآن الميكروبيومات لدى أشخاص مصابين وغير مصابين بالسرطان، مستخدمةً تسلسل الحمض النووي لحصر الأنواع البكتيرية الموجودة. ربطت هذه الأعمال أنواعاً محددة ومجتمعات بكتيرية أوسع بسرطانات الأمعاء والفم والرئتين والكبد والجلد وأعضاء أخرى. لكن هذه اللقطات لها حدود؛ فهي تظهر الارتباط وليس دليلاً قاطعاً على أن ميكروباً ما يسبب المرض. كما أنها قد تفوت بكتيريا تصبح ضارة فقط ضمن تركيبات معينة، وتكافح في كشف الميكروبات التي تحمي السرطان بهدوء. يحدد المؤلفون عدة استراتيجيات مفاهيمية — من دراسة نوع واحد في كل مرة، إلى مقارنة مجموعات كبيرة من المرضى، إلى تتبع التطور المشترك لخلايا السرطان وخلطات بكتيرية معقدة — كل منها يلتقط جزءاً من الصورة لكنه يقصر عن رسم خارطة كاملة لكيفية تشكيل البكتريوم للأورام.
تصغير تجارب السرطان إلى قطرات ميكروسكوبية
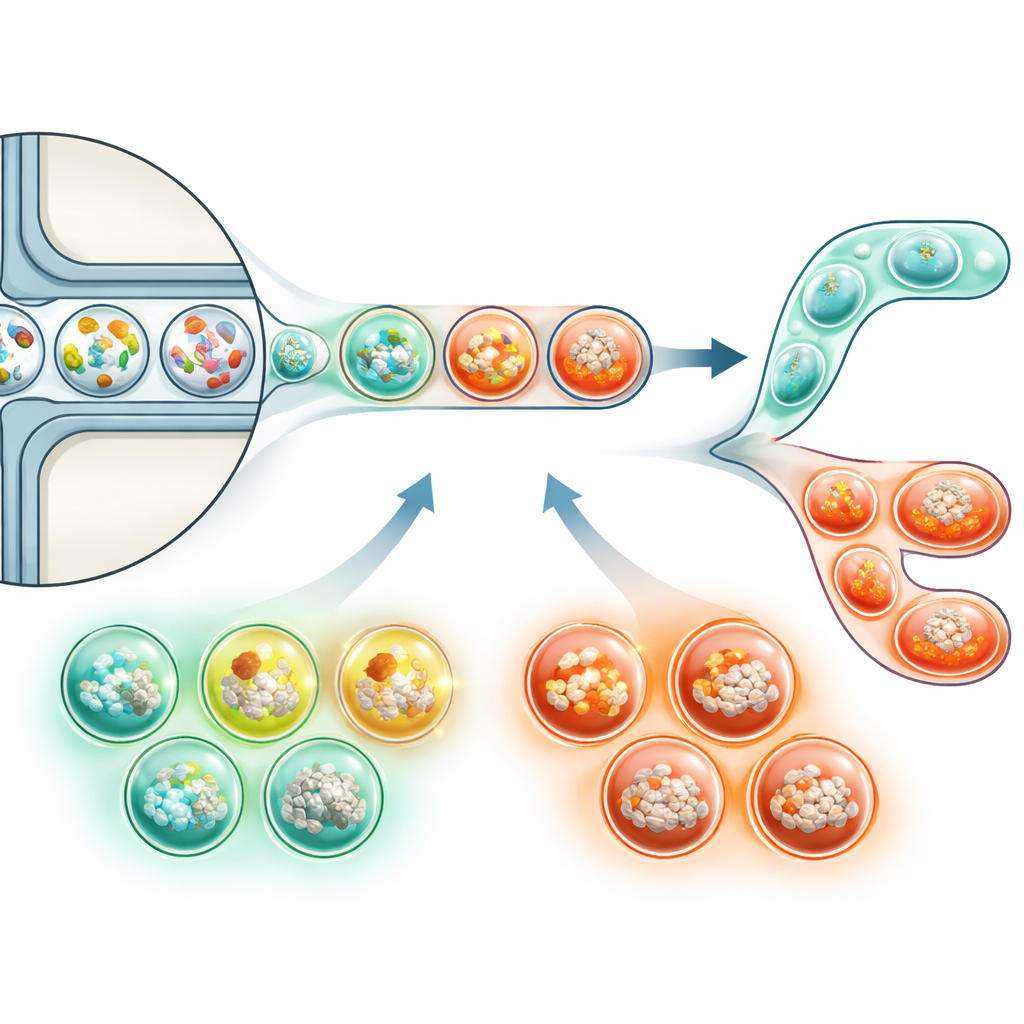
لتغطية هذه الثغرات، تسلط المقالة الضوء على تقنيات الميكروفلويديات التي تصغّر التجارب إلى ملايين القطرات الميكروسكوبية. يمكن لكل قطرة أن تعمل كأنبوب اختبار صغير، تحوي مزيجاً فريداً من البكتيريا والخلايا البشرية. باستخدام تصاميم شرائح ذكية، يستطيع الباحثون توليد هذه القطرات بسرعة ونموها وفرزها بناءً على إشارات بسيطة، مثل التألق الذي يدل على نمو خلايا السرطان. تجعل «الباركودات» الوراثية داخل القطرات من الممكن لاحقاً تسلسل كل المادة الجينية دفعة واحدة مع تتبع أي البكتيريا والخلايا جاءت من أي قطرة. مدموجة مع طرق تسلسل قوية، قد تتيح هذه النهج للعلماء أخيراً اختبار آلاف مجتمعات بكتيرية مصغرة مقابل خلايا سرطانية بالتوازي، مكشفةً التراكيب التي تروّج للسرطان وتلك التي تكبحه.
فهم فيض البيانات
تولد هذه التجارب عالية الإنتاجية مجموعات بيانات ضخمة ومعقدة. يصف المؤلفون كيف يمكن للأدوات الإحصائية، وتقنيات تخفيض الأبعاد، وتحليل الشبكات، والذكاء الاصطناعي الحديث أن تساعد في غربلة هذا الفيضان. تستطيع هذه الطرق إبراز أنماط، مثل مجموعات من البكتيريا التي تميل للظهور معاً في سرطانات عدوانية أو في أنسجة تبدو محمية، كما يمكنها اقتراح فرضيات قابلة للاختبار حول كيفية تفاعل الميكروبات مع بعضها البعض ومع الأورام. ومن المهم أن تُستند النماذج الحاسوبية إلى الأساس البيولوجي لتحويل هذه الأنماط إلى أفكار آلية عن السببية، موجهةً جولة التجارب التالية.
تحويل علم البيئة الميكروبية إلى طب
في النهاية، يجادل المقال بأن السرطان لا يمكن فهمه بالكامل إذا ركزنا فقط على الجينات والخلايا البشرية. تشكل بكتيراتنا المقيمة خلفية بيئية يمكن أن تميل بالتوازن نحو المرض أو الصحة. من خلال تطوير طرق جديدة لدراسة مجتمعات بكتيرية كاملة جنباً إلى جنب مع خلايا السرطان — ومزاوجة هذه التجارب بأدوات تحليل بيانات متقدمة — يأمل الباحثون أن ينتقلوا من مجرد رصد الميكروبات الخطرة إلى إعادة تشكيل البكتريوم عمداً. الرؤية بعيدة المدى جريئة: الوقاية من السرطان أو علاجه ليس فقط عن طريق استهداف الأورام مباشرةً، بل أيضاً عبر هندسة النظم البيئية الميكروبية التي تعيش بداخلنا.
الاستشهاد: Alshareedah, I., Brunner, J.D., Chain, P.S.G. et al. Significance and challenges in dissecting cancer-bacteriome interactions. BJC Rep 4, 22 (2026). https://doi.org/10.1038/s44276-026-00229-7
الكلمات المفتاحية: ميكروبيوم السرطان, البكتريوم, البيئة الدقيقة للورم, الميكروفلويديات, العلاج الميكروبي