Clear Sky Science · ru
Значение и сложности в изучении взаимодействий между раком и бактериомом
Почему маленькие жильцы важны для рака
Каждый человек носит триллионы бактерий, которые тихо сосуществуют с нами, образуя богатые сообщества на коже, во рту, лёгких и особенно в кишечнике. В этой статье рассматривается провокационная идея: эти микробные соседи могут как способствовать развитию рака, так и, не менее важно, сдерживать его. Изучая, как целые бактериальные сообщества взаимодействуют с опухолями — и почему технически это так тяжело исследовать — авторы утверждают, что понимание этой скрытой экосистемы может открыть новые пути для раннего обнаружения и лечения рака.
Скрытый мир внутри нас
Человеческое тело является домом для огромного «бактериома», тысячи видов бактерий, чья суммарная численность клеток сопоставима с нашей собственной. Разные органы населены разными наборами бактерий, и эти наборы меняются со временем и от человека к человеку. Сейчас учёные знают, что некоторые виды бактерий способны толкать здоровые клетки к раку, повреждая ДНК, поддерживая длительное воспаление или блокируя встроенные тормоза роста. Другие, напротив, кажутся полезными: они мобилизуют иммунные клетки против опухолей или изменяют микроокружение опухоли так, что замедляют развитие рака. Тем не менее большинство наших обитателей никогда не проверяли на предмет их влияния на рак, оставляя обширный неизведанный ландшафт потенциальных помощников и злодеев.
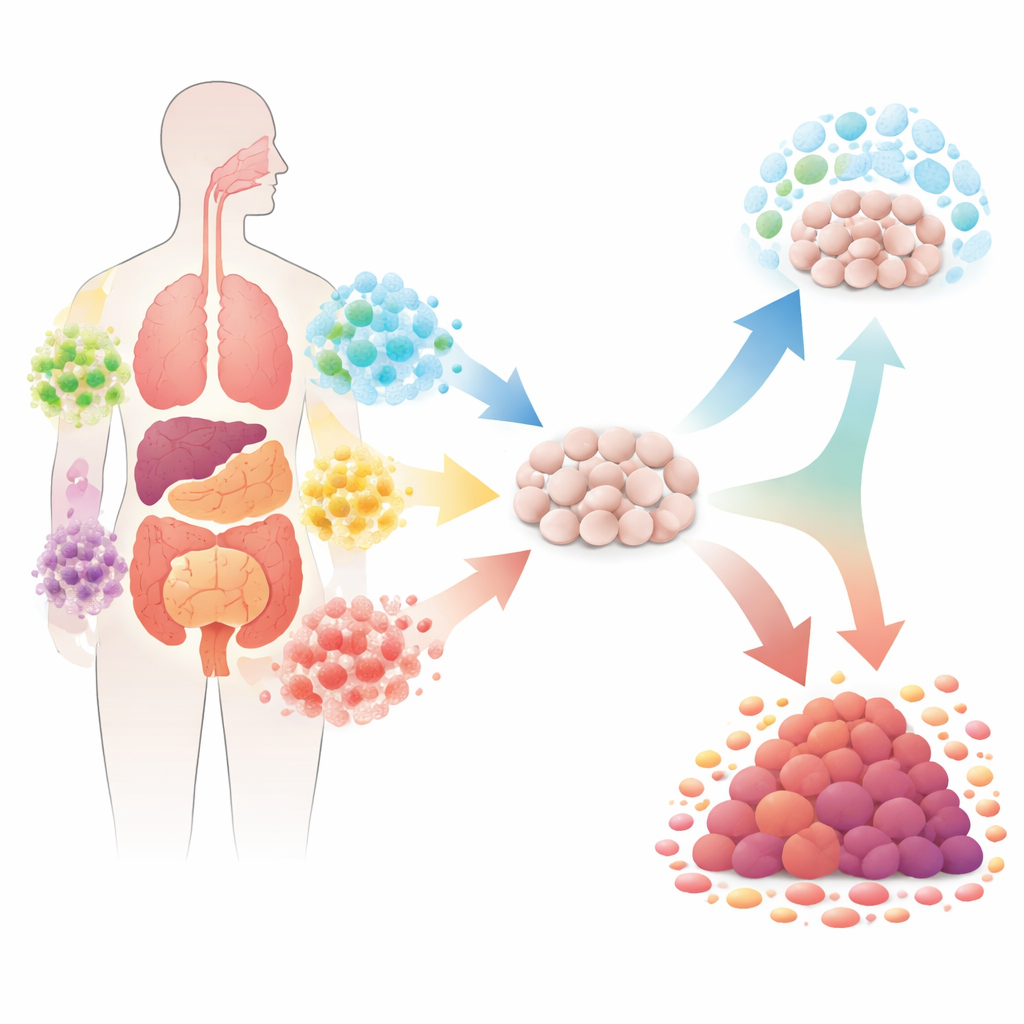
Как бактерии могут подтолкнуть клетки к опухолям
В статье рассматриваются несколько хорошо изученных примеров, показывающих, как бактерии могут инициировать или подпитывать опухоли. В желудке Helicobacter pylori вызывает приток иммунных клеток, которые выделяют реактивные молекулы, повреждающие ДНК и поддерживающие затяжное воспаление, способное привести к раку. Некоторые штаммы Escherichia coli синтезируют небольшое нестабильное соединение — колибактин — которое напрямую повреждает ДНК, повышая частоту мутаций в соседних клетках. В толстой кишке Fusobacterium nucleatum и Bacteroides fragilis могут нарушать ключевые сигнальные пути, контролирующие скорость деления клеток и их гибель. В совокупности эти примеры выявляют общую закономерность: бактерии могут формировать риск рака, многократно подвергая ткань стрессу для ДНК, иммунного баланса и механизмов роста в течение многих лет.
От корреляции к причинности
Многочисленные исследования до сих пор сравнивали микробиомы людей с раком и без него, используя секвенирование ДНК для каталогизации присутствующих бактерий. Эта работа связывает конкретные виды и более широкие бактериальные сообщества с раками кишечника, рта, лёгких, печени, кожи и других органов. Но такие снимки имеют ограничения. Они показывают ассоциацию, а не доказательство того, что микроорганизм вызывает болезнь. Они пропускают бактерии, опасные лишь в определённых сочетаниях, и испытывают трудности с выявлением микробов, которые тихо защищают от рака. Авторы описывают несколько концептуальных стратегий — от изучения по одному виду, до сравнения больших групп пациентов и отслеживания совместной эволюции раковых клеток и сложных бактериальных наборов — каждая из которых захватывает часть картины, но не позволяет полностью отобразить, как бактериом формирует опухоли.
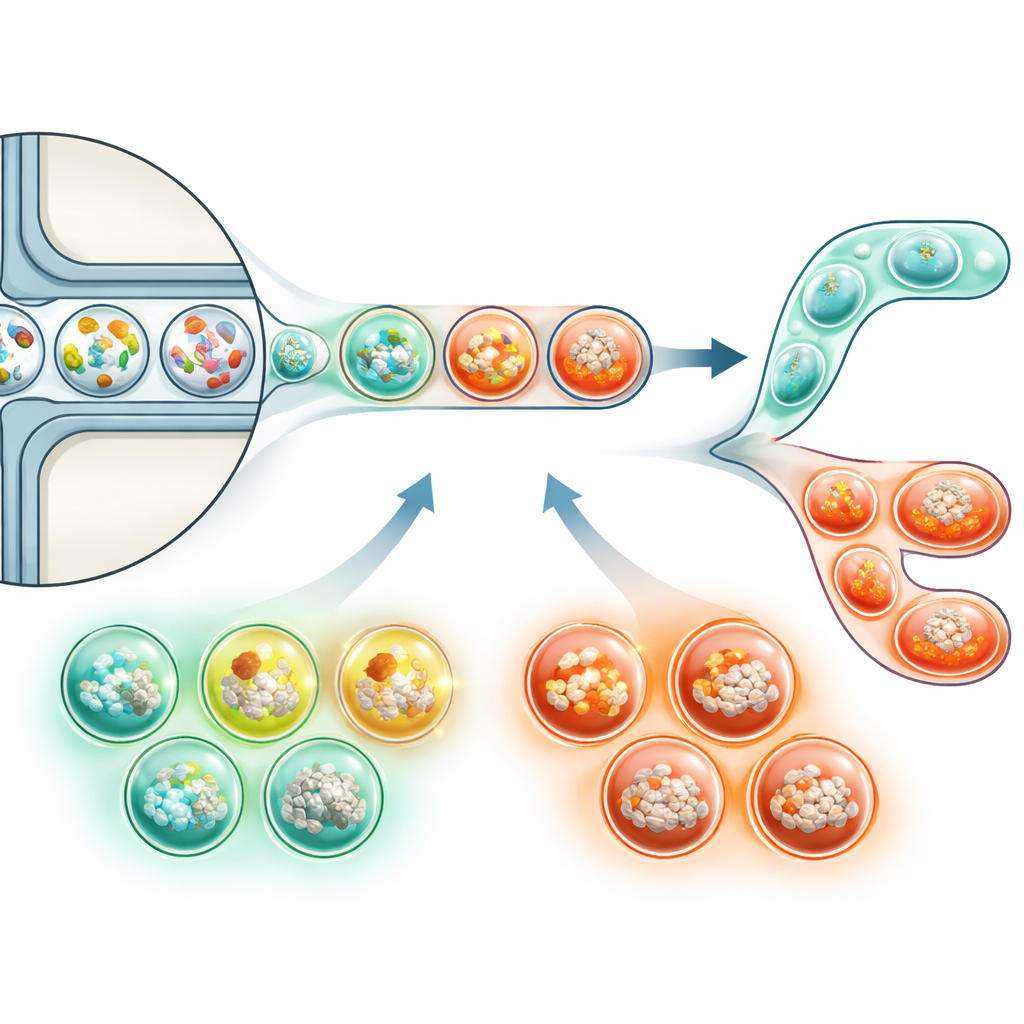
Уменьшая эксперименты по раку до крошечных капель
Чтобы преодолеть эти пробелы, статья выделяет микрофлюидные технологии, которые сокращают эксперименты до миллионов микроскопических капель. Каждая капля может выступать в роли крошечной пробирки, содержащей уникальную смесь бактерий и человеческих клеток. С помощью продуманных чип-дизайнов исследователи могут быстро генерировать, выращивать и сортировать эти капли на основе простых сигналов, таких как флюоресценция, отражающая рост раковых клеток. ДНК «штрих-коды» внутри капель позволяют затем секвенировать весь генетический материал массово и при этом отследить, какие бактерии и клетки пришли из какой капли. В сочетании с мощными методами секвенирования такой подход может наконец позволить учёным параллельно протестировать тысячи различных мини-бактериальных сообществ против раковых клеток, выявляя как стимулирующие, так и подавляющие рак комбинации.
Осмысление потока данных
Такие высокопроизводительные эксперименты порождают огромные, сложные наборы данных. Авторы описывают, как статистические инструменты, методы снижения размерности, сетевой анализ и современные методы искусственного интеллекта могут помочь просеять этот поток. Эти методы могут выявлять закономерности, например группы бактерий, которые часто встречаются вместе при агрессивных опухолях или в кажущихся защищёнными тканях, и предлагать проверяемые гипотезы о том, как разные микробы взаимодействуют друг с другом и с опухолями. Важно, что вычислительные модели, основанные на биологии, можно использовать для перевода этих паттернов в механистические идеи о причине и следствии, направляя следующий раунд экспериментов.
Преобразование микробной экологии в медицину
В конце концов авторы утверждают, что рак нельзя полностью понять, сосредотачиваясь только на человеческих генах и клетках. Наши обитатели образуют экологический фон, который может склонять чашу весов в сторону болезни или здоровья. Разрабатывая новые способы изучения целых бактериальных сообществ вместе с раковыми клетками — и сочетая эти эксперименты с продвинутыми инструментами анализа данных — исследователи надеются перейти от простого обнаружения опасных микробов к целенаправленному изменению бактериома. Долгосрочное видение смело: предотвращать или лечить рак не только посредством прямого удара по опухолям, но и за счёт инженерии микробных экосистем, которые живут внутри нас.
Цитирование: Alshareedah, I., Brunner, J.D., Chain, P.S.G. et al. Significance and challenges in dissecting cancer-bacteriome interactions. BJC Rep 4, 22 (2026). https://doi.org/10.1038/s44276-026-00229-7
Ключевые слова: микробиом рака, бактериом, микроокружение опухоли, микрофлюидика, микробная терапия