Clear Sky Science · tr
Kanser-bakteriyom etkileşimlerini çözmede önemi ve zorluklar
Neden Küçük Sakinler Kanser İçin Önemli?
Her insan vücudunda sessizce yaşayan trilyonlarca bakteri taşır; bu bakteriler cildimizde, ağızda, akciğerlerde ve özellikle bağırsaklarımızda zengin topluluklar oluşturur. Bu makale kışkırtıcı bir fikri inceliyor: bu mikrobiyal komşular kanserleri tetikleyebilir veya aynı derecede önemli bir şekilde onları geride tutmaya yardımcı olabilir. Bakteri topluluklarının tümüyle tümörlerle nasıl etkileştiğini ve bunu incelemenin neden teknik olarak bu kadar zor olduğunu ele alarak, yazarlar bu gizli ekosistemi anlamanın erken teşhis ve kanser tedavisi için yeni yollar açabileceğini savunuyor.
İçimizdeki Gizli Dünya
İnsan vücudu, toplam hücre sayısı bizimkine denk olabilecek binlerce bakteri türünden oluşan muazzam bir “bakteriyom”un evidir. Farklı organlar farklı bakteri karışımlarına ev sahipliği yapar ve bu karışımlar zaman içinde ve kişiler arasında değişir. Araştırmacılar artık bazı bakteri türlerinin DNA’ya zarar vererek, uzun süreli iltihabı körükleyerek veya kontrolsüz büyümeyi frenleyen mekanizmaları engelleyerek sağlıklı hücreleri kansera yönlendirebileceğini biliyor. Diğerleri ise bağışıklık hücrelerini tümörlere saldırmaya çağırarak veya tümör ortamını kanseri yavaşlatacak şekilde değiştirerek ters etki yapıyor gibi görünüyor. Yine de yerleşik bakterilerimizin çoğu kanser üzerindeki etkileri açısından hiç test edilmedi; bu da potansiyel yardımcılar ve düşmanlarla dolu geniş bir bilinmeyen manzara bırakıyor.
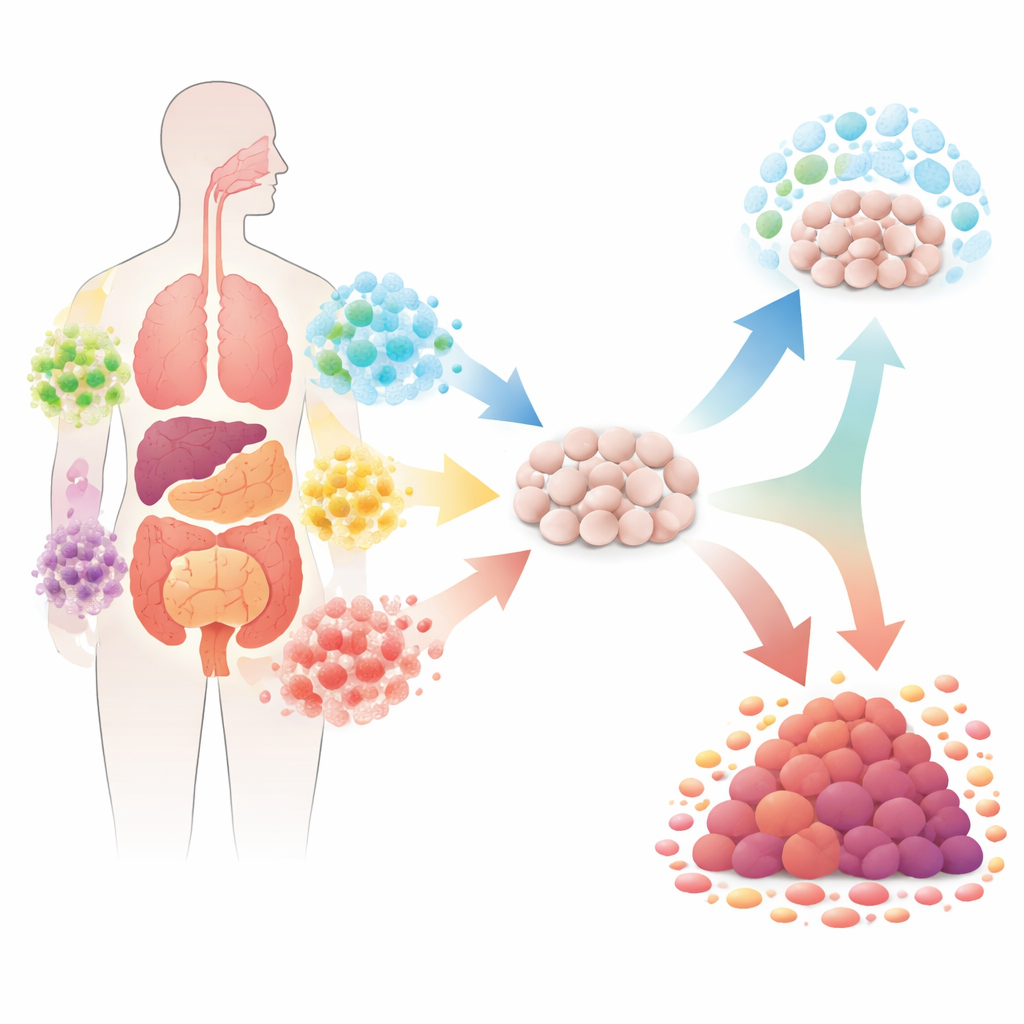
Bakterilerin Hücreleri Tümörlere Nasıl İtebildiği
Makale, bakterilerin tümörleri başlatmaya veya beslemeye nasıl yardımcı olabildiğini gösteren birkaç iyi çalışılmış örneği gözden geçiriyor. Mide ortamında Helicobacter pylori, reaktif moleküller salgılayan bağışıklık hücrelerinin dalgalarını tetikler; bu moleküller DNA’ya zarar vererek uzun süreli iltihabı ve zamanla kansere yol açabilecek süreçleri destekler. Bazı Escherichia coli suşları kolibaktin adı verilen küçük, kararsız bir kimyasal üretir; bu molekül doğrudan DNA’yı zedeler ve yakındaki hücrelerde mutasyon oranlarını artırır. Kalın bağırsakta Fusobacterium nucleatum ve Bacteroides fragilis, hücrelerin ne kadar hızlı bölündüğünü ve ne zaman öldüğünü kontrol eden ana sinyal yollarını bozabilir. Bu vakalar birlikte ortak bir deseni ortaya koyuyor: bakteriler, yıllar boyunca bir dokunun DNA’sına, bağışıklık dengesine ve büyüme kontrol mekanizmalarına tekrarlanan stres uygulayarak kanser riskini şekillendirebilir.
Korelasyondan Nedenselliğe
Şimdiye kadar birçok çalışma, kanserli ve kansersiz kişilerin mikrobiyomlarını karşılaştırdı ve hangi bakterilerin bulunduğunu kataloglamak için DNA dizileme kullandı. Bu çalışmalar, belirli türleri ve daha geniş bakteri topluluklarını bağırsak, ağız, akciğer, karaciğer, deri ve diğer organlardaki kanserlerle ilişkilendirdi. Ancak bu tür anlık görüntülerin sınırları var. Bunlar ilişkiyi gösterebilir, bir mikrobun hastalığa neden olduğunu ispatlayamaz. Belirli kombinasyonlarda tehlikeli olan bakterileri atlayabilirler ve sessizce kansere karşı koruyucu etki yapan mikropları tespit etmekte zorlanırlar. Yazarlar, tek bir türü ayrı ayrı incelemekten büyük hasta gruplarını karşılaştırmaya ve kanser hücreleri ile karmaşık bakteri karışımlarının ortak evrimini izlemeye kadar birkaç kavramsal stratejiyi özetliyor; her biri tablonun bir bölümünü yakalıyor ancak bakteriyomun tümörü nasıl şekillendirdiğini tam olarak haritalamıyor.
Kanser Deneylerini Minik Damlacıklara Küçültmek
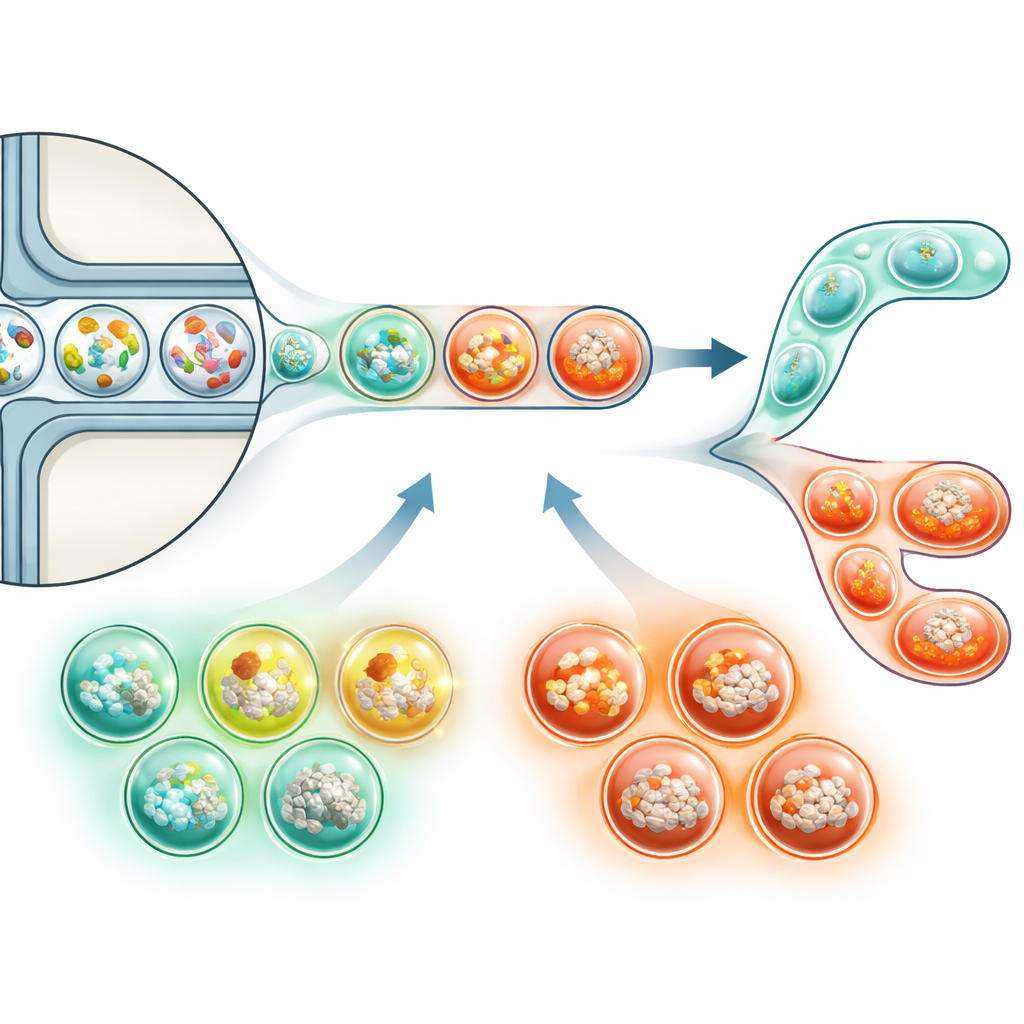
Bu boşlukları aşmak için makale, deneyleri milyonlarca mikroskobik damlacığa küçülten mikroakışkan teknolojilerini vurguluyor. Her damlacık benzersiz bir karışım bakteriye ve insan hücresine ev sahipliği yapan küçük bir test tüpü gibi davranabilir. Akıllı çip tasarımları kullanılarak, araştırmacılar bu damlacıkları hızlıca üretebilir, büyütebilir ve kanser hücresi büyümesini bildiren floresans gibi basit sinyallere göre ayırabilir. Damlacıkların içindeki DNA “barkodları”, daha sonra tüm genetik materyali topluca dizilemek mümkünken hangi bakterilerin ve hücrelerin hangi damlacıklardan geldiğini izlemeyi mümkün kılar. Güçlü dizileme yöntemleriyle birleştirildiğinde, bu yaklaşım sonunda bilim insanlarının binlerce farklı mini bakteri topluluğunu paralel olarak kanser hücrelerine karşı test etmesine, hem kanser-p�romot� hem de kanser-supress� kombinasyonları açığa çıkarmasına izin verebilir.
Veri Selini Anlamlandırmak
Böyle yüksek verimli deneyler muazzam ve karmaşık veri setleri üretir. Yazarlar, bu sele karşı istatistiksel araçların, boyut indirgeme tekniklerinin, ağ analizinin ve modern yapay zekânın nasıl yardımcı olabileceğini anlatıyor. Bu yöntemler, agresif kanserlerde veya görünüşte korunmuş dokularda birlikte ortaya çıkma eğiliminde olan bakteri grupları gibi desenleri öne çıkarabilir ve farklı mikropların birbirleriyle ve tümörlerle nasıl etkileştiğine dair test edilebilir hipotezler önerebilir. Önemli olarak, biyolojiye dayanan hesaplamalı modeller bu desenleri nedensel ve mekanistik fikirlere çevirmek için kullanılabilir ve sonraki deneyleri yönlendirebilir.
Mikrobiyal Ekolojiyi Tıbbın Hizmetine Çevirmek
Sonuç olarak, makale kanseri yalnızca insan genleri ve hücrelerine odaklanarak tam olarak anlayamayacağımızı savunuyor. Yerleşik bakterilerimiz, dengeyi hastalığa veya sağlığa kaydırabilecek ekolojik bir zemin oluşturur. Tüm bakteri topluluklarını kanser hücreleriyle birlikte incelemenin yeni yollarını geliştirerek — ve bu deneyleri gelişmiş veri analiz araçlarıyla eşleştirerek — araştırmacılar tehlikeli mikropları sadece tespit etmekten bakteriyomu kasıtlı olarak yeniden şekillendirmeye doğru ilerlemeyi umut ediyor. Uzun vadeli vizyon cesur: yalnızca tümörleri doğrudan hedefleyerek değil, içinde yaşadığımız mikrobiyal ekosistemleri mühendislik yoluyla değiştirerek kanseri önlemek veya tedavi etmek.
Atıf: Alshareedah, I., Brunner, J.D., Chain, P.S.G. et al. Significance and challenges in dissecting cancer-bacteriome interactions. BJC Rep 4, 22 (2026). https://doi.org/10.1038/s44276-026-00229-7
Anahtar kelimeler: kanser mikrobiyomu, bakteriyom, tümör mikroçevresi, mikroakışkanlar, mikrobiyal terapi