Clear Sky Science · it
Significato e sfide nello studio delle interazioni tra cancro e batterioma
Perché i piccoli inquilini contano nel cancro
Ogni persona ospita trilioni di batteri che condividono silenziosamente i nostri corpi, formando comunità ricche sulla pelle, nella bocca, nei polmoni e soprattutto nell’intestino. Questo articolo esplora un’idea provocatoria: che questi vicini microbici possano contribuire allo sviluppo dei tumori o, altrettanto importante, ostacolarli. Esaminando come intere comunità batteriche interagiscono con i tumori — e perché è così difficile studiarle dal punto di vista tecnico — gli autori sostengono che comprendere questo ecosistema nascosto potrebbe aprire nuove strade per la diagnosi precoce e il trattamento del cancro.
Il mondo nascosto dentro di noi
Il corpo umano ospita un vasto “batterioma”, migliaia di specie batteriche il cui numero complessivo di cellule è paragonabile al nostro. Organi diversi ospitano mix distinti di batteri, e questi mix cambiano nel tempo e da persona a persona. Oggi i ricercatori sanno che alcune specie batteriche possono spingere le cellule sane verso il cancro danneggiando il DNA, provocando infiammazione cronica o bloccando i freni intrinseci alla crescita incontrollata. Altre sembrano agire in senso opposto, richiamando cellule immunitarie a combattere i tumori o modificando il microambiente tumorale in modi che rallentano la malattia. Tuttavia la maggior parte dei batteri residenti non è mai stata testata per i loro effetti sul cancro, lasciando un vasto paesaggio di potenziali alleati e avversari ancora sconosciuto.
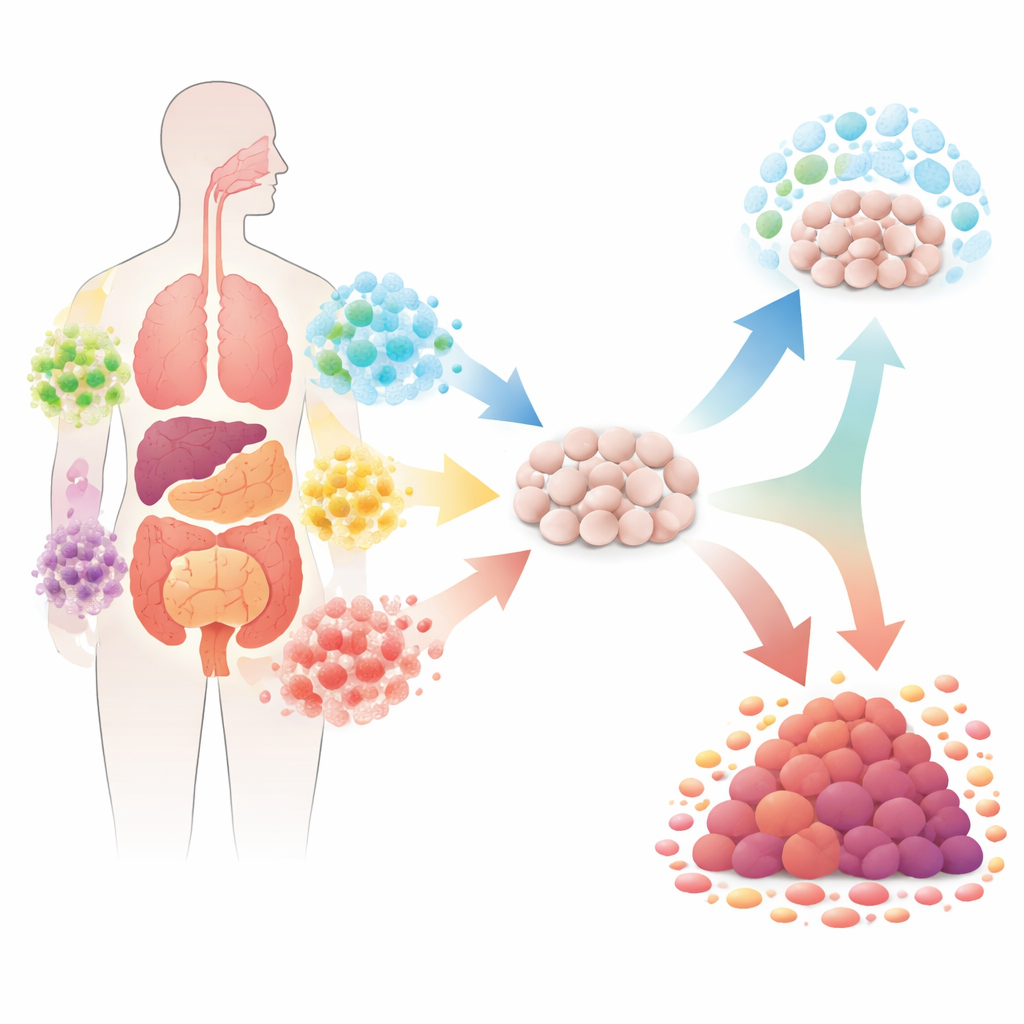
Come i batteri possono spingere le cellule verso i tumori
L’articolo passa in rassegna diversi esempi ben studiati che mostrano come i batteri possano innescare o alimentare i tumori. Nello stomaco, Helicobacter pylori induce ondate di cellule immunitarie che rilasciano molecole reattive, danneggiando il DNA e promuovendo un’infiammazione di lunga durata che può portare al cancro. Alcuni ceppi di Escherichia coli producono una piccola e instabile sostanza chimica chiamata colibactina che danneggia direttamente il DNA, aumentando i tassi di mutazione nelle cellule vicine. Nel colon, Fusobacterium nucleatum e Bacteroides fragilis possono entrambi alterare vie di segnalazione chiave che controllano la velocità di divisione cellulare e i processi di morte cellulare. Nel complesso, questi casi rivelano uno schema comune: i batteri possono modulare il rischio di cancro stressando ripetutamente il DNA del tessuto, l’equilibrio immunitario e i meccanismi di controllo della crescita nel corso di molti anni.
Dalla correlazione alla causa
Finora molti studi hanno confrontato i microbiomi di persone con e senza cancro, usando il sequenziamento del DNA per catalogare quali batteri sono presenti. Questo lavoro ha collegato specie specifiche e comunità batteriche più ampie a tumori dell’intestino, della bocca, dei polmoni, del fegato, della pelle e di altri organi. Ma questi istantanee hanno dei limiti. Possono mostrare associazioni, non la prova che un microbo causi la malattia. Non cogliere i batteri pericolosi solo in certe combinazioni e fatica a individuare i microbi che proteggono silenziosamente contro il cancro. Gli autori delineano diverse strategie concettuali — dallo studio di una singola specie alla volta, al confronto di grandi gruppi di pazienti, al monitoraggio dell’evoluzione congiunta delle cellule tumorali e di mix batterici complessi — che ciascuna cattura una parte del quadro ma non bastano a mappare pienamente come il batterioma influenzi i tumori.
Ridurre gli esperimenti sul cancro a minuscole goccioline
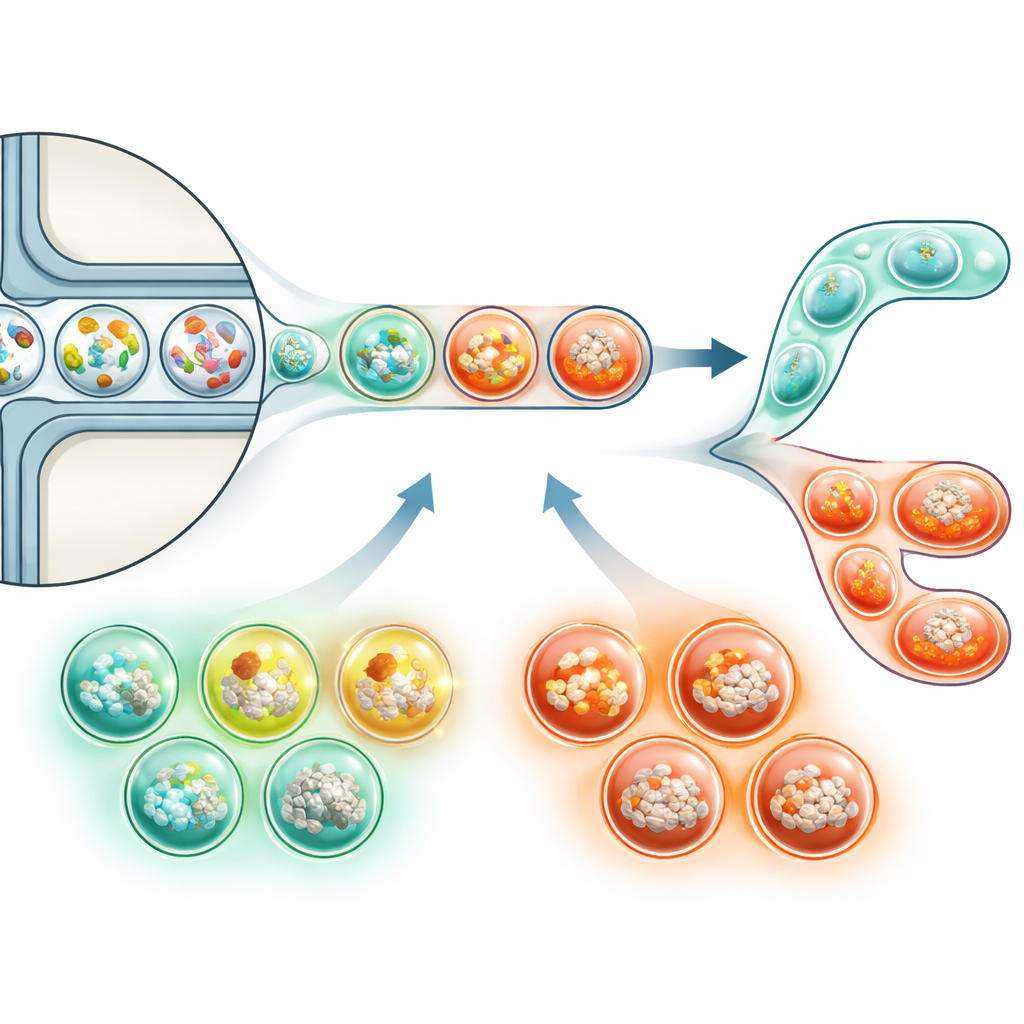
Per colmare queste lacune, l’articolo mette in luce le tecnologie microfluidiche che comprimono gli esperimenti in milioni di goccioline microscopiche. Ogni gocciolina può funzionare come una piccola provetta, contenente una miscela unica di batteri e cellule umane. Grazie a progetti intelligenti di chip, i ricercatori possono generare, coltivare e separare rapidamente queste goccioline basandosi su segnali semplici, come la fluorescenza che indica la crescita delle cellule tumorali. I “codici a barre” del DNA all’interno delle goccioline rendono possibile sequenziare in massa tutto il materiale genetico in seguito pur tracciando quali batteri e cellule provenivano da quale gocciolina. Abbinato a potenti metodi di sequenziamento, questo approccio potrebbe finalmente consentire di testare in parallelo migliaia di diverse mini-comunità batteriche contro cellule tumorali, rivelando combinazioni sia promotrici che soppressive del cancro.
Dare senso al diluvio di dati
Esperimenti ad alto rendimento di questo tipo generano set di dati enormi e complessi. Gli autori descrivono come strumenti statistici, tecniche di riduzione della dimensionalità, analisi di rete e l’intelligenza artificiale moderna possano aiutare a setacciare questo flusso. Questi metodi possono evidenziare schemi, come gruppi di batteri che tendono a comparire insieme in tumori aggressivi o in tessuti apparentemente protetti, e possono suggerire ipotesi verificabili su come diversi microbi interagiscono tra loro e con i tumori. È importante che modelli computazionali radicati nella biologia possano tradurre questi schemi in idee meccanicistiche su causa ed effetto, guidando il prossimo ciclo di esperimenti.
Trasformare l’ecologia microbica in medicina
In definitiva, l’articolo sostiene che il cancro non può essere compreso appieno concentrandosi solo sui geni e sulle cellule umane. I nostri batteri residenti costituiscono uno sfondo ecologico che può inclinare l’equilibrio verso malattia o salute. Sviluppando nuovi modi per studiare intere comunità batteriche insieme alle cellule tumorali — e abbinando questi esperimenti a strumenti avanzati di analisi dei dati — i ricercatori sperano di passare dal semplice riconoscere microbi pericolosi al rimodellare intenzionalmente il batterioma. La visione a lungo termine è ambiziosa: prevenire o trattare il cancro non solo mirando direttamente ai tumori, ma anche ingegnerizzando gli ecosistemi microbici che vivono dentro di noi.
Citazione: Alshareedah, I., Brunner, J.D., Chain, P.S.G. et al. Significance and challenges in dissecting cancer-bacteriome interactions. BJC Rep 4, 22 (2026). https://doi.org/10.1038/s44276-026-00229-7
Parole chiave: microbioma del cancro, batterioma, microambiente tumorale, microfluidica, terapia microbica