Clear Sky Science · zh
体外 γ-氨基丁酸 A (GABAA) 受体在 α+/γ2– 界面上对 53 种处方及设计类苯二氮卓类药物的激动与结合作用
这对日常生活的重要性
苯二氮卓类药物是治疗焦虑、失眠和癫痫等疾病中使用最广泛的药物之一,但许多也被用于娱乐或滥用,有时会造成致命后果。近年来,非法市场上出现了一波“设计型”衍生物,常以长得相似的药丸出售,几乎没有或根本没有医学检测。本研究提出了一个简单而紧迫的问题:这些新化合物对大脑主要抑制系统的作用有多强烈?化学结构上的细微调整如何改变它们的效应?
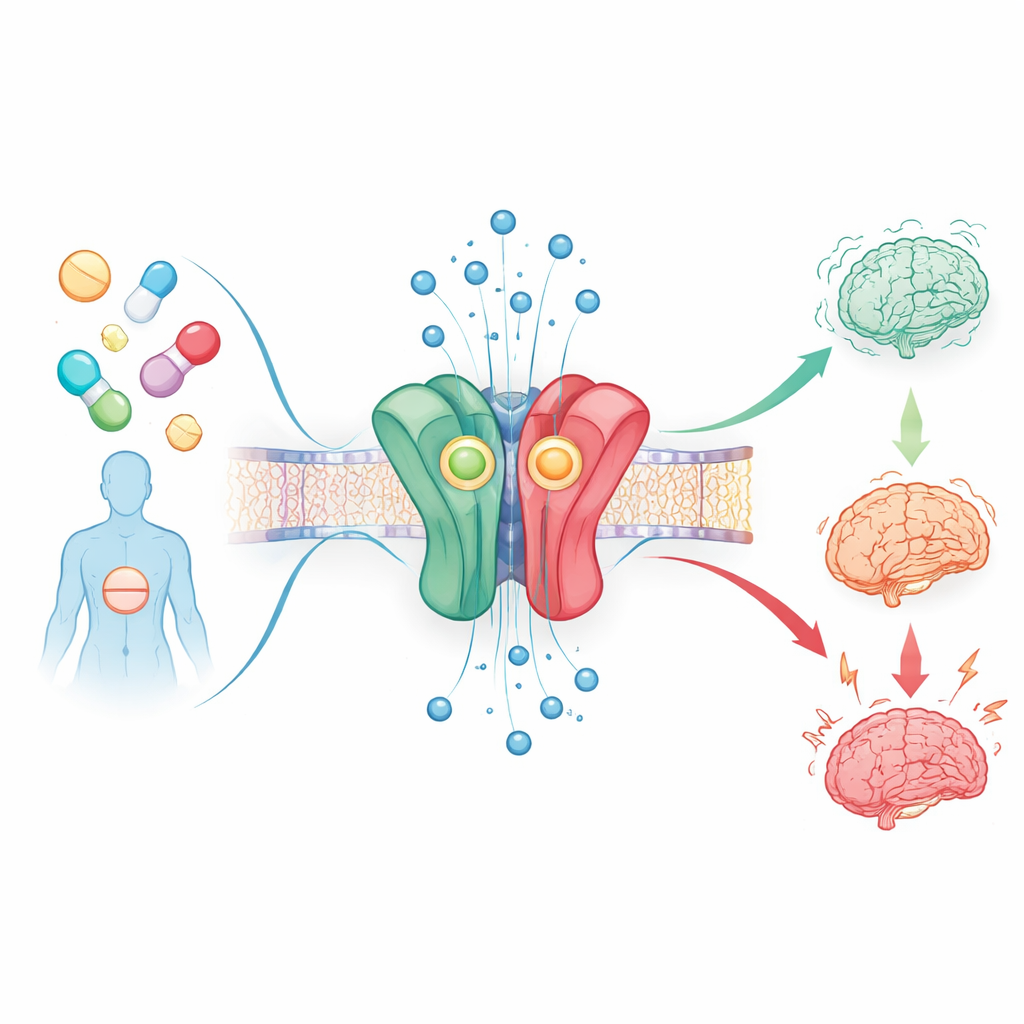
这些药物作用的大脑开关
本研究中的所有药物都作用于大脑的同一个关键靶点:GABAA 受体,一种允许氯离子流入神经细胞以抑制其活动的蛋白通道。常规苯二氮卓通过附着在该受体的特定接触点,使当天然信使 GABA 存在时通道更易开放,这就是它们减轻焦虑并促进睡眠的原因。研究人员使用一种复杂的细胞测定来测量 53 种处方和设计型苯二氮卓对该受体亚型(称为 α1β2γ2)的影响,通过追踪通道开放时产生的微小电流来进行评估。
强度和方向范围广泛
研究团队发现,大多数化合物在一定程度上增强受体活性,但方式并不相同。有些设计型药物的效力可达地西泮的大约 60 倍,意味着测试中只需极微量即可产生强烈效应。其他一些几乎没有任何作用。两种相关化合物则显著不同于大多数苯二氮卓:它们不是增强抑制性电流,而是削弱它们。这些“负调节剂”很重要,因为它们可能产生与用户期望的标准镇静剂截然不同的体验和风险。
细微的化学变化带来大的功能转变
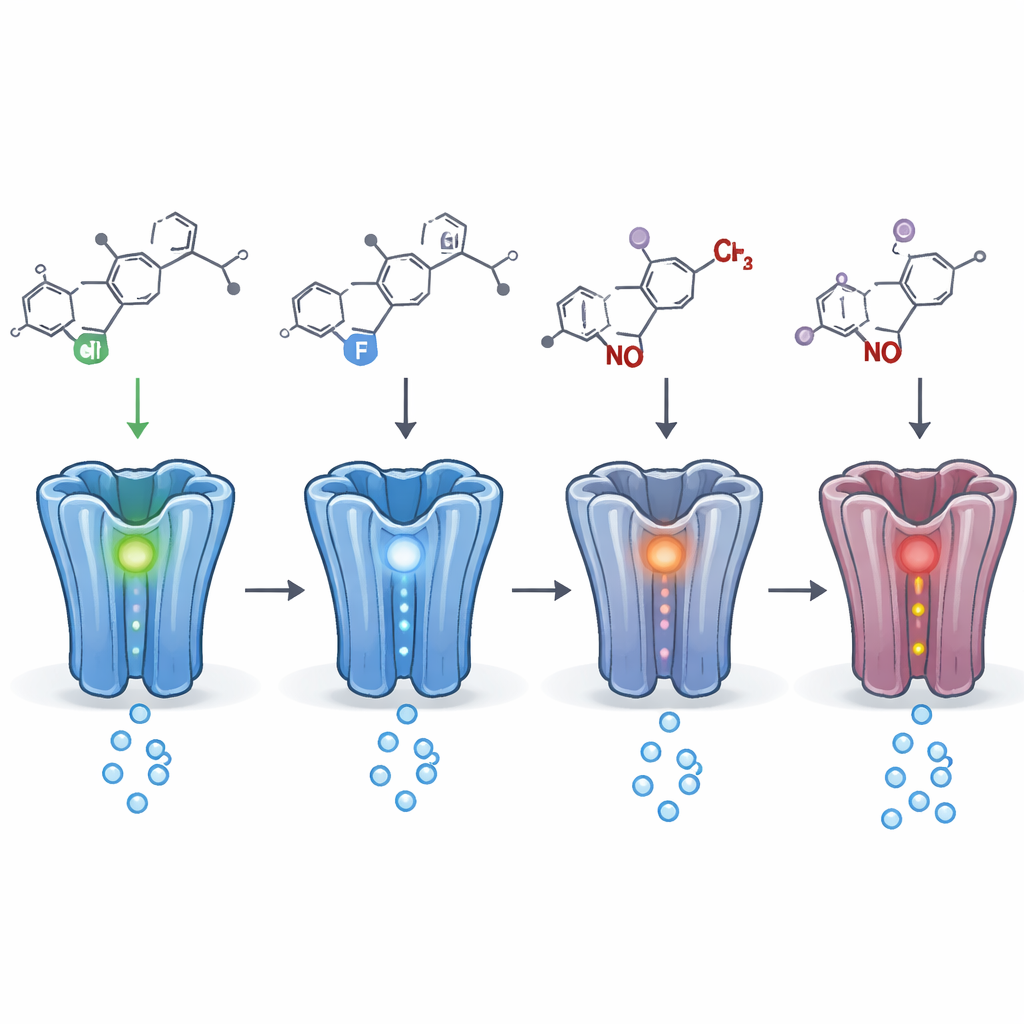
通过比较许多结构接近的化合物,作者能够绘制出哪些微小结构变化最为关键。在特定位置用一种卤素原子(如氯、氟或溴)替换另一种,经常改变药物在受体上的效力。在某些情况下,将单个卤素从附着环的一个位置移动到另一个位置,会将药物从增强镇静的作用翻转为抑制作用。在其他位置的变化,例如添加或去除小侧链或制成在体内被转化的“前药”版本,往往会降低或延迟活性,但很少会完全消除活性。代谢物——体内形成的分解产物——几乎总是保留在受体上的显著活性,有时其强度与母体药物相当或更强。
隐蔽的结合位点与混合信号
为弄清这些药物在受体上的作用位点,研究人员加入了氟马西尼,这是一种阻断经典苯二氮卓位点并用于逆转过量反应的药物。对于大多数化合物,氟马西尼抹除了它们的效应,证实其作用主要来自已知的位点。但有少数药物即使在氟马西尼存在时仍显示出一定的增强作用,暗示它们可能还与同一受体上的其他接触点相互作用。那些负调节剂以及一些乍看之下似乎无活性的化合物,在主要位点被阻断时仍继续降低受体活性,这表明它们的抑制效应必定通过受体表面的其他区域介导。
这对使用者、临床医生和政策制定者的意义
对普通人而言,核心信息是并非所有类苯二氮卓的药丸都相同,即便它们外观相似或名字相近。街头流通的设计型版本在强度上差异极大,并且可能通过大脑抑制开关的多个接触点发挥作用。有些远比常见药物更强,有些很弱,少数甚至产生相反效应。由于许多活性代谢物也有贡献,整体效应可能比预期更强且持续更久。这项工作提供了一张详细的地图,将微小化学修饰与关键大脑受体的功能结果联系起来,有助于毒理学家解释中毒事件、减害团体评估相对风险,以及监管机构在这些设计型药物广泛流行之前预判它们的潜在行为。
引用: Norman, C., Liin, S.I., Jauregi-Miguel, A. et al. In vitro γ-aminobutyric acid A (GABAA) receptor activity and binding interactions at the α+/γ2– interface of 53 prescription and designer benzodiazepines. Commun Chem 9, 155 (2026). https://doi.org/10.1038/s42004-026-02001-x
关键词: 设计类苯二氮卓类药物, GABAA 受体, 药物安全, 构效关系, 娱乐性镇静剂