Clear Sky Science · fr
Activité in vitro et interactions de liaison sur le récepteur γ-aminobutyrique A (GABAA) à l’interface α+/γ2– de 53 benzodiazépines sur ordonnance et de synthèse
Pourquoi cela compte pour la vie quotidienne
Les benzodiazépines figurent parmi les médicaments les plus prescrits pour l’anxiété, l’insomnie et les crises, mais beaucoup sont aussi consommés à des fins récréatives ou détournés de leur usage, parfois avec des conséquences mortelles. Ces dernières années, une vague de versions « de synthèse » est apparue sur le marché illicite, souvent vendue sous forme de comprimés ressemblants et peu ou pas testés médicalement. Cette étude pose une question simple mais urgente : dans quelle mesure ces nouveaux composés affectent-ils le principal système calmant du cerveau, et comment de petites modifications de leur structure chimique modifient-elles leurs effets ?
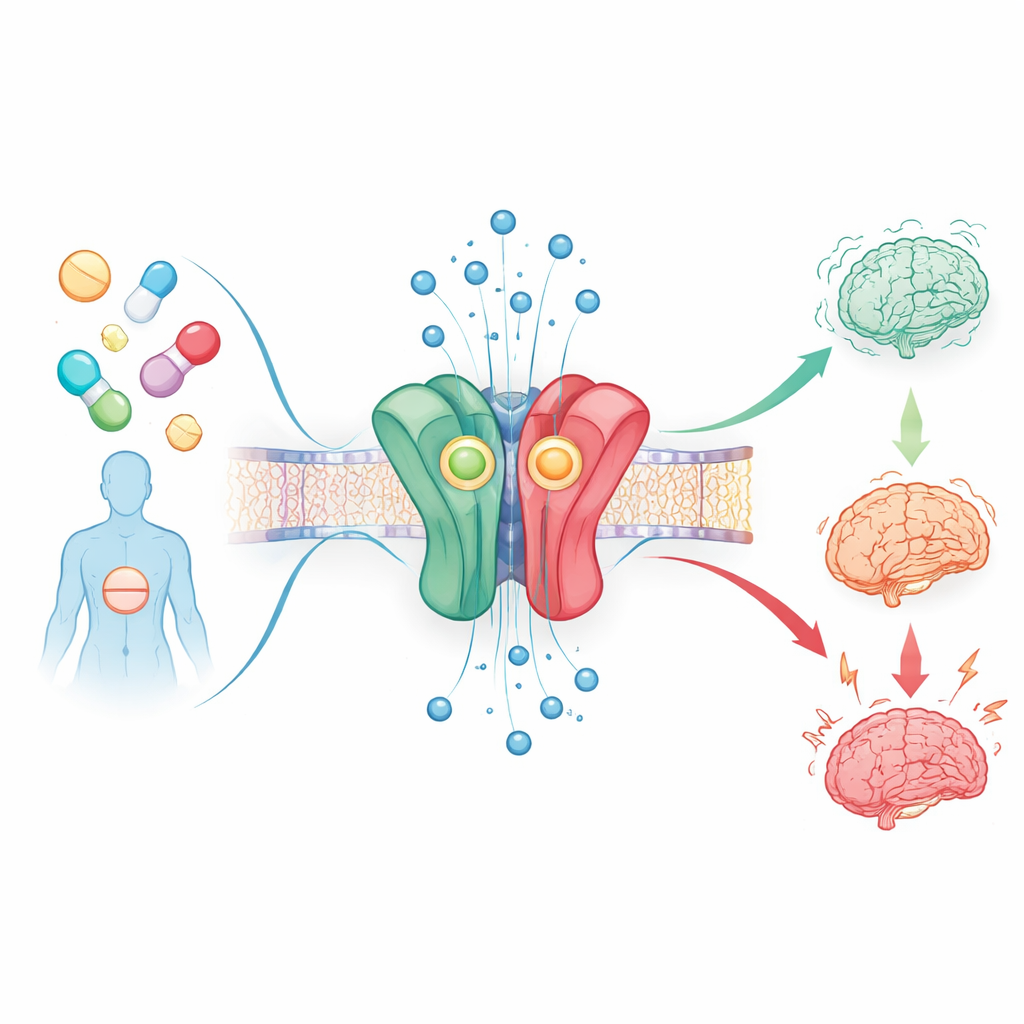
Le commutateur cérébral sur lequel agissent ces drogues
Tous les médicaments étudiés agissent sur la même cible clé du cerveau : le récepteur GABAA, un canal protéique qui laisse entrer des ions chlorure dans les cellules nerveuses et réduit leur activité. Les benzodiazépines classiques se lient à un point de contact particulier de ce récepteur et facilitent l’ouverture du canal lorsque le messager naturel GABA est présent, ce qui explique leur effet anxiolytique et sédatif. Les chercheurs ont utilisé un test cellulaire sophistiqué pour mesurer comment 53 benzodiazépines, prescrites ou de synthèse, influencent ce sous-type de récepteur, connu sous le nom α1β2γ2, en suivant les très faibles courants électriques qui circulent lors de l’ouverture du canal.
Une grande variété d’intensité et d’orientation
L’équipe a constaté que la plupart des composés augmentaient dans une certaine mesure l’activité du récepteur, mais pas tous de la même manière. Certaines drogues de synthèse se sont révélées jusqu’à environ 60 fois plus puissantes que le diazépam, ce qui signifie qu’une quantité infime suffit à produire un fort effet dans le test. D’autres n’ont presque eu aucun effet. Deux composés apparentés se sont distingués en faisant l’inverse de la plupart des benzodiazépines : au lieu d’amplifier le courant calmant, ils l’affaiblissaient. Ces « modulateurs négatifs » sont importants car ils peuvent entraîner des expériences et des risques très différents de ce à quoi les consommateurs s’attendent lorsqu’ils pensent prendre un sédatif classique.
De très petites modifications chimiques, de grands changements fonctionnels
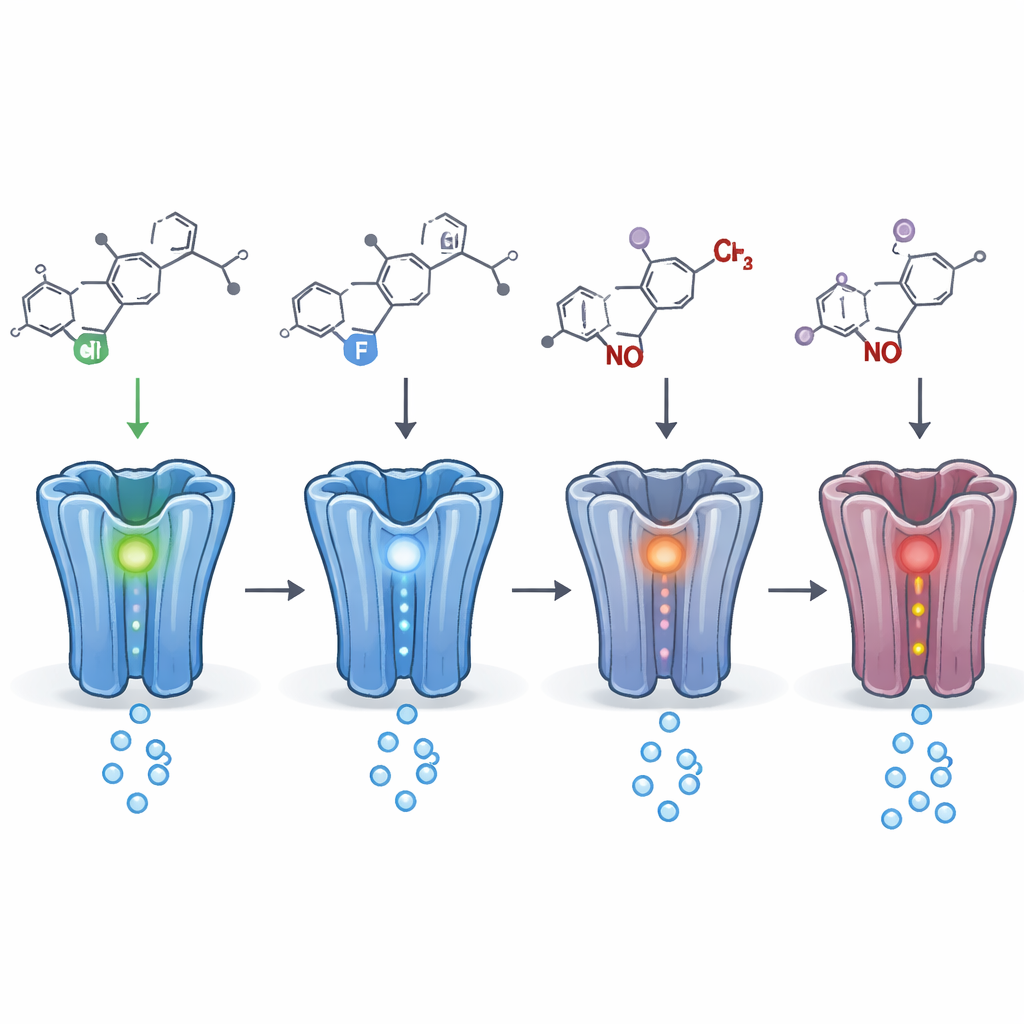
En comparant de nombreux proches cousins chimiques, les auteurs ont pu cartographier quelles petites modifications structurelles comptaient le plus. Remplacer un atome d’halogène (comme le chlore, le fluor ou le brome) par un autre à des positions spécifiques changeait souvent la puissance d’un médicament sur le récepteur. Dans certains cas, déplacer un seul halogène d’un emplacement d’un anneau substitué à un autre transformait un amplificateur calmant en inhibiteur. Des modifications à d’autres positions, comme l’ajout ou la suppression de petites chaînes latérales ou la création de versions « prémédicament » (prodrugs) converties dans l’organisme, avaient tendance à réduire ou retarder l’activité mais rarement à l’éliminer complètement. Les métabolites — les produits de dégradation formés dans le corps — conservaient presque toujours une activité significative sur le récepteur, et parfois étaient aussi puissants ou plus puissants que la molécule parente.
Sites de liaison cachés et signaux mixtes
Pour déterminer où sur le récepteur ces drogues agissaient, les chercheurs ont ajouté du flumazénil, un médicament qui bloque le site classique des benzodiazépines et est utilisé pour inverser les surdoses. Pour la majorité des composés, le flumazénil a éliminé leurs effets, confirmant que leur action provient principalement de ce site connu. Mais une poignée de drogues a continué de montrer un certain effet d’amplification même en présence de flumazénil, suggérant qu’elles peuvent aussi interagir avec d’autres points de contact sur le même récepteur. Les modulateurs négatifs, et quelques composés apparemment inactifs au premier abord, ont continué de réduire l’activité du récepteur même lorsque le site principal était bloqué, montrant que leurs effets inhibiteurs doivent être médiés ailleurs à la surface du récepteur.
Ce que cela signifie pour les usagers, les cliniciens et les décideurs
Pour le grand public, le message principal est que tous les comprimés de type benzodiazépine ne se valent pas, même s’ils se ressemblent ou portent un nom similaire. Les versions de synthèse qui circulent aujourd’hui couvrent une très large gamme de puissance et peuvent agir par plus d’un point de contact sur le « commutateur » calmant du cerveau. Certaines sont bien plus puissantes que les médicaments connus, d’autres sont faibles, et quelques-unes vont même dans la direction opposée. Parce que de nombreux métabolites actifs contribuent également, l’effet global peut être plus fort et durer plus longtemps que prévu. Ce travail fournit une carte détaillée reliant de petites modifications chimiques à des résultats fonctionnels sur un récepteur cérébral clé, aidant les toxicologues à interpréter les intoxications, les groupes de réduction des risques à conseiller sur les risques relatifs, et les autorités à anticiper le comportement de futures drogues de synthèse avant qu’elles ne se répandent.
Citation: Norman, C., Liin, S.I., Jauregi-Miguel, A. et al. In vitro γ-aminobutyric acid A (GABAA) receptor activity and binding interactions at the α+/γ2– interface of 53 prescription and designer benzodiazepines. Commun Chem 9, 155 (2026). https://doi.org/10.1038/s42004-026-02001-x
Mots-clés: benzodiazépines de synthèse, récepteur GABAA, sécurité médicamenteuse, relations structure-activité, sédatifs récréatifs