Clear Sky Science · de
In vitro γ-Aminobuttersäure-A (GABAA)-Rezeptoraktivität und Bindungsinteraktionen an der α+/γ2–Schnittstelle von 53 verschreibungspflichtigen und Designer-Benzodiazepinen
Warum das im Alltag wichtig ist
Benzodiazepine zählen zu den am häufigsten eingesetzten Arzneimitteln gegen Angst, Schlafstörungen und Krampfanfälle, werden aber auch häufig freizeitlich konsumiert oder missbraucht, mitunter mit tödlichen Folgen. In den letzten Jahren ist eine Welle von "Designer"‑Varianten auf dem Schwarzmarkt aufgetaucht, die oft als nachgeahmte Pillen verkauft werden und kaum oder gar nicht medizinisch geprüft sind. Diese Studie stellt eine einfache, aber dringliche Frage: Wie stark beeinflussen diese neuen Verbindungen das wichtigste beruhigende System des Gehirns, und wie verändern kleine Änderungen in ihrer chemischen Struktur ihre Wirkung?
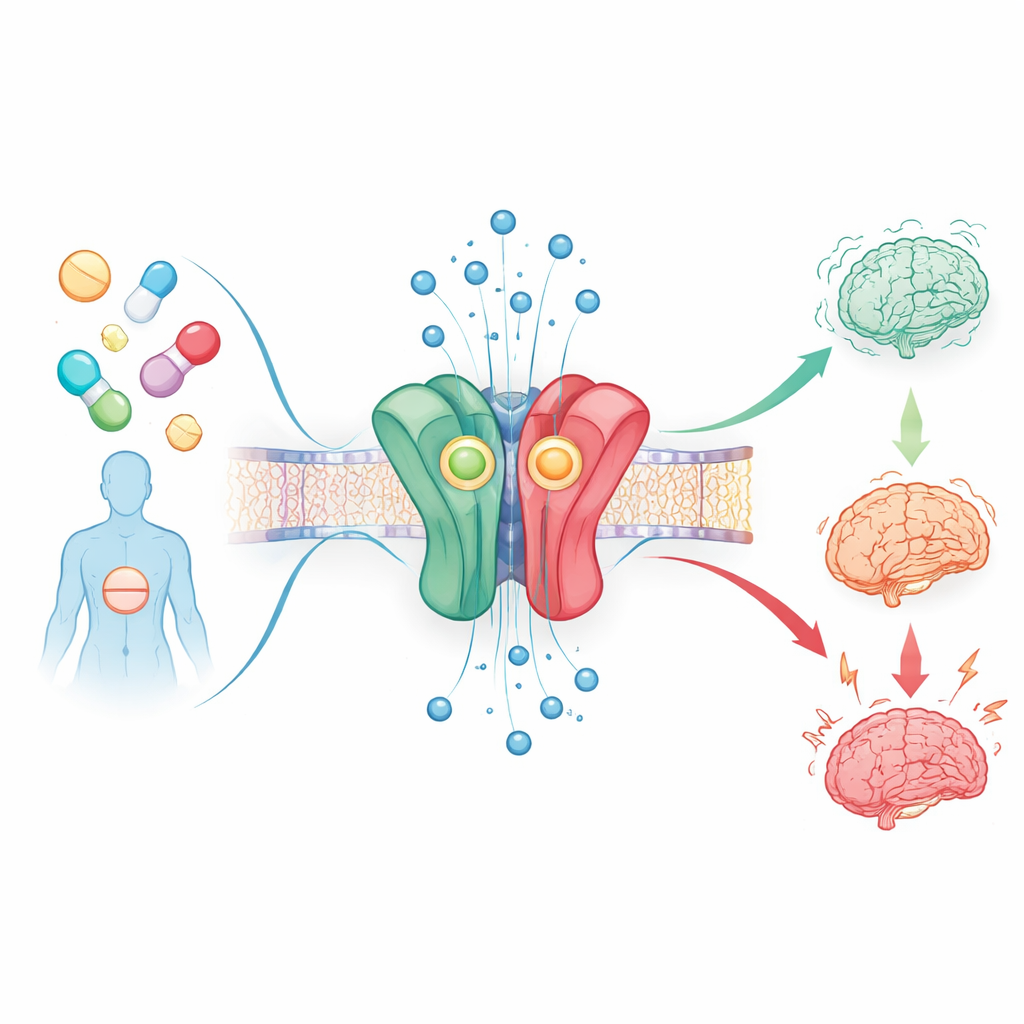
Der Schalter im Gehirn, auf den diese Wirkstoffe einwirken
Alle in dieser Studie untersuchten Wirkstoffe greifen an demselben zentralen Ziel im Gehirn an: dem GABAA‑Rezeptor, einem Proteinkanalsystem, das Chloridionen in Nervenzellen fließen lässt und deren Erregbarkeit dämpft. Übliche Benzodiazepine binden an einen bestimmten Kontaktpunkt dieses Rezeptors und erleichtern das Öffnen des Kanals, wenn der natürliche Botenstoff GABA vorhanden ist, weshalb sie Angst reduzieren und Schlaf fördern. Die Forscher nutzten einen ausgefeilten zellbasierten Test, um zu messen, wie 53 verschiedene verschreibungspflichtige und Designer‑Benzodiazepine diesen Rezeptorsubtyp, bekannt als α1β2γ2, beeinflussen, indem sie die winzigen elektrischen Ströme verfolgten, die beim Öffnen des Kanals fließen.
Große Bandbreite an Wirksamkeit und Richtung
Das Team stellte fest, dass die meisten Verbindungen die Rezeptoraktivität in gewissem Maße erhöhten, aber nicht alle auf dieselbe Weise. Einige Designer‑Drogen waren bis zu etwa 60‑mal wirksamer als Diazepam, was bedeutet, dass nur eine Spurmenge in dem Test eine starke Wirkung zeigte. Andere zeigten kaum eine Wirkung. Zwei verwandte Verbindungen fielen dadurch auf, dass sie das Gegenteil dessen bewirkten, was die meisten Benzodiazepine tun: Statt den beruhigenden Strom zu verstärken, schwächten sie ihn ab. Diese „negativen Modulatoren“ sind wichtig, weil sie sehr unterschiedliche Erlebnisse und Risiken hervorrufen können, als Nutzer erwarten, wenn sie glauben, ein übliches Sedativum einzunehmen.
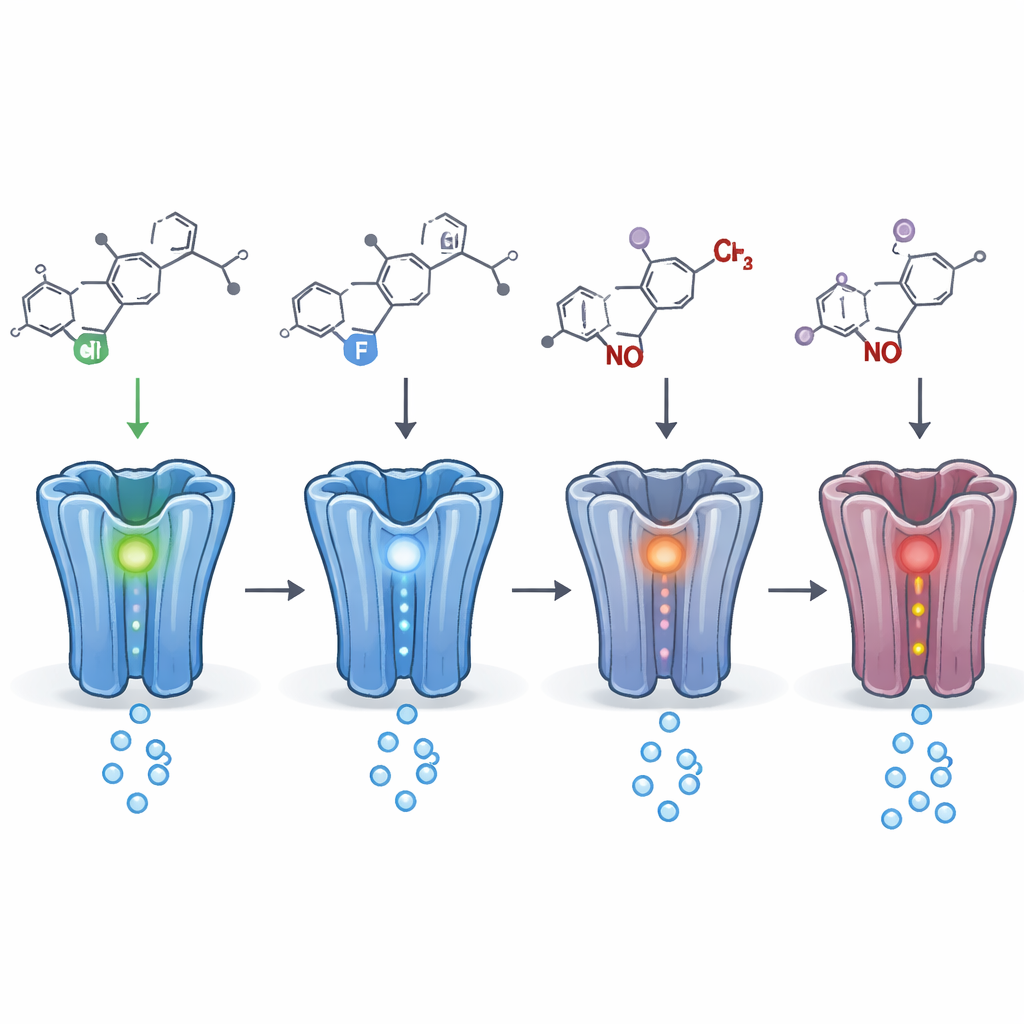
Kleine chemische Änderungen, große funktionelle Verschiebungen
Durch den Vergleich vieler enger chemischer Verwandter konnten die Autorinnen und Autoren abbilden, welche kleinen Strukturänderungen am bedeutsamsten sind. Der Austausch eines Halogenatoms (wie Chlor, Fluor oder Brom) durch ein anderes an bestimmten Positionen veränderte oft, wie stark ein Wirkstoff am Rezeptor wirkt. In einigen Fällen reichte das Verschieben eines einzelnen Halogens von einer Stelle an einem angehängten Ring zu einer anderen aus, um einen Wirkstoff von einem beruhigenden Verstärker in einen Hemmer zu verwandeln. Änderungen an anderen Positionen, etwa das Hinzufügen oder Entfernen kleiner Seitenketten oder das Herstellen von Prodrugs, die im Körper umgewandelt werden, führten tendenziell zu abgeschwächter oder verzögerter Aktivität, entfernten sie aber selten vollständig. Metaboliten — die im Körper gebildeten Abbauprodukte — behielten fast immer eine relevante Aktivität am Rezeptor und waren manchmal genauso stark oder stärker als das Ausgangsmedikament.
Versteckte Bindungsstellen und gemischte Signale
Um herauszufinden, wo am Rezeptor diese Substanzen wirkten, setzten die Forschenden Flumazenil zu, ein Medikament, das die klassische Benzodiazepin‑Stelle blockiert und zur Aufhebung von Überdosierungen verwendet wird. Bei der Mehrzahl der Verbindungen tilgte Flumazenil deren Wirkung vollständig, was bestätigte, dass ihre Wirkung überwiegend von dieser bekannten Stelle ausgeht. Eine Handvoll Drogen zeigte jedoch weiterhin eine teilweise verstärkende Wirkung, selbst in Anwesenheit von Flumazenil, was darauf hindeutet, dass sie möglicherweise auch mit anderen Kontaktpunkten desselben Rezeptors interagieren. Die negativen Modulatoren und einige Verbindungen, die auf den ersten Blick inaktiv schienen, verringerten die Rezeptoraktivität weiter, selbst wenn die Hauptstelle blockiert war, was zeigt, dass ihre hemmenden Effekte an anderen Stellen der Rezeptoroberfläche vermittelt werden müssen.
Was das für Nutzer, Kliniker und Politik bedeutet
Für Laien ist die Kernbotschaft: Nicht alle benzodiazepin‑ähnlichen Pillen sind gleich, auch wenn sie ähnlich aussehen oder denselben Namen tragen. Die derzeit auf der Straße kursierenden Designer‑Varianten decken ein enormes Spektrum an Potenz ab und können über mehr als einen Kontaktpunkt am beruhigenden Schalter des Gehirns wirken. Einige sind deutlich stärker als bekannte Arzneimittel, einige sind schwach, und einige wirken sogar in die entgegengesetzte Richtung. Da viele aktive Metaboliten ebenfalls beitragen, kann die Gesamtwirkung stärker und länger anhaltend sein als erwartet. Diese Arbeit liefert eine detaillierte Karte, die kleine chemische Änderungen mit funktionellen Ergebnissen an einem wichtigen Rezeptor des Gehirns verknüpft, und hilft Toxikologinnen und Toxikologen bei der Interpretation von Vergiftungen, Schadensminderungsgruppen bei der Beratung zu relativen Risiken und Regulierungsbehörden dabei, vorherzusehen, wie künftige Designer‑Drogen sich verhalten könnten, bevor sie weite Verbreitung finden.
Zitation: Norman, C., Liin, S.I., Jauregi-Miguel, A. et al. In vitro γ-aminobutyric acid A (GABAA) receptor activity and binding interactions at the α+/γ2– interface of 53 prescription and designer benzodiazepines. Commun Chem 9, 155 (2026). https://doi.org/10.1038/s42004-026-02001-x
Schlüsselwörter: Designer-Benzodiazepine, GABAA-Rezeptor, Arzneimittelsicherheit, Struktur‑Aktivitäts‑Beziehungen, rezeptfreie Sedativa