Clear Sky Science · ar
النشاط والارتباط لمستقبل γ-أمينوبيوتيريك من نوع A (GABAA) في المختبر عند واجهة α+/γ2– لِـ 53 بنزوديازيبينًا موصوفًا ومصممًا
لماذا يهم هذا في الحياة اليومية
تُعدُّ البنزوديازيبينات من أكثر الأدوية استخدامًا للقلق والأرق والنوبات، لكن العديد منها يُؤخذ الترفيه أو يُساء استخدامه، وأحيانًا بعواقب مميتة. في السنوات الأخيرة، ظهرت موجة من النسخ «المصممة» في السوق غير المشروع، غالبًا ما تُباع كأقراص متشابهة الشكل مع اختبارات طبية قليلة أو منعدمة. يطرح هذا البحث سؤالًا بسيطًا لكنه ملحًا: ما مدى تأثير هذه المركبات الجديدة على نظام التهدئة الرئيسي في الدماغ، وكيف تغيّر التعديلات الصغيرة في بنيتها الكيميائية آثارها؟
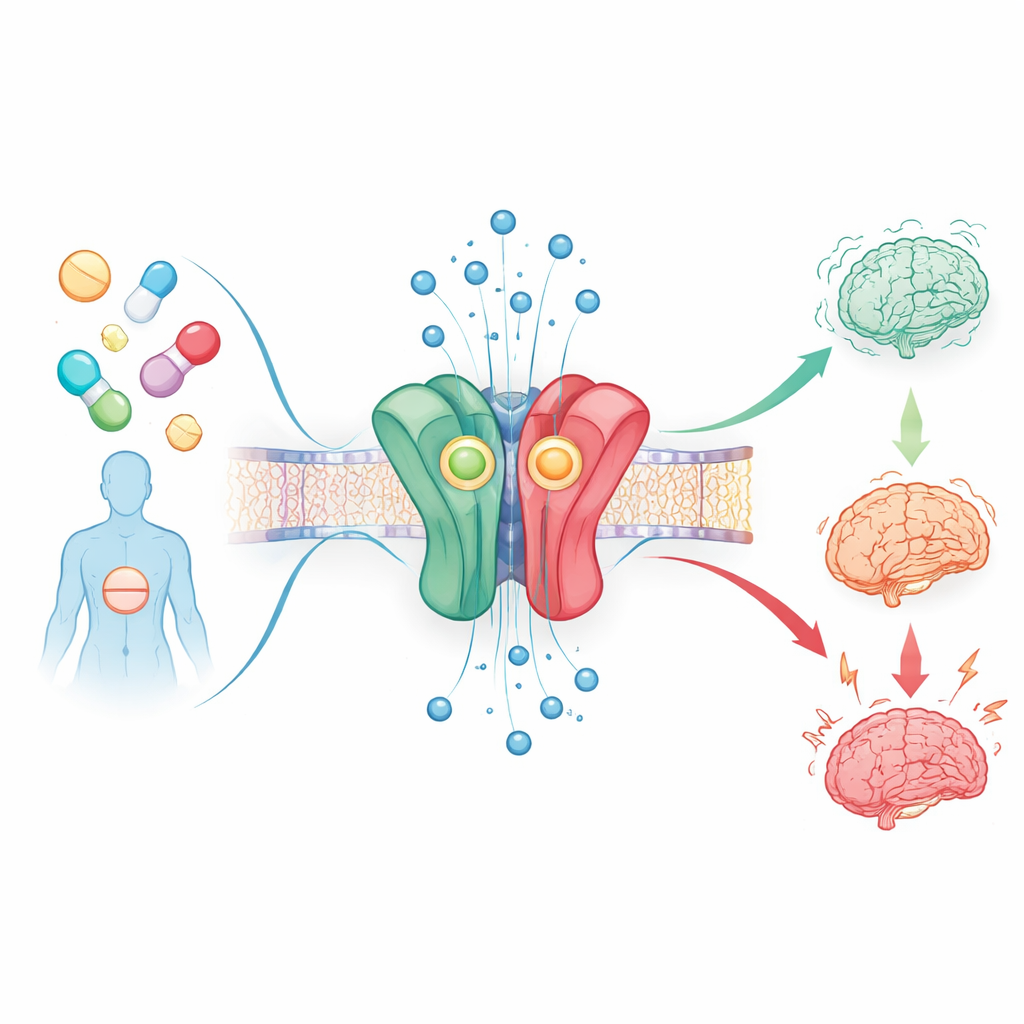
المفتاح العصبي الذي تعمل عليه هذه الأدوية
تعمل جميع الأدوية في هذه الدراسة على نفس الهدف الأساسي في الدماغ: مستقبل GABAA، وهو قناة بروتينية تسمح لأيونات الكلوريد بالدخول إلى الخلايا العصبية وتُخَمِّد نشاطها. تَلتصق البنزديازيبينات العادية بنقطة تلامس معينة على هذا المستقبل وتجعل القناة تفتح بسهولة أكبر عندما يكون الناقل الطبيعي GABA حاضرًا، ولذلك تُقلِّل القلق وتُساعد على النوم. استخدم الباحثون اختبارًا متقدّمًا قائمًا على الخلايا لقياس كيف يؤثر 53 بنزوديازيبينًا موصوفًا ومصممًا على هذا النوع من المستقبل، المعروف باسم α1β2γ2، عن طريق تتبُّع التيارات الكهربائية الضئيلة التي تتدفق عند فتح القناة.
نطاق واسع من القوة والاتجاه
وجد الفريق أن معظم المركبات عززت نشاط المستقبل إلى حد ما، لكن ليس كلها بنفس الطريقة. كانت بعض الأدوية المصممة أقوى بما يصل إلى نحو 60 ضعفًا من الديازيبام، ما يعني أن كمية ضئيلة فقط كانت كافية لإحداث تأثير قوي في الاختبار. وبعضها بالكاد أظهر أي تأثير. برز مركبان مرتبطان لفعلهما عكس ما تفعله معظم البنزوديازيبينات: فبدلًا من تعزيز التيار المهدئ، قلّلا منه. تُعتبر هذه «المنظمّات السالبة» مهمة لأنها قد تُنتج تجارب ومخاطر مختلفة تمامًا عما يتوقعه المستخدمون عند اعتقادهم أنهم يتناولون مهدئًا عاديًا.
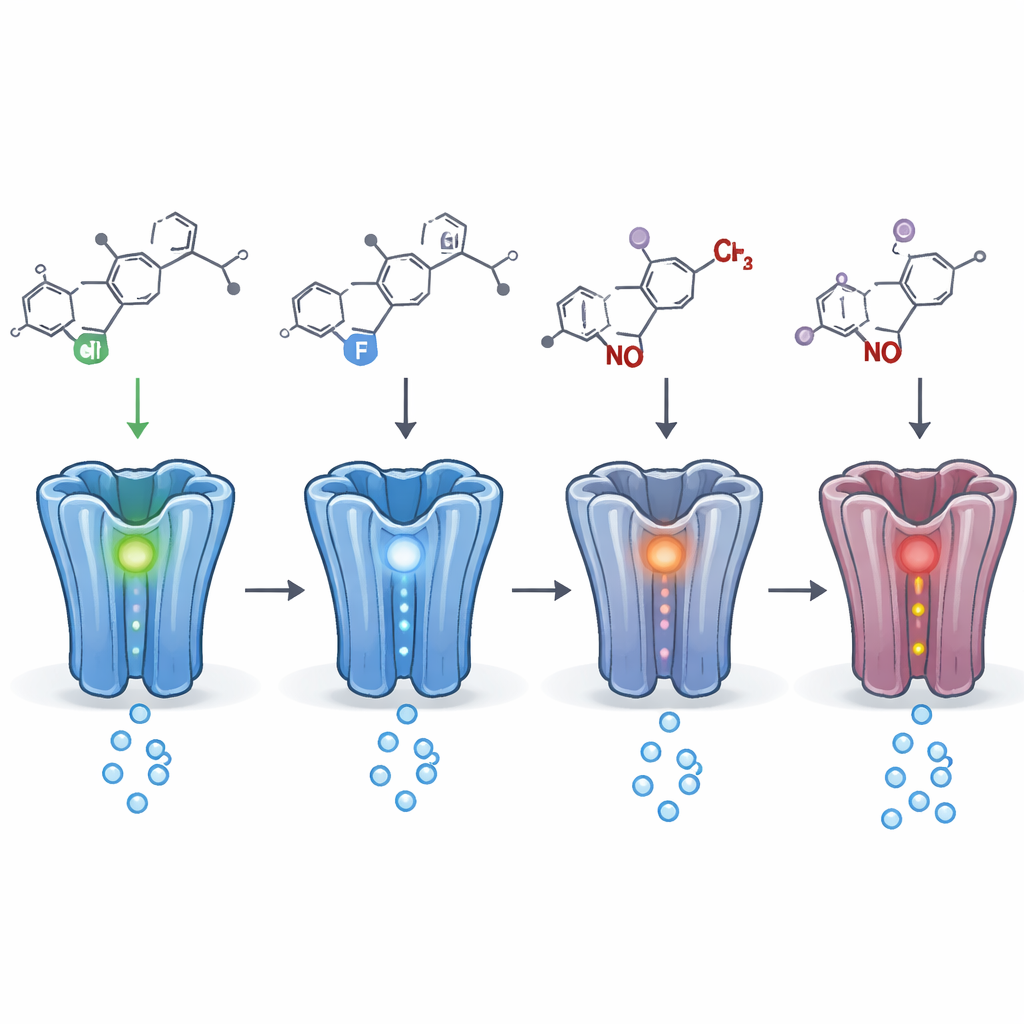
تغييرات كيميائية طفيفة، تحوّلات وظيفية كبيرة
بمقارنة العديد من الأقارب الكيميائيين المتقاربين، تمكن المؤلفون من رسم خريطة للتغييرات البنائية الصغيرة ذات الأثر الأكبر. غالبًا ما تغيّر استبدال ذرة هالوجين واحدة (مثل الكلور أو الفلور أو البروم) بأخرى في مواقع محددة مدى قوة الدواء على المستقبل. في بعض الحالات، أدى تحريك هالوجين واحد من موضع إلى آخر على حلقة ملحقة إلى قلب تأثير الدواء من مُعزّز مهدئ إلى مثبّت. أما التغييرات في مواقع أخرى، مثل إضافة أو إزالة سلاسل جانبية صغيرة أو صنع نسخ «برودواغ» تتحول داخل الجسم، فكانت تميل إلى تقليل أو تأخير النشاط لكنها نادرًا ما تزيله تمامًا. وكادت المستقلبات — نواتج التحلل المتشكلة في الجسم — أن تحتفظ دومًا بنشاط ذي معنى عند المستقبل، وفي أحيانٍ كانت بقوة مساوية أو أقوى من الدواء الأم.
مواقع ارتباط مخفية وإشارات مختلطة
لاكتشاف أين على المستقبل تعمل هذه الأدوية، أضاف الباحثون الفلومازينيل، وهو دواء يمنع موقع البنزوديازيبين الكلاسيكي ويُستخدم لعكس حالات الجرعة الزائدة. بالنسبة لغالبية المركبات، ألغى الفلومازينيل تأثيراتها، مما أكد أن عملها يأتي أساسًا من هذا الموقع المعروف. لكن عددًا قليلاً من الأدوية أظهر بعض التأثير المعزّز حتى بوجود الفلومازينيل، مما يوحي بأنها قد تتفاعل أيضًا مع نقاط تلامس أخرى على نفس المستقبل. استمرت المنظّمات السالبة، وبعض المركبات التي بدت خاملة للوهلة الأولى، في تقليل نشاط المستقبل حتى عند حجب الموقع الرئيسي، مما يدل على أن تأثيراتها المثبطة يجب أن تكون متوسّطة في أماكن أخرى على سطح المستقبل.
ما يعنيه هذا للمستخدمين والأطباء وصانعي السياسات
بالنسبة للشخص العادي، الرسالة الأساسية هي أن ليس كل قرص شبيه بالبنزوديازيبين متشابهًا، حتى لو بدا متشابهًا أو يحمل اسمًا مألوفًا. النسخ المصممة المتداولة حاليًا في الشوارع تغطي نطاقًا هائلًا من القوة ويمكن أن تعمل عبر أكثر من نقطة تلامس واحدة على مفتاح التهدئة في الدماغ. بعضها أقوى بكثير من الأدوية المعروفة، وبعضها ضعيف، وقليل منها يدفع في الاتجاه المعاكس. وبما أن العديد من المستقلبات النشطة تسهم أيضًا، قد يكون التأثير الكلي أقوى وأطول أمدًا مما يُتوقع. توفر هذه الدراسة خريطة مفصلة تربط التعديلات الكيميائية الصغيرة بالنتائج الوظيفية عند مستقبل دماغي رئيسي، مما يساعد السُمِّيَّين على تفسير حالات التسمم، ومجموعات الحد من الضرر على تقديم نصائح حول المخاطر النسبية، والمنظمين على توقع كيف قد تتصرف الأدوية المصممة المستقبلية قبل أن تنتشر على نطاق واسع.
الاستشهاد: Norman, C., Liin, S.I., Jauregi-Miguel, A. et al. In vitro γ-aminobutyric acid A (GABAA) receptor activity and binding interactions at the α+/γ2– interface of 53 prescription and designer benzodiazepines. Commun Chem 9, 155 (2026). https://doi.org/10.1038/s42004-026-02001-x
الكلمات المفتاحية: بنزوديازيبينات مصممة, مستقبل GABAA, سلامة الأدوية, علاقات البنية والنشاط, مهدئات ترفيهية