Clear Sky Science · es
Actividad in vitro del receptor γ-aminobutírico A (GABAA) e interacciones de unión en la interfaz α+/γ2– de 53 benzodiazepinas de prescripción y de diseño
Por qué esto importa en la vida cotidiana
Las benzodiazepinas están entre los medicamentos más usados para la ansiedad, el insomnio y las convulsiones, pero muchos también se consumen de forma recreativa o se usan de manera indebida, a veces con consecuencias mortales. En los últimos años ha surgido en el mercado ilícito una oleada de versiones “de diseño”, con frecuencia vendidas como píldoras similares a las habituales y con escasas o nulas pruebas médicas. Este estudio plantea una pregunta simple pero urgente: ¿con qué intensidad afectan estas nuevas sustancias al principal sistema calmante del cerebro, y cómo modifican sus efectos pequeños cambios en su estructura química?
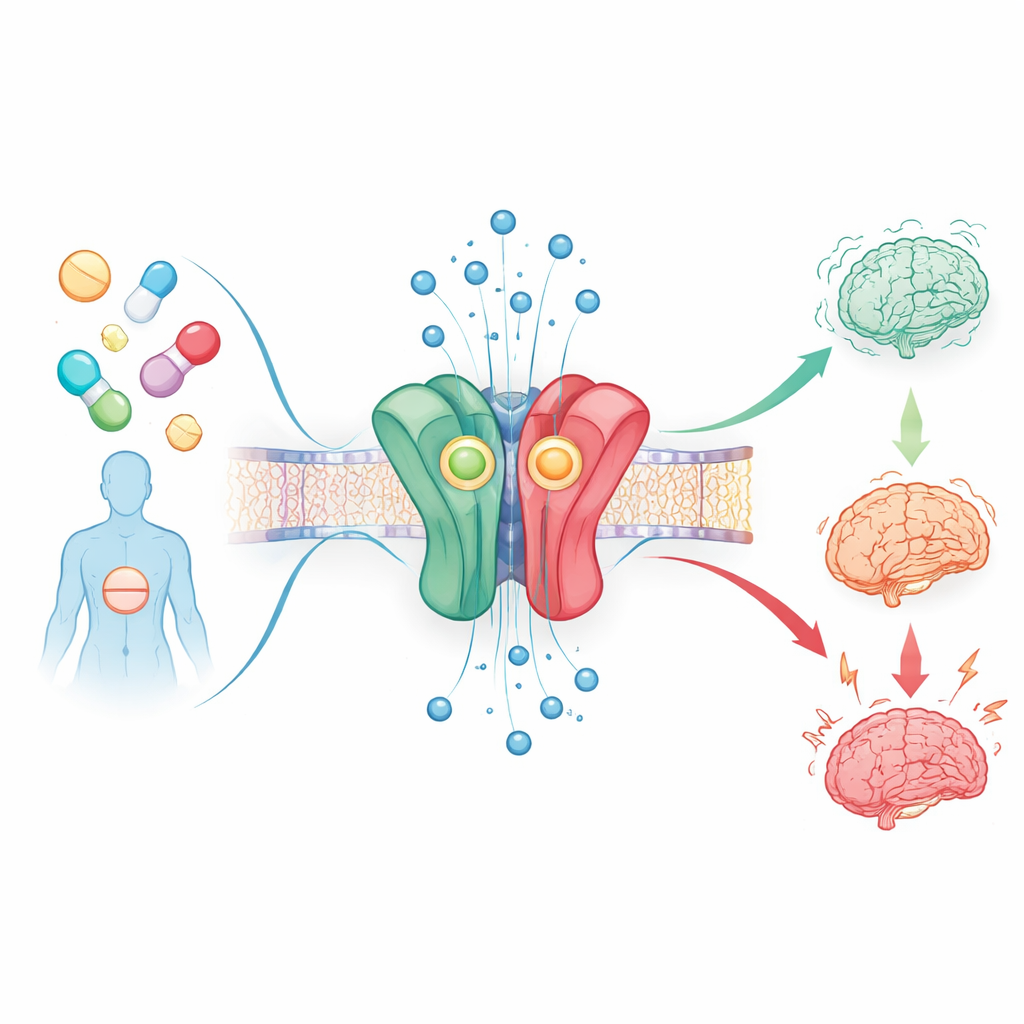
El interruptor cerebral sobre el que actúan estos fármacos
Todos los fármacos de este estudio actúan sobre el mismo objetivo clave en el cerebro: el receptor GABAA, un canal proteico que permite la entrada de iones cloruro en las neuronas y atenúa su actividad. Las benzodiazepinas comunes se unen a un punto de contacto particular en este receptor y facilitan que el canal se abra cuando está presente el mensajero natural GABA, por lo que reducen la ansiedad y favorecen el sueño. Los investigadores usaron una prueba celular sofisticada para medir cómo 53 benzodiazepinas, tanto de prescripción como de diseño, influyen en este subtipo de receptor, conocido como α1β2γ2, registrando las pequeñas corrientes eléctricas que fluyen cuando se abre el canal.
Una amplia gama de intensidad y dirección
El equipo encontró que la mayoría de los compuestos potenciaban la actividad del receptor en cierto grado, pero no todos del mismo modo. Algunos fármacos de diseño resultaron hasta unas 60 veces más potentes que el diazepam, lo que significa que bastaba una cantidad muy pequeña para producir un efecto fuerte en la prueba. Otros apenas mostraron actividad. Dos compuestos relacionados destacaron por hacer lo contrario de lo que hacen la mayoría de las benzodiazepinas: en lugar de aumentar la corriente calmante, la disminuían. Estos “moduladores negativos” son importantes porque podrían generar experiencias y riesgos muy distintos de los que esperan los usuarios cuando creen estar tomando un sedante estándar.
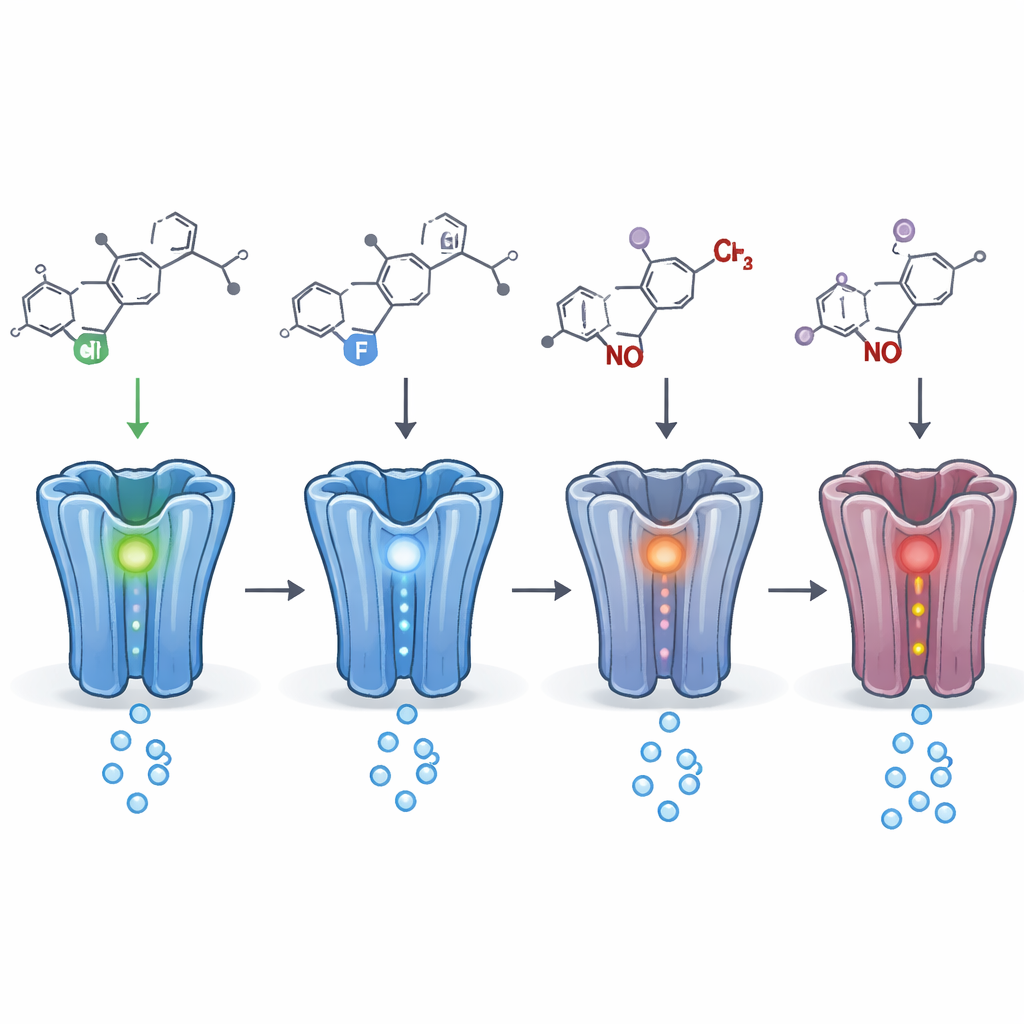
Pequeños cambios químicos, grandes variaciones funcionales
Al comparar muchos parientes químicos cercanos, los autores pudieron trazar qué cambios estructurales pequeños importaban más. Sustituir un halógeno (como cloro, flúor o bromo) por otro en posiciones específicas a menudo modificaba la potencia de un fármaco sobre el receptor. En algunos casos, mover un único halógeno de un lugar a otro en un anillo unido convertía un potenciador calmante en un inhibidor. Cambios en otras posiciones, como añadir o quitar pequeñas cadenas laterales o crear versiones “profármaco” que se convierten en el organismo, tendían a reducir o retrasar la actividad pero rara vez la eliminaban por completo. Los metabolitos—los productos de degradación formados en el cuerpo—casi siempre conservaban actividad relevante en el receptor y, a veces, eran tan potentes o más que el fármaco original.
Sitios de unión ocultos y señales mixtas
Para averiguar dónde en el receptor actuaban estos fármacos, los investigadores añadieron flumazenil, un medicamento que bloquea el sitio clásico de las benzodiazepinas y se usa para revertir sobredosis. Para la mayoría de los compuestos, el flumazenil anuló sus efectos, confirmando que su acción procede principalmente de este sitio conocido. Pero un puñado de fármacos siguió mostrando algún efecto potenciador incluso en presencia de flumazenil, lo que sugiere que también pueden interactuar con otros puntos de contacto en el mismo receptor. Los moduladores negativos, y algunos compuestos que a primera vista parecían inactivos, continuaron reduciendo la actividad del receptor incluso cuando el sitio principal estaba bloqueado, lo que demuestra que sus efectos inhibitorios deben mediarse en otras regiones de la superficie del receptor.
Qué significa esto para usuarios, clínicos y políticas
Para el público general, el mensaje central es que no todas las píldoras semejantes a benzodiazepinas son iguales, aunque parezcan similares o compartan un nombre. Las versiones de diseño que circulan actualmente abarcan una enorme gama de potencias y pueden actuar a través de más de un punto de contacto en el interruptor calmante del cerebro. Algunas son mucho más potentes que los medicamentos conocidos, otras son débiles y unas pocas incluso actúan en la dirección contraria. Dado que muchos metabolitos activos también contribuyen, el efecto global puede ser más fuerte y durar más de lo esperado. Este trabajo proporciona un mapa detallado que vincula pequeños ajustes químicos con resultados funcionales en un receptor cerebral clave, ayudando a los toxicólogos a interpretar intoxicaciones, a los grupos de reducción de daños a aconsejar sobre riesgos relativos y a los reguladores a anticipar cómo podrían comportarse futuros fármacos de diseño antes de que alcancen un uso generalizado.
Cita: Norman, C., Liin, S.I., Jauregi-Miguel, A. et al. In vitro γ-aminobutyric acid A (GABAA) receptor activity and binding interactions at the α+/γ2– interface of 53 prescription and designer benzodiazepines. Commun Chem 9, 155 (2026). https://doi.org/10.1038/s42004-026-02001-x
Palabras clave: benzodiazepinas de diseño, receptor GABAA, seguridad de fármacos, relaciones estructura‑actividad, sedantes recreativos