Clear Sky Science · zh
Ref-1 驱动溃疡性结肠炎诱发的造血细胞系统性缺陷
为什么肠道疾病会影响你的血液
溃疡性结肠炎通常被认为是大肠的疾病,会引起疼痛、出血和频繁如厕。该研究表明,长期存在的肠道炎症其影响可以延伸到制造新血细胞的工厂——骨髓。通过追踪来自发炎结肠的信号如何重塑血液生成,研究者们还测试了可能有助于同时恢复肠道和血液平衡的药物。
当肠道问题“与”骨髓对话
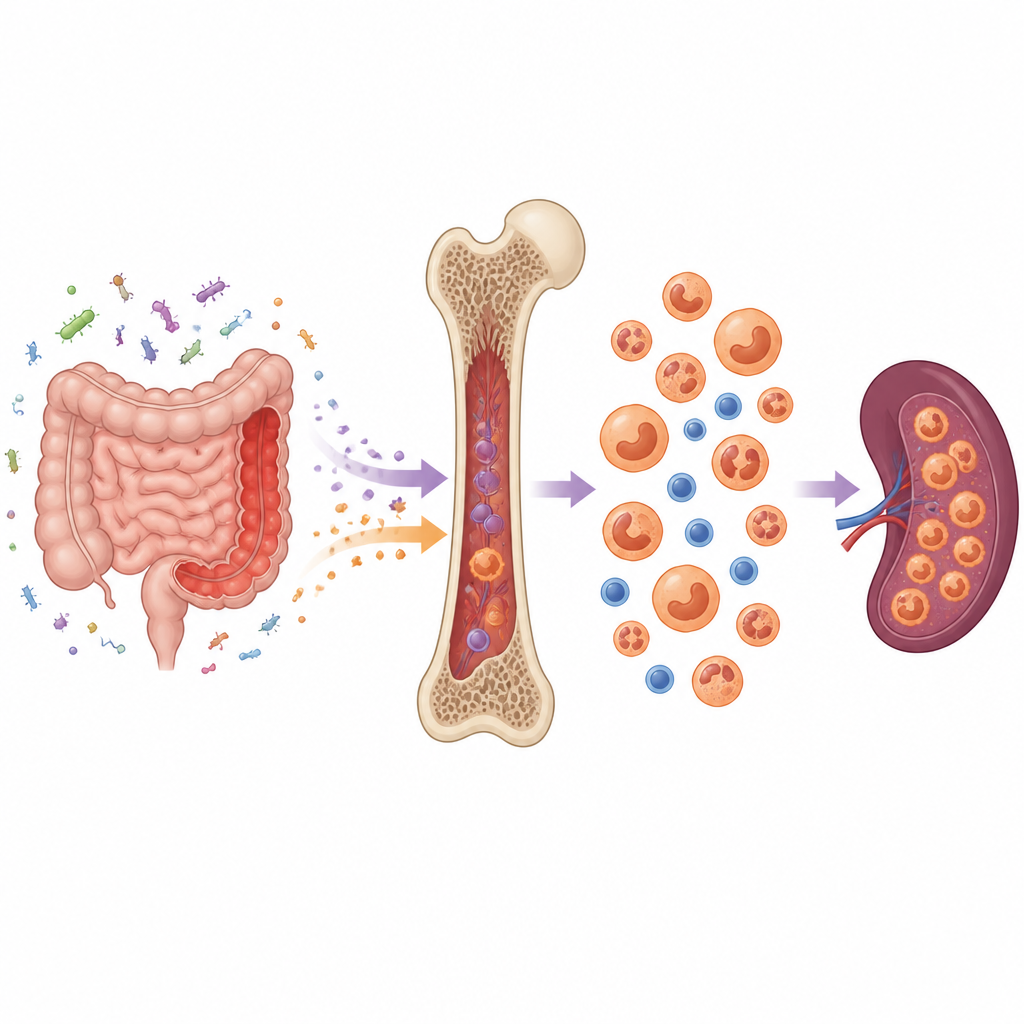
在溃疡性结肠炎中,免疫系统对肠道微生物反应过度,损伤肠黏膜并使细菌产物和炎性分子漏入血液循环。研究团队使用了模拟人类慢性溃疡性结肠炎的小鼠模型。他们发现,持续的肠道炎症导致骨髓超负荷,总细胞数增多、早期造血细胞库扩大。这些干细胞和祖细胞不再安静地自我更新,而是变得更为活跃,循环更快且死亡率降低。
从平衡血液到髓系偏向
通常,骨髓中的干细胞会产生白细胞、红细胞和血小板的混合。在易患结肠炎的小鼠中,这一平衡发生了改变。早期前体细胞被推动更多地产生髓系细胞,如中性粒细胞和促炎性单核细胞,而牺牲了淋巴细胞和红细胞前体等其他谱系。脾脏也出现了类似变化,肿大并开始作为备用的造血部位发挥作用。这些改变形成了一个反馈回路,将更多的炎性细胞输送回受损的肠道。
问题核心的氧化还原开关
研究者们深入探查了导致这种血液生成偏向的分子开关。他们关注一种称为 Ref-1 的蛋白,该蛋白帮助控制其他蛋白如何响应细胞内化学环境的变化。在结肠炎中,Ref-1 活性与促生长因子 G-CSF 水平升高以及低氧传感器 HIF-1α 的激活相关。共同作用下,这些信号在线粒体干细胞和祖细胞上开启了白细胞介素-1 的受体,使其倾向于反复产生炎性髓系细胞。
将开关调回去
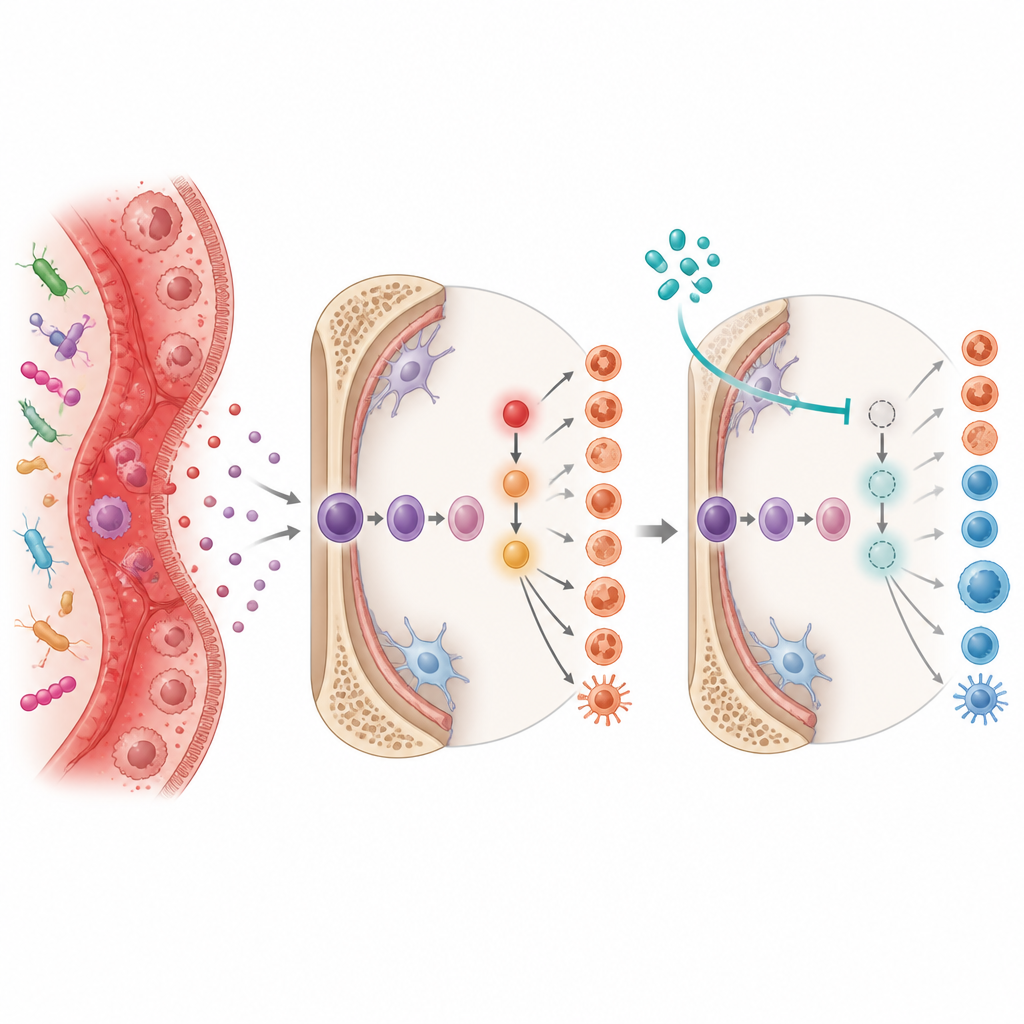
为验证是否可以中断这一信号级联,团队在结肠炎小鼠中使用了两种药物。APX3330 阻断 Ref-1 的氧化还原(redox)功能,而 echinomycin 干扰 HIF-1α。两种药物均在慢性结肠炎发病过程中给药。在每种情况下,药物都减少了肠道病变的迹象,使肿大的脾脏缩小,并在骨髓和脾脏中恢复了更健康的干细胞与成熟血细胞比例。在移植实验中,来自药物处理结肠炎小鼠的骨髓移植植入效果更好,并使受体动物的结肠更长寿、更健康,这表明仅通过纠正干细胞行为就能缓解肠道损伤。
这对溃疡性结肠炎患者意味着什么
总体而言,这项工作揭示了慢性肠道炎症如何将机体的造血系统重编程为自我增强的炎性状态的通路。通过识别 Ref-1、HIF-1α 和白细胞介素-1 受体作为这一链条中的关键步骤,研究提示针对这些分子的药物未来可能不仅能缓解肠道症状,还能重置不健康的血细胞生成。尽管这些发现来自小鼠而尚非临床疗法,但它们强调了肠道与骨髓的紧密联系,并指明了思考和管理长期炎性肠病的新方向。
引用: Kumar, R., Kanumuri, R., Burns, S.S. et al. Ref-1 drives ulcerative colitis induced systemic defects in hematopoietic cells. Commun Biol 9, 635 (2026). https://doi.org/10.1038/s42003-026-09860-z
关键词: 溃疡性结肠炎, 骨髓, 造血, 炎症, 干细胞