Clear Sky Science · sv
Ref-1 driver ulcerös kolit-inducerade systemiska brister i hematopoetiska celler
Varför tarmsjukdom kan påverka ditt blod
Ulcerös kolit ses vanligen som en sjukdom i tjocktarmen som ger smärta, blödningar och frekventa toalettbesök. Denna studie visar att effekten av långvarig tarminflammation kan nå ända till benmärgen, fabriken som tillverkar nya blodceller. Genom att spåra hur signaler från en inflammerad tjocktarm omformar blodbildningen testar forskarna också läkemedel som kan hjälpa till att återställa balans både i tarmen och i blodet.
När tarmproblem talar med benmärgen
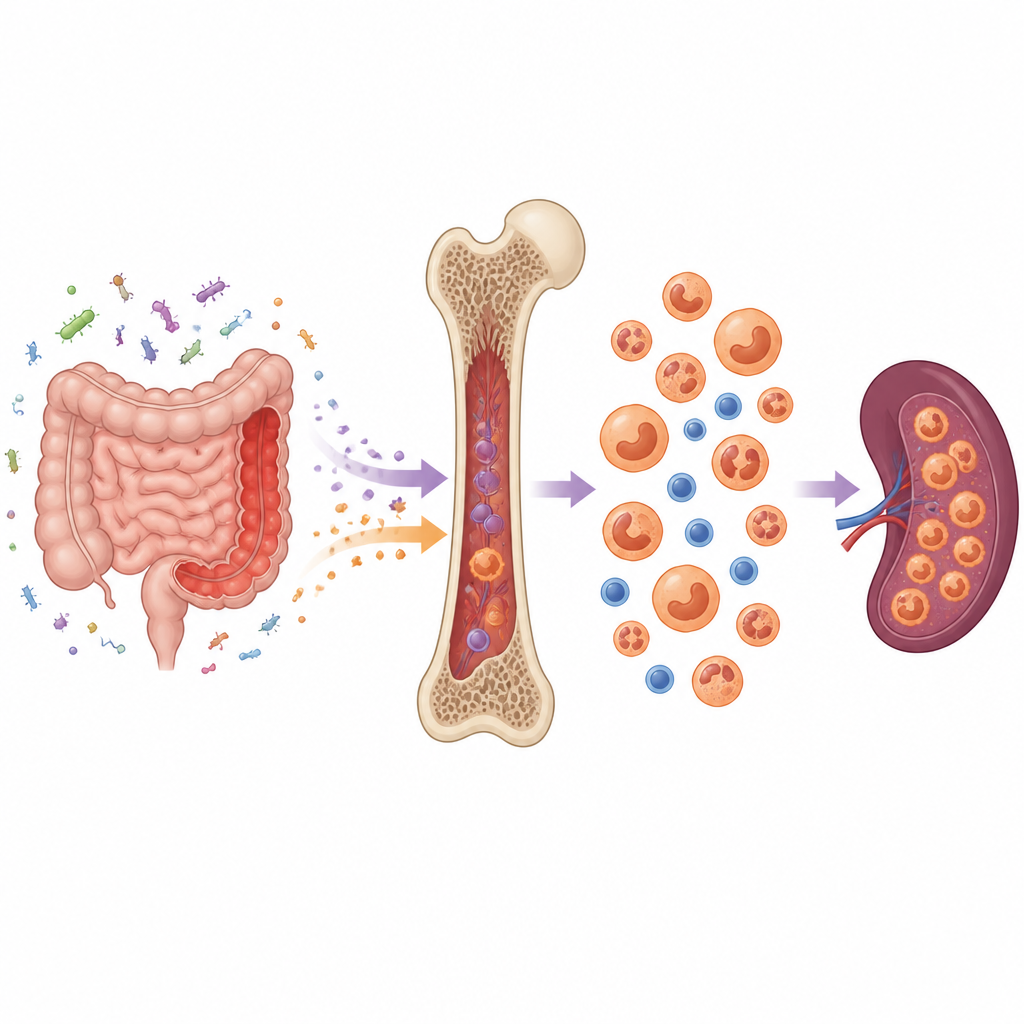
Vid ulcerös kolit överreagerar immunsystemet mot tarmens mikrober, vilket skadar tarmens slemhinna och tillåter bakteriella produkter och inflammatoriska molekyler att läcka ut i blodomloppet. Forskarna använde en musmodell som efterliknar kronisk ulcerös kolit hos människor. De fann att den pågående tarminflammationen gjorde att benmärgen blev överbelastad, med fler totala celler och en förstorad pool av tidiga blodbildande celler. Istället för att stillsamt förnya sig själva blev dessa stam- och progenitorceller mer aktiva, cyklade snabbare och dog mer sällan.
Från balanserat blod till en myeloid förskjutning
Normalt genererar stamceller i märgen en blandning av vita blodkroppar, röda blodkroppar och trombocyter. Hos möss benägna för kolit skiftade denna balans. Tidiga förstadier pressades att producera fler myeloida celler, såsom neutrofiler och inflammatoriska monocyter, på bekostnad av andra linjer som lymfocyter och röda blodcellspre-kursorer. Liknande förändringar syntes i mjälten, som blev förstorad och började fungera som en reservplats för blodproduktion. Dessa förändringar skapade en återkopplingsslinga som förde fler inflammatoriska celler tillbaka till den sjuka tarmen.
En redoxomkopplare i hjärtat av problemet
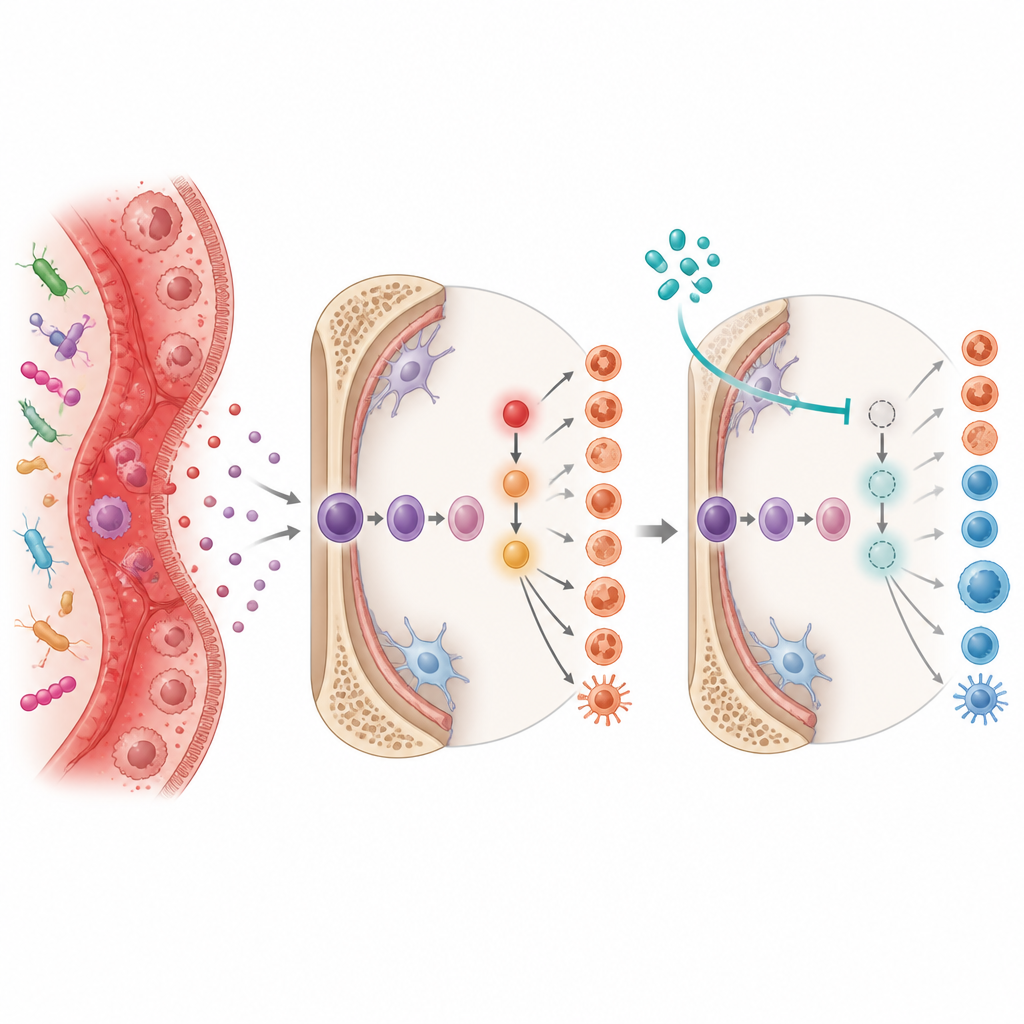
Forskarna grävde i de molekylära brytarna bakom denna snedvridna blodproduktion. De fokuserade på ett protein kallat Ref-1, som hjälper till att styra hur andra proteiner svarar på förändringar i cellens kemiska miljö. Vid kolit kopplades Ref-1-aktivitet till höga nivåer av tillväxtfaktorn G-CSF och till aktivering av HIF-1α, en sensor för låg syrehalt som också svarar på inflammation. Tillsammans slog dessa signaler på receptorer för alarmmolekylen interleukin 1 på stam- och progenitorceller och styrde dem mot upprepade cykler av inflammatorisk myeloid produktion.
Att stänga av brytarna igen
För att se om detta signalflöde kunde avbrytas behandlade teamet kolitmöss med två läkemedel. APX3330 blockerar Ref-1:s redox- eller oxidation-reduktionsfunktion, medan echinomycin stör HIF-1α. Båda behandlingarna gavs under utvecklingen av kronisk kolit. I båda fallen minskade läkemedlen tecken på tarmsjukdom, krympte förstorade mjältar och återställde en hälsosammare blandning av stamceller och mogna blodceller i benmärg och mjälte. I transplantationsförsök engraftade benmärg från läkemedelsbehandlade kolitmöss bättre och ledde till längre, friskare tjocktarmar hos mottagarna, vilket visar att korrigering av stamcellsbeteendet i sig kunde lindra tarmskadan.
Vad detta innebär för personer med ulcerös kolit
Sammanfattningsvis visar detta arbete en väg genom vilken kronisk tarminflammation kan omprogrammera kroppens blodbildande system till ett självförstärkande inflammatoriskt tillstånd. Genom att identifiera Ref-1, HIF-1α och interleukin 1-receptorn som nyckelsteg i denna kedja antyder studien att läkemedel som riktar sig mot dessa molekyler en dag kan hjälpa inte bara att dämpa tarmens symtom utan också återställa en ohälsosam blodcellsproduktion. Även om dessa fynd kommer från möss och ännu inte är behandlingar för patienter, framhäver de hur nära sammanlänkade tarm och benmärg är och pekar mot nya sätt att tänka kring hantering av långvarig inflammatorisk tarmsjukdom.
Citering: Kumar, R., Kanumuri, R., Burns, S.S. et al. Ref-1 drives ulcerative colitis induced systemic defects in hematopoietic cells. Commun Biol 9, 635 (2026). https://doi.org/10.1038/s42003-026-09860-z
Nyckelord: ulcerös kolit, benmärg, hematopoes, inflammation, stamceller