Clear Sky Science · pl
Ref-1 napędza uogólnione defekty w komórkach krwiotwórczych wywołane wrzodziejącym zapaleniem jelita
Dlaczego choroba jelit może wpływać na krew
Wrzodziejące zapalenie jelita zwykle postrzega się jako schorzenie jelita grubego, wywołujące ból, krwawienia i częste wizyty w toalecie. Ta praca pokazuje jednak, że wpływ długotrwałego zapalenia jelit sięga aż do szpiku kostnego — fabryki, która wytwarza nowe komórki krwi. Śledząc, jak sygnały z zapalnego jelita przekształcają procesy krwiotwórcze, badacze testowali też leki, które mogą pomóc przywrócić równowagę zarówno w jelicie, jak i w krwi.
Gdy problemy jelitowe komunikują się ze szpikiem
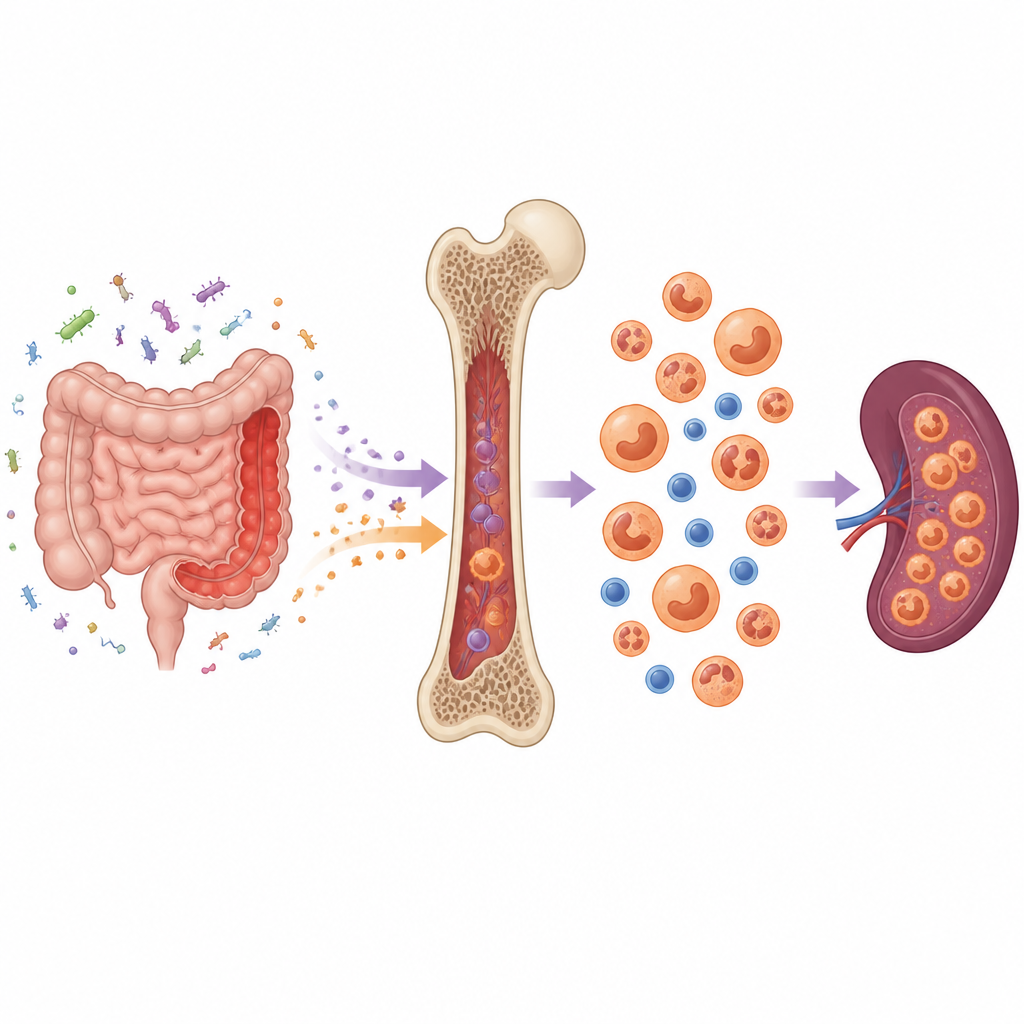
W wrzodziejącym zapaleniu jelita układ odpornościowy nadmiernie reaguje na mikroby w jelicie, uszkadzając wyściółkę jelitową i pozwalając produktom bakteryjnym oraz cząsteczkom zapalnym przedostać się do krwi. Zespół użył modelu mysiego odzwierciedlającego przewlekłe wrzodziejące zapalenie jelita u ludzi. Stwierdzili, że utrzymujące się zapalenie jelita powodowało przeciążenie szpiku: zwiększała się liczba komórek i powiększała pula wczesnych komórek krwiotwórczych. Zamiast spokojnie odnawiać się, te komórki macierzyste i prekursorowe stały się bardziej aktywne, szybciej się dzieliły i rzadziej umierały.
Z równowagi krwi w stronę przewagi mieloidalnej
Zazwyczaj komórki macierzyste w szpiku wytwarzają mieszankę białych krwinek, erytrocytów i płytek krwi. U myszy podatnych na zapalenie jelit ta równowaga uległa przesunięciu. Wczesne prekursory zostały skierowane do produkcji większej liczby komórek mieloidalnych, takich jak neutrofile i zapalne monocyty, kosztem innych linii, np. limfocytów i prekursorów erytrocytów. Podobne zmiany wystąpiły w śledzionie, która uległa powiększeniu i zaczęła pełnić funkcję zapasowego miejsca produkcji krwi. Te zmiany tworzyły pętlę sprzężenia zwrotnego, dostarczając więcej komórek zapalnych do chorego jelita.
Przełącznik redoks w centrum problemu
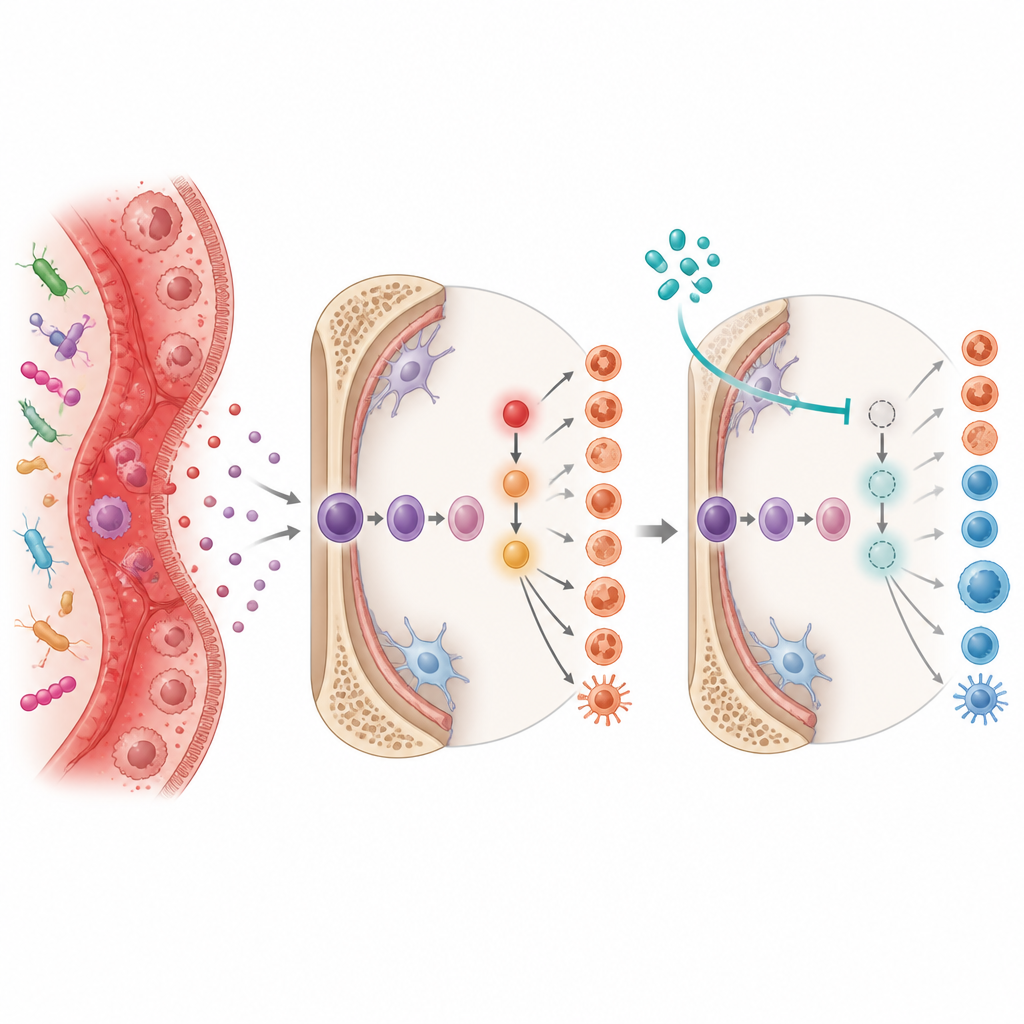
Badacze zagłębili się w molekularne przełączniki stojące za tym zaburzonym wytwarzaniem krwi. Skoncentrowali się na białku zwanym Ref-1, które pomaga kontrolować, jak inne białka reagują na zmiany w środowisku chemicznym komórki. W zapaleniu jelit aktywność Ref-1 wiązała się z wysokim poziomem czynnika wzrostu G-CSF i z aktywacją HIF-1α — czujnika niskiego poziomu tlenu, który także reaguje na zapalenie. Te sygnały razem włączały receptory dla alarmowej cząsteczki interleukiny 1 na komórkach macierzystych i prekursorowych, skłaniając je do powtarzających się cykli produkcji zapalnych komórek mieloidalnych.
Przygaszanie przełączników
Aby sprawdzić, czy tę kaskadę sygnałową da się przerwać, zespół leczył myszy z zapaleniem jelit dwoma lekami. APX3330 blokuje funkcję redoks, czyli reakcję utleniania/redukcji Ref-1, podczas gdy echinomycin zakłóca działanie HIF-1α. Oba leki podawano w trakcie rozwoju przewlekłego zapalenia jelit. W każdym przypadku leczenie zmniejszało objawy choroby jelit, kurczyło powiększone śledziony i przywracało zdrowszy skład komórek macierzystych oraz dojrzałych komórek krwi w szpiku i śledzionie. W eksperymentach transplantacyjnych szpik od myszy leczonych lekami lepiej wszczepiał się i prowadził do dłuższych, zdrowszych okrężnic u biorców, co pokazuje, że skorygowanie zachowania komórek macierzystych samo w sobie może złagodzić uszkodzenia jelit.
Co to oznacza dla osób z wrzodziejącym zapaleniem jelita
Podsumowując, praca ujawnia szlak, dzięki któremu przewlekłe zapalenie jelit może przeprogramować system wytwarzania krwi w organizmie, zamieniając go w samonapędzający się stan zapalny. Identyfikując Ref-1, HIF-1α i receptor dla interleukiny 1 jako kluczowe kroki w tym łańcuchu, badanie sugeruje, że leki celujące w te molekuły mogłyby w przyszłości nie tylko złagodzić objawy jelitowe, ale także zresetować niezdrową produkcję komórek krwi. Chociaż wyniki pochodzą z badań na myszach i nie są jeszcze terapiami dla pacjentów, podkreślają, jak blisko powiązane są jelito i szpik kostny, i wskazują nowe kierunki myślenia o leczeniu przewlekłych chorób zapalnych jelit.
Cytowanie: Kumar, R., Kanumuri, R., Burns, S.S. et al. Ref-1 drives ulcerative colitis induced systemic defects in hematopoietic cells. Commun Biol 9, 635 (2026). https://doi.org/10.1038/s42003-026-09860-z
Słowa kluczowe: wrzodziejące zapalenie jelita, szpik kostny, hematopoeza, zapalenie, komórki macierzyste