Clear Sky Science · zh
通过单细胞RNA谱分析剖析胃窦肠化生及早期肠型胃癌的分化起源
为什么胃黏膜细胞的变化很重要
胃癌是全球最致命的癌症之一,部分原因在于常常在晚期才被发现。然而在肿瘤出现之前,胃的下段(窦部)上皮细胞会经历一系列微妙的变化,这些变化可能在多年间逐步展开。本研究提出了一个简单但关键的问题:在这条病程路径上,究竟哪些具体细胞最先表现出类癌特征,以及普通胃细胞如何被重新编程为类肠细胞并进一步转变为癌细胞?通过逐个追踪单个细胞,研究者描绘出这一隐秘演变的路线图,并指向可能更早发现和干预癌变的新途径。 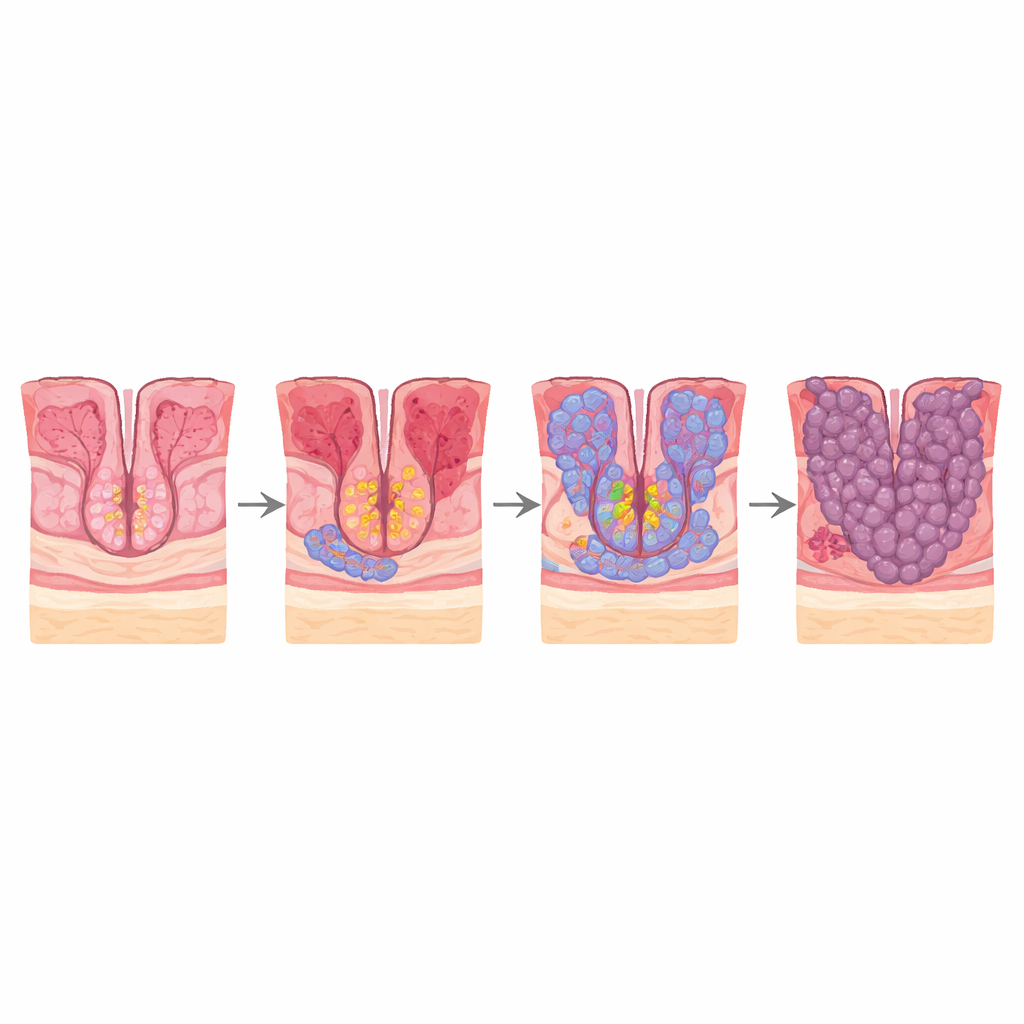
从炎症到早期癌变的演进路线
大多数肠型胃癌遵循已描述的序列:慢性胃炎、腺体丧失(萎缩)、胃上皮被肠样细胞取代(肠化生),最终发展为早期癌。作者重新分析了覆盖这一全过程的活检单细胞RNA测序数据——包括非萎缩性胃炎、萎缩性胃炎、肠化生和早期胃癌。该技术可读取数千个单细胞中活跃的基因,从而对每个细胞进行分类并推断其可能的“家族谱系”。他们将这些数据与空间转录组学相结合(补回每个细胞在组织中的位置信息),并用患者样本的染色验证关键模式。
健康但受炎症影响的胃中的关键参与者
在早期的非萎缩性胃炎阶段,窦部上皮主要由三种上皮细胞构成:覆盖表面的胃小凹黏液细胞、位于腺体深处的腺体黏液细胞,以及位于两者之间数量较少的祖细胞群。通过分析基因活性和发育“评分”,研究团队显示这些祖细胞位于系统的根部,通过一个中间、较不分化的状态产生小凹和腺体黏液细胞。特定的调控蛋白,尤其是称为TAGLN2的蛋白,在祖细胞向小凹黏液细胞分化时被激活,助推这一在炎症期间的正常更新过程。
当修复演变为类肠组织
随着病情进展至慢性萎缩性胃炎并进入肠化生,细胞谱系的平衡发生转变。小凹黏液细胞减少,而腺体黏液细胞和新的类肠细胞类型扩大。在肠化生中,研究者发现祖细胞和腺体黏液细胞都能获得类肠干细胞的特征,进而成熟为吸收性肠细胞——这是肠道的标志性细胞。他们追踪到两条并行的路径,在达到一个中间的类肠干细胞状态后汇聚,最终分化为成熟的肠上皮细胞。另一条分泌性祖细胞分支则生成杯状细胞,即肠道中分泌黏液的细胞。一组代谢调控蛋白,尤其是HNF4A和ESRRA,在这些路径上逐步被激活,似乎引导了胃向肠的转化。人组织的空间图谱显示腺体中标记物沿轴呈平滑梯度,证实这些转变以连续、分层的方式发生。 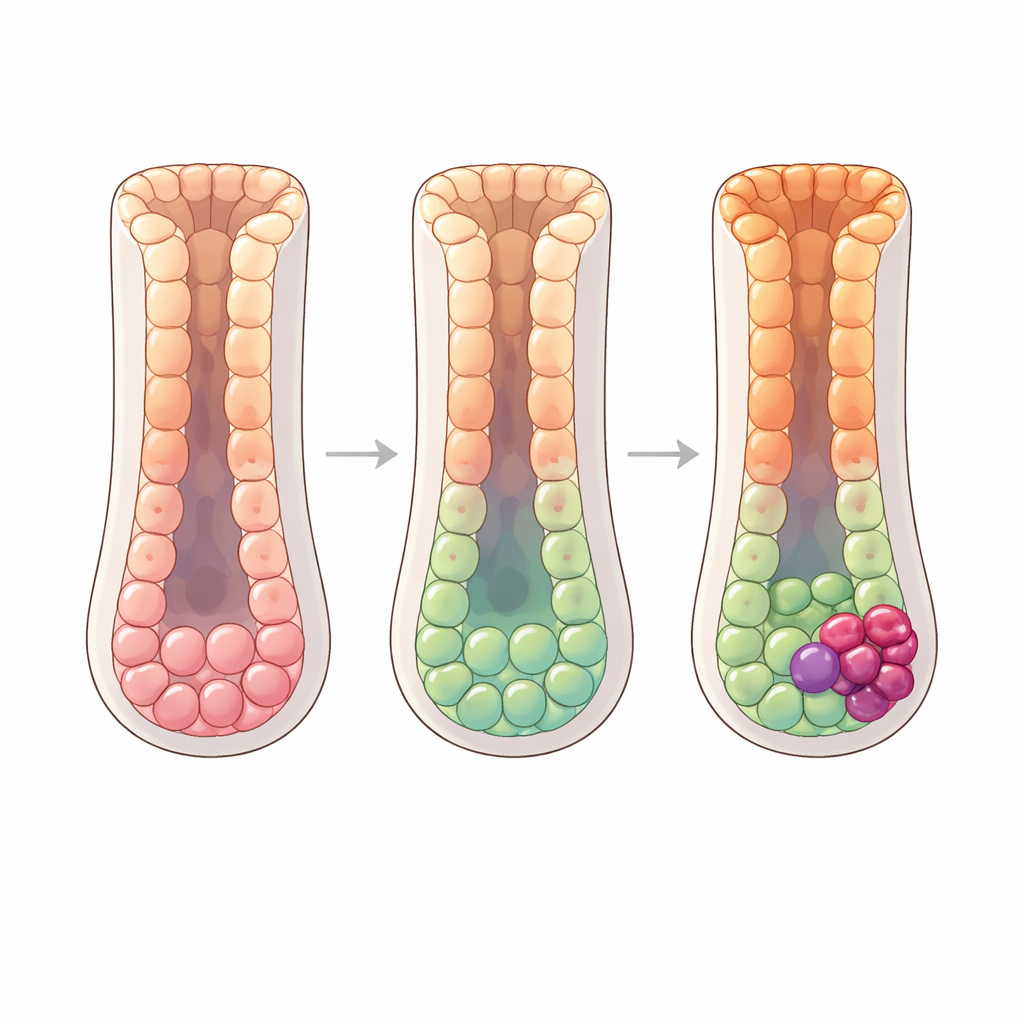
定位早期肿瘤的可能起始细胞
在早期胃癌样本中,团队考察了哪些非癌细胞在基因表达及染色体改变方面与新兴的癌细胞最为相似。祖细胞显示出最高的相似性,包括匹配的拷贝数变化模式,暗示至少部分癌症直接起源于这类细胞群。在祖细胞中,他们识别出一类由两种基因KIAA0101和PRAP1标记的亚群,在癌变组织中强烈富集,而在其他部位几乎不可检测。这类双阳性细胞在空间图谱中聚集于恶性区域,并在荧光染色中被标出,支持它们是早期肿瘤直接前体的观点。随着这些祖细胞向癌细胞转变,额外的调控蛋白如SIRT6和XRCC4被激活,可能有助于耐受DNA损伤、维持炎症应答并支持这一危险转变过程中的细胞存活。
对预防和早期发现的意义
对外行而言,这项工作将“胃部刺激可能导致癌变”这一模糊认知,转化为一张详细的路线图,说明在胃窦腺体内谁在何时何地扮演何种角色。研究表明,一小群祖细胞及腺体黏液细胞作为一个中心发动机,能从正常修复被重新导向,形成类肠组织并最终发展为早期癌。通过标记高危祖细胞的特定分子标志(如KIAA0101和PRAP1)以及关键控制开关(HNF4A、ESRRA、SIRT6),该研究提出了可在常规活检中识别危险变化的新检测思路,并指出了可在可见肿瘤形成前打断这一过程的潜在治疗靶点。
引用: Yin, H., Zhang, H., Zheng, S. et al. Dissecting the differentiation origins of intestinal metaplasia and early intestinal-type gastric cancer in gastric antrum by single-cell RNA profiling. npj Precis. Onc. 10, 167 (2026). https://doi.org/10.1038/s41698-026-01355-8
关键词: 胃癌, 肠化生, 单细胞RNA测序, 细胞谱系, 癌前病变