Clear Sky Science · de
Analyse der Differenzierungsursprünge von intestinaler Metaplasie und frühem intestinalem Magenkrebs im Antrum durch Einzelzell‑RNA‑Profiling
Warum Veränderungen der Magenschleimhautzellen wichtig sind
Magenkrebs gehört zu den weltweit tödlichsten Krebserkrankungen, unter anderem weil er häufig spät entdeckt wird. Noch bevor ein Tumor sichtbar wird, durchlaufen die Zellen, die den unteren Teil des Magens (das Antrum) auskleiden, über Jahre hinweg eine Folge subtiler Veränderungen. Die Studie stellt eine einfache, aber entscheidende Frage: Welche konkreten Zellen entlang dieses Wegs beginnen zuerst, sich wie Krebszellen zu verhalten, und wie werden normale Magenschleimhautzellen so umprogrammiert, dass sie intestinal‑ähnlich und schließlich krebsartig werden? Indem die Forschenden einzelne Zellen einzeln verfolgen, kartieren sie diese verborgene Entwicklung und weisen auf neue Möglichkeiten hin, Krebs früher zu erkennen und möglicherweise zu verhindern. 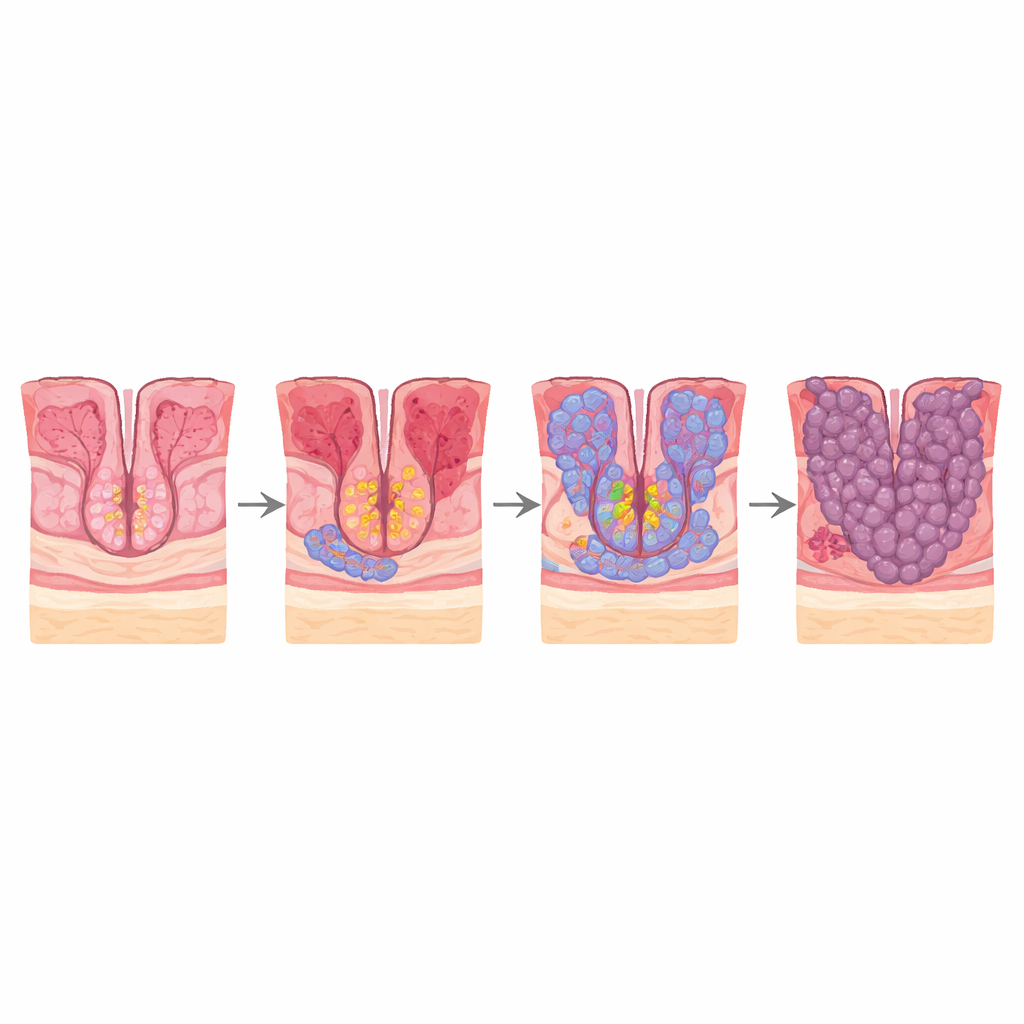
Die Reise von Reizung bis Frühkarzinom verfolgen
Die meisten intestinal‑typischen Magenkarzinome entstehen über eine gut beschriebene Abfolge: chronische Gastritis, Verlust normaler Drüsen (Atrophie), Ersetzung von Magenzellen durch darmähnliche Zellen (intestinale Metaplasie) und schließlich Frühkarzinom. Die Autor:innen werteten erneut Einzelzell‑RNA‑Sequenzierungsdaten aus Biopsien aus, die diesen gesamten Weg abdeckten – nicht‑atrophische Gastritis, atrophe Gastritis, intestinale Metaplasie und frühe Magenkrebsproben. Diese Technologie liest aus, welche Gene in Tausenden einzelner Zellen aktiv sind, wodurch jede Zelle klassifiziert und ihr wahrscheinlicher „Stammbaum“ geschlossen werden kann. Sie kombinierten diese Daten mit räumlicher Transkriptomik, die die Lage jeder Zelle im Gewebe rekonstituiert, und mit Färbungen von Patientenproben, um zentrale Muster zu bestätigen.
Die Hauptakteure in einem gesunden, aber entzündeten Magen
Im frühen, nicht‑atrophischen Gastritisstadium wird das Antrum von drei Haupttypen von Epithelzellen dominiert: Oberflächenbindende Pit‑Schleimhautzellen, tiefer in den Drüsen liegende Glandula‑Schleimhautzellen und ein kleineres Reservoir an Vorläuferzellen, das sich dazwischen befindet. Durch die Analyse der Genaktivität und von Entwicklungs‑„Scores“ zeigen die Forschenden, dass diese Vorläuferzellen an der Wurzel des Systems sitzen und sowohl Pit‑ als auch Glandula‑Schleimhautzellen über einen intermediären, weniger festgelegten Zustand hervorbringen. Bestimmte Regulationsproteine, insbesondere eines namens TAGLN2, werden eingeschaltet, wenn Vorläuferzellen zu Pit‑Schleimhautzellen werden, und unterstützen so diesen normalen Erneuerungsprozess während der Entzündung.
Wenn Reparatur in darmähnliches Gewebe umschlägt
Mit dem Voranschreiten der Erkrankung hin zu chronischer atropher Gastritis und schließlich intestinaler Metaplasie verschiebt sich das Gleichgewicht der Zelllinien. Pit‑Schleimhautzellen nehmen ab, während Glandula‑Schleimhautzellen und neue darmähnliche Zelltypen expandieren. In der intestinalen Metaplasie finden die Forschenden, dass sowohl Vorläuferzellen als auch Glandula‑Schleimhautzellen Merkmale intestinaler Stammzellen annehmen und dann zu absorptiven Enterozyten ausreifen, den typischen Zellen des Darms. Sie verfolgen zwei parallele Pfade, die auf einen intermediären intestinal‑ähnlichen Stammzellzustand zulaufen, bevor sie in voll entwickelte Enterozyten münden. Ein anderer sekretorischer Vorläuferzweig bildet Becherzellen, die schleimproduzierenden Zellen des Darms. Eine Gruppe von Stoffwechsel‑Regulatoren, insbesondere HNF4A und ESRRA, wird entlang dieser Pfade zunehmend aktiver und scheint die Transformation vom Magen zum Darm zu lenken. Räumliche Karten menschlichen Gewebes zeigen einen sanften Gradienten von Markern entlang der Drüsen, was bestätigt, dass diese Übergänge kontinuierlich und geschichtet erfolgen. 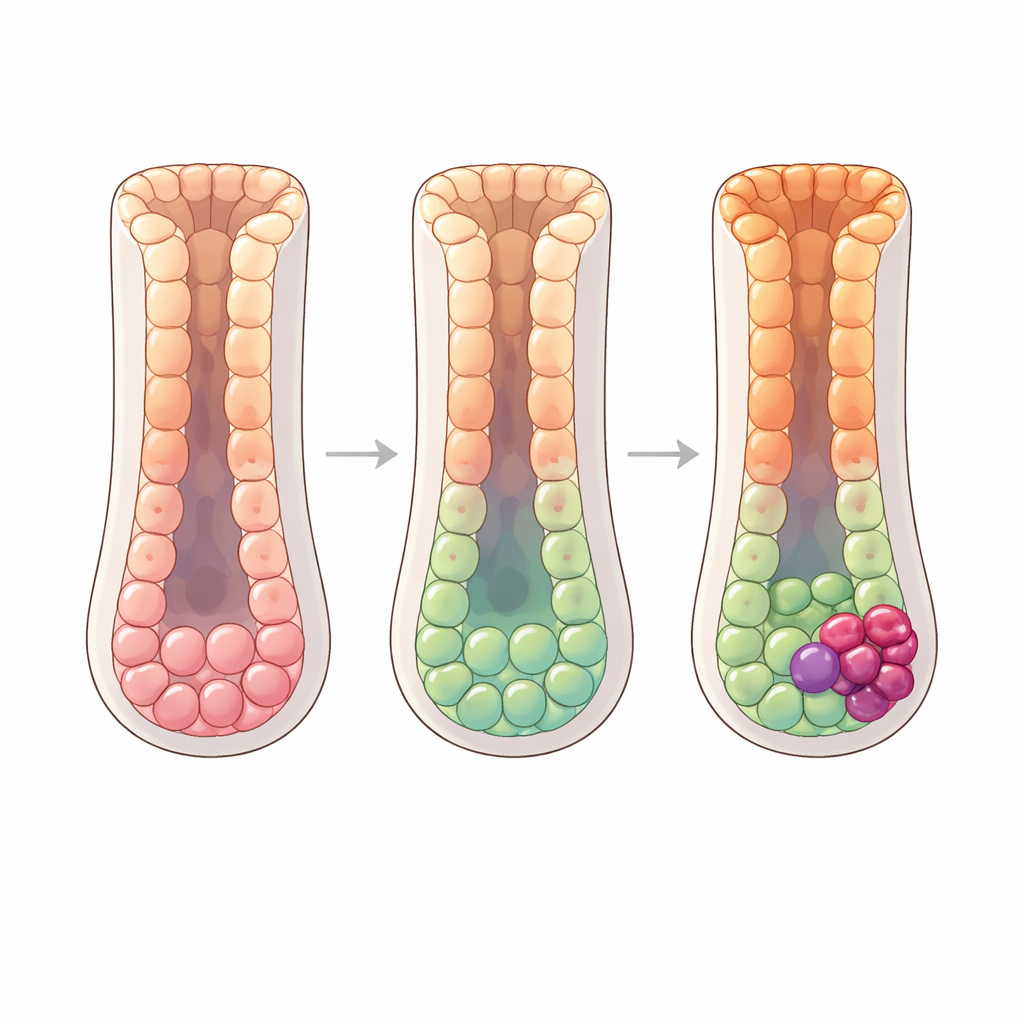
Die wahrscheinlichsten Ausgangszellen früher Tumoren eingrenzen
In Proben von frühem Magenkrebs untersuchen die Autor:innen, welche nicht‑tumorösen Zellen den entstehenden Krebszellen am ähnlichsten sind — sowohl hinsichtlich Genexpression als auch chromosomaler Veränderungen. Vorläuferzellen zeigen die höchste Ähnlichkeit, einschließlich übereinstimmender Muster von Kopienzahländerungen, was nahelegt, dass zumindest ein Teil der Tumoren direkt aus diesem Pool entsteht. Innerhalb der Vorläuferzellen identifizieren sie eine Subpopulation, die durch zwei Gene, KIAA0101 und PRAP1, markiert ist und in Krebsgewebe stark angereichert, sonst aber kaum nachweisbar ist. Diese doppelt positiven Zellen gruppieren sich in räumlichen Karten innerhalb maligner Bereiche und werden durch fluoreszenzbasierte Färbungen hervorgehoben, was die Idee stützt, dass sie unmittelbare Vorstufen früher Tumoren sind. Weitere Regulationsproteine, wie SIRT6 und XRCC4, werden aktiviert, wenn diese Vorläufer in Krebszellen übergehen, und könnten DNA‑Schadens‑Toleranz, Entzündungsantworten und Überleben während dieses gefährlichen Übergangs unterstützen.
Folgen für Prävention und Früherkennung
Für einen Laien verwandelt diese Arbeit ein unscharfes Bild – „Magenreizung kann zu Krebs führen“ – in eine detaillierte Landkarte, wer wann was und wo in den Drüsen des Magenantrums tut. Sie zeigt, dass ein kleiner Pool von Vorläufer- und Glandula‑Schleimhautzellen als zentrales Triebwerk fungiert, das von normaler Reparatur auf den Bau von darmähnlichem Gewebe und schließlich auf frühe Karzinome umgelenkt werden kann. Durch das Hervorheben spezifischer molekularer Marker hochriskanter Vorläufer (wie KIAA0101 und PRAP1) und zentraler Steuerungsschalter (HNF4A, ESRRA, SIRT6) schlägt die Studie neue Tests vor, die gefährliche Veränderungen in Routinediagnostik‑Biopsien erkennen könnten, sowie neue Therapieansätze, um den Prozess zu unterbrechen, bevor ein sichtbarer Tumor entsteht.
Zitation: Yin, H., Zhang, H., Zheng, S. et al. Dissecting the differentiation origins of intestinal metaplasia and early intestinal-type gastric cancer in gastric antrum by single-cell RNA profiling. npj Precis. Onc. 10, 167 (2026). https://doi.org/10.1038/s41698-026-01355-8
Schlüsselwörter: Magenkrebs, intestinale Metaplasie, Einzelzell‑RNA‑Sequenzierung, Zelllinie, präkanzeröse Läsionen