Clear Sky Science · fr
Dissection des origines de différenciation de la métaplasie intestinale et du cancer gastrique précoce de type intestinal dans l’antre gastrique par profilage ARN‑single‑cell
Pourquoi les modifications des cellules de la muqueuse gastrique sont importantes
Le cancer de l’estomac fait partie des cancers les plus meurtriers au monde, en partie parce qu’il est souvent découvert tardivement. Pourtant, avant l’apparition d’une tumeur, les cellules qui tapissent la partie inférieure de l’estomac (l’antre) traversent une série de changements subtils qui peuvent s’étaler sur des années. Cette étude pose une question simple mais cruciale : quelles cellules précises, au cours de ce cheminement, commencent d’abord à se comporter comme des cellules cancéreuses, et comment des cellules gastriques ordinaires sont‑elles reprogrammées en cellules de type intestinal puis en cellules cancéreuses ? En suivant les cellules une par une, les auteurs cartographient ce trajet caché et indiquent de nouvelles façons de repérer et éventuellement d’empêcher le cancer plus tôt. 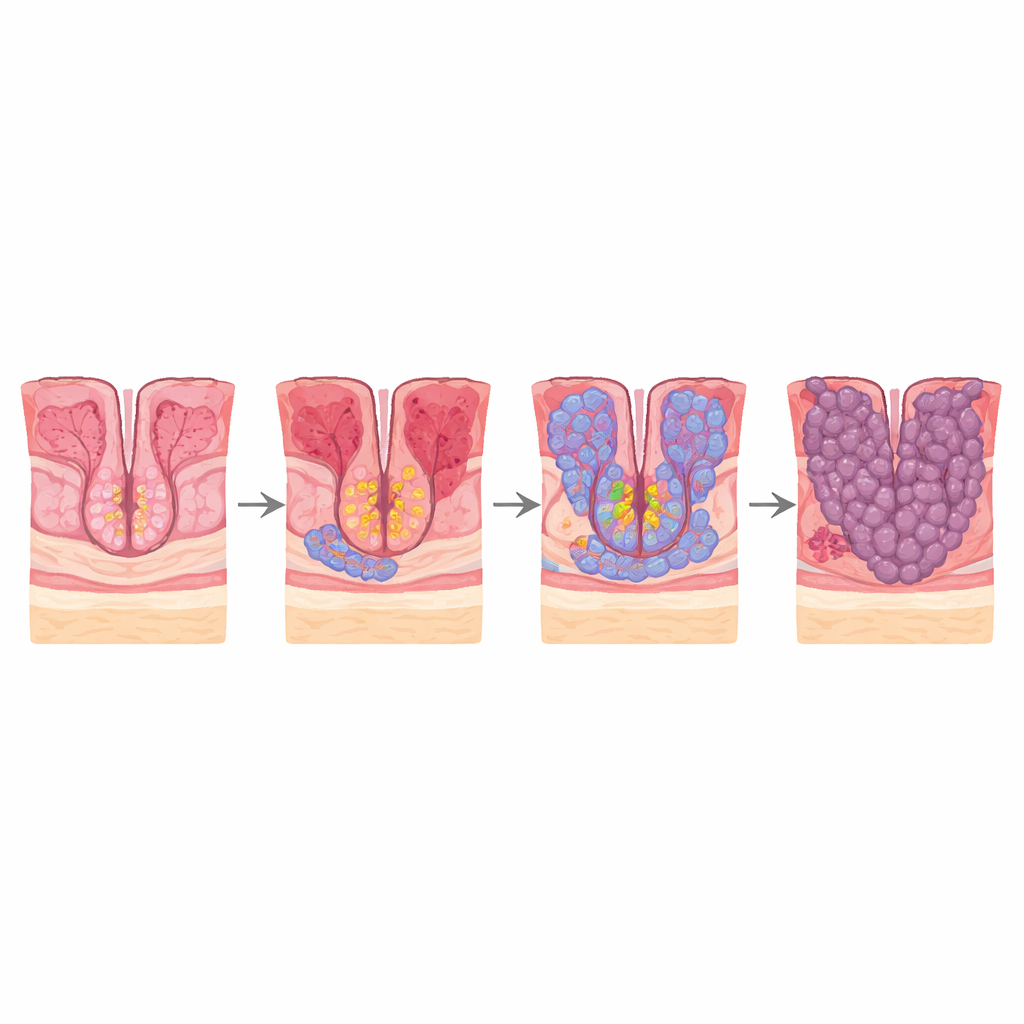
Suivre le parcours de l’irritation au cancer précoce
La plupart des cancers gastriques de type intestinal se développent selon une séquence bien décrite : gastrite chronique, perte des glandes normales (atrophie), remplacement des cellules gastriques par des cellules de type intestinal (métaplasie intestinale), puis cancer précoce. Les auteurs ont réanalysé des données de séquençage ARN unicellulaire issues de prélèvements couvrant l’ensemble de ce parcours : gastrite non atrophique, gastrite atrophique, métaplasie intestinale et cancer gastrique précoce. Cette technologie révèle quels gènes sont actifs dans des milliers de cellules individuelles, permettant de classer chaque cellule et d’inférer son « arbre généalogique » probable. Ils ont combiné ces données avec la transcriptomique spatiale, qui restitue la position de chaque cellule dans le tissu, ainsi qu’avec des colorations d’échantillons de patients pour confirmer les motifs clés.
Les acteurs clés dans un estomac sain mais enflammé
Au stade précoce de gastrite non atrophique, l’épithélium de l’antre est dominé par trois types cellulaires épithéliaux principaux : les cellules muqueuses de surface (pit mucous cells) qui tapissent la surface, les cellules muqueuses glandulaires plus profondes, et un pool plus réduit de cellules progénitrices situées entre les deux. En analysant l’activité génique et des « scores » de développement, l’équipe montre que ces cellules progénitrices se trouvent à la racine du système, donnant naissance à la fois aux cellules muqueuses de surface et aux cellules muqueuses glandulaires via un état intermédiaire moins engagé. Des protéines de contrôle spécifiques, en particulier une appelée TAGLN2, s’activent lorsque les progéniteurs deviennent des cellules muqueuses de surface, contribuant à piloter ce processus normal de renouvellement pendant l’inflammation.
Quand la réparation se transforme en tissu de type intestinal
À mesure que la maladie progresse vers la gastrite atrophique chronique puis la métaplasie intestinale, l’équilibre des lignées évolue. Les cellules muqueuses de surface déclinent, tandis que les cellules muqueuses glandulaires et de nouveaux types cellulaires de type intestinal se développent. Dans la métaplasie intestinale, les chercheurs montrent que les cellules progénitrices et les cellules muqueuses glandulaires peuvent acquérir des caractéristiques de cellules souches de type intestinal puis mûrir en entérocytes absorbants, caractéristiques de l’intestin. Ils retracent deux voies parallèles qui convergent vers un état stem‑cellulaire intermédiaire de type intestinal avant d’aboutir à des entérocytes pleinement différenciés. Une autre branche progénitrice sécrétoire donne naissance aux cellules caliciformes (goblet cells), cellules sécrétrices de mucus normalement présentes dans l’intestin. Un ensemble de régulateurs métaboliques, notamment HNF4A et ESRRA, s’active de plus en plus le long de ces trajectoires et semble orienter la transformation gastrique→intestinale. Des cartes spatiales de tissus humains montrent un gradient lisse de marqueurs le long des glandes, confirmant que ces transitions se produisent de façon continue et stratifiée. 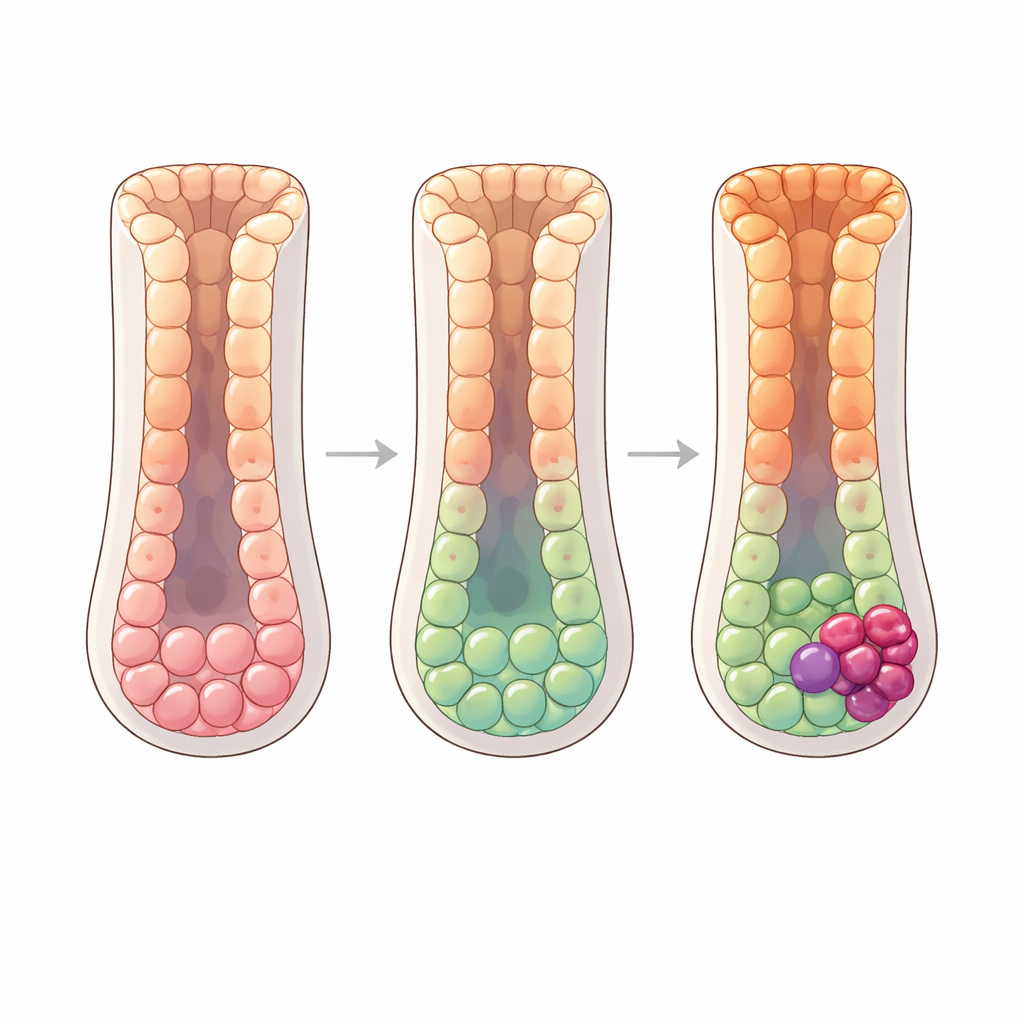
Identifier les cellules probablement à l’origine des tumeurs précoces
Dans les échantillons de cancer gastrique précoce, l’équipe recherche quelles cellules non cancéreuses ressemblent le plus aux cellules tumorales émergentes, tant en expression génique qu’en altérations chromosomiques. Les cellules progénitrices montrent la plus forte similarité, y compris des schémas correspondants de variations du nombre de copies, ce qui suggère qu’au moins certains cancers émergent directement de ce pool. Parmi les progéniteurs, ils identifient un sous‑ensemble marqué par deux gènes, KIAA0101 et PRAP1, fortement enrichi dans les tissus cancéreux et à peine détectable ailleurs. Ces cellules doublement positives se regroupent dans des régions malignes sur les cartes spatiales et sont mises en évidence par des colorations fluorescentes, soutenant l’idée qu’elles sont des précurseurs immédiats des tumeurs précoces. D’autres protéines régulatrices, telles que SIRT6 et XRCC4, s’activent lorsque ces progéniteurs basculent vers des cellules cancéreuses et pourraient aider à soutenir la tolérance aux dommages de l’ADN, l’inflammation et la survie au cours de cette transition dangereuse.
Ce que cela signifie pour la prévention et la détection précoce
Pour un observateur non spécialiste, ce travail transforme une image floue — « une irritation de l’estomac peut conduire au cancer » — en une feuille de route détaillée de qui fait quoi, quand et où à l’intérieur des glandes de l’antre gastrique. Il montre qu’un petit pool de progéniteurs et de cellules muqueuses glandulaires agit comme un moteur central qui peut être détourné du renouvellement normal vers la construction de tissu de type intestinal puis, éventuellement, vers le cancer précoce. En signalant des marqueurs moléculaires spécifiques des progéniteurs à haut risque (tels que KIAA0101 et PRAP1) et des commutateurs de contrôle clés (HNF4A, ESRRA, SIRT6), l’étude propose de nouveaux tests pouvant détecter des changements dangereux dans des biopsies de routine et de nouvelles cibles thérapeutiques visant à interrompre le processus avant qu’une tumeur visible ne se forme.
Citation: Yin, H., Zhang, H., Zheng, S. et al. Dissecting the differentiation origins of intestinal metaplasia and early intestinal-type gastric cancer in gastric antrum by single-cell RNA profiling. npj Precis. Onc. 10, 167 (2026). https://doi.org/10.1038/s41698-026-01355-8
Mots-clés: cancer gastrique, métaplasie intestinale, séquençage ARN unicellulaire, lignée cellulaire, lésions précancéreuses