Clear Sky Science · es
Disecando los orígenes de la diferenciación en la metaplasia intestinal y el cáncer gástrico temprano de tipo intestinal en el antro gástrico mediante perfilado de ARN unicelular
Por qué importan los cambios en las células del revestimiento del estómago
El cáncer de estómago es uno de los más mortales del mundo, en parte porque con frecuencia se detecta de forma tardía. Sin embargo, antes de que aparezca un tumor, las células que recubren la parte inferior del estómago (el antro) atraviesan una serie de cambios sutiles que pueden desarrollarse durante años. Este estudio plantea una pregunta simple pero crucial: ¿qué células exactas a lo largo de este recorrido empiezan primero a comportarse como cancerosas, y cómo se reprograman las células gástricas ordinarias en células de aspecto intestinal y, después, cancerosas? Al seguir células individuales una por una, los investigadores trazan este trayecto oculto y señalan nuevas vías para detectar y, posiblemente, detener el cáncer antes.
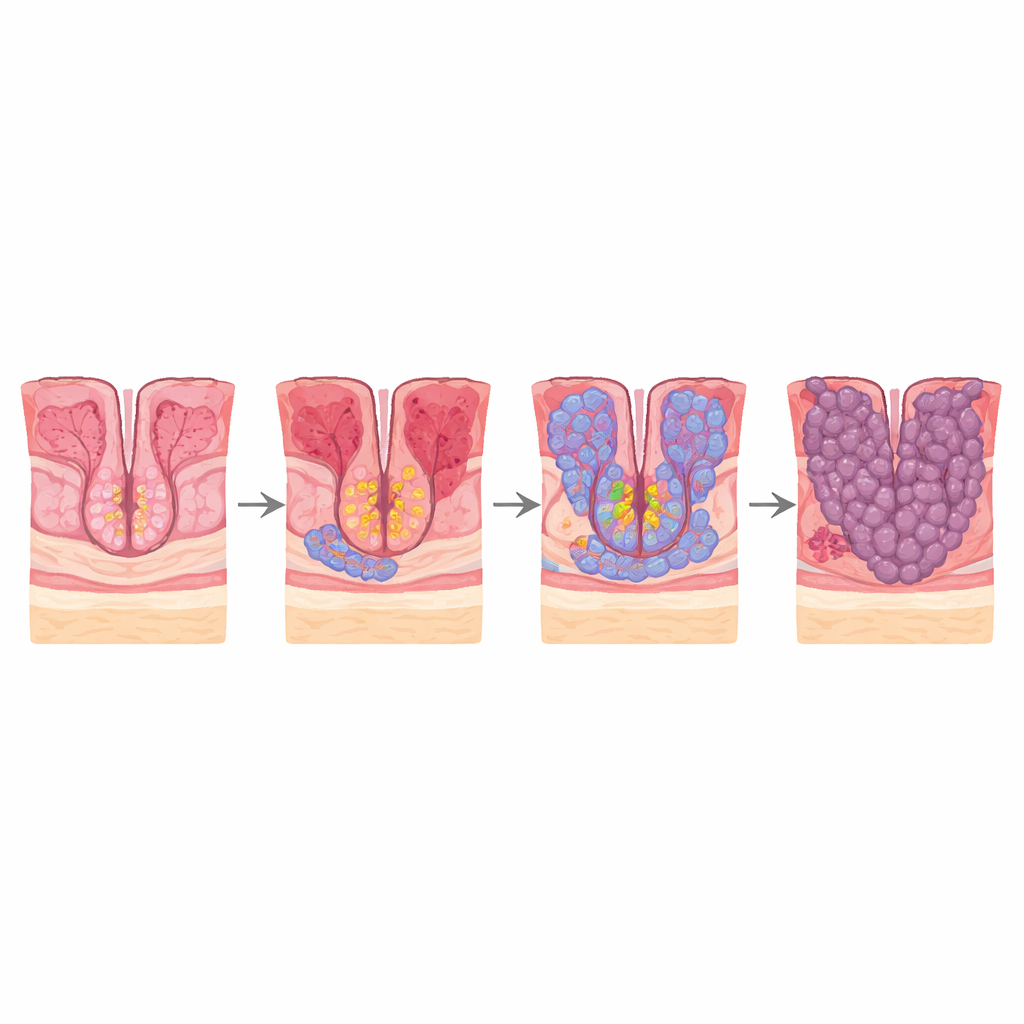
Siguiendo el viaje desde la irritación hasta el cáncer temprano
La mayoría de los cánceres gástricos de tipo intestinal surgen mediante una secuencia bien descrita: gastritis crónica, pérdida de glándulas normales (atrofia), reemplazo de células gástricas por células de aspecto intestinal (metaplasia intestinal) y, finalmente, cáncer temprano. Los autores reanalizaron datos de secuenciación de ARN unicelular de biopsias que abarcan todo este recorrido: gastritis no atrófica, gastritis atrófica, metaplasia intestinal y cáncer gástrico temprano. Esta tecnología lee qué genes están activos en miles de células individuales, lo que permite clasificar cada célula e inferir su probable “árbol genealógico”. Combinan estos datos con transcriptómica espacial, que reincorpora la posición de cada célula en el tejido, y con tinciones de muestras de pacientes para confirmar los patrones clave.
Los protagonistas en un estómago sano pero inflamado
En la etapa temprana de gastritis no atrófica, el revestimiento del antro está dominado por tres tipos principales de células epiteliales: células mucosas de fosa que recubren la superficie, células mucosas de glándula más profundas y un grupo más pequeño de células progenitoras ubicadas entre ellas. Mediante el análisis de la actividad génica y de “puntuaciones” de desarrollo, el equipo demuestra que estas células progenitoras ocupan la raíz del sistema, dando lugar tanto a las células mucosas de fosa como a las de glándula a través de un estado intermedio menos comprometido. Proteínas de control específicas, especialmente una llamada TAGLN2, se activan cuando las progenitoras se convierten en células mucosas de fosa, ayudando a impulsar este proceso normal de renovación durante la inflamación.
Cuando la reparación se transforma en tejido de tipo intestinal
A medida que la enfermedad progresa hacia gastritis atrófica crónica y luego a metaplasia intestinal, el equilibrio de linajes cambia. Las células mucosas de fosa disminuyen, mientras que las células mucosas de glándula y nuevos tipos celulares de aspecto intestinal se expanden. En la metaplasia intestinal, los investigadores observan que tanto las células progenitoras como las células mucosas de glándula pueden adquirir características de células madre de tipo intestinal y luego madurar hacia enterocitos absortivos, las células emblemáticas del intestino. Trazan dos trayectorias paralelas que convergen en un estado intermedio de células madre de tipo intestinal antes de terminar en enterocitos plenamente desarrollados. Otra rama progenitora secretora da lugar a células caliciformes, las células secretoras de moco que se encuentran normalmente en el intestino. Un conjunto de proteínas reguladoras del metabolismo, especialmente HNF4A y ESRRA, se vuelven progresivamente más activas a lo largo de estas rutas y parecen dirigir la transformación gástrica a intestinal. Mapas espaciales de tejido humano muestran un gradiente suave de marcadores a lo largo de las glándulas, confirmando que estas transiciones ocurren de forma continua y en capas.
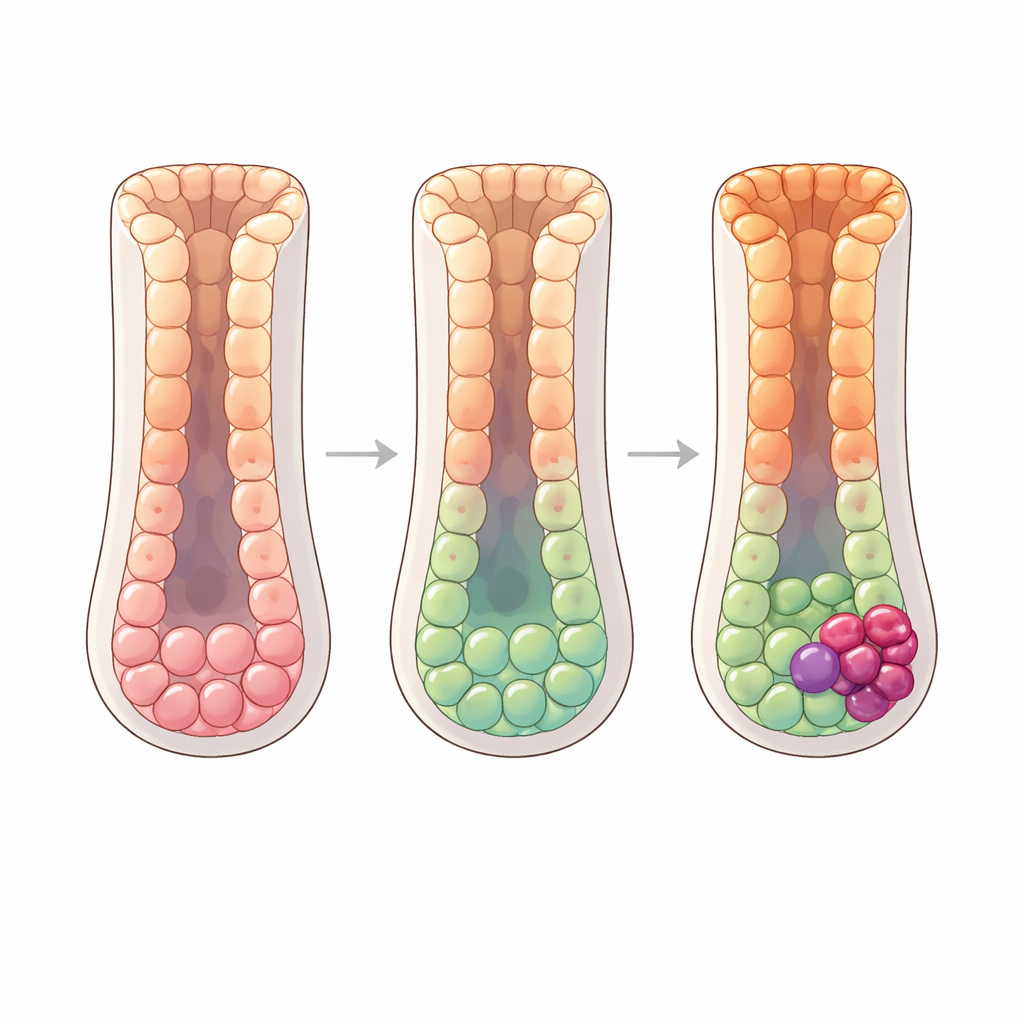
Localizando las células probablemente iniciadoras de los tumores tempranos
En muestras de cáncer gástrico temprano, el equipo investiga qué células no cancerosas se parecen más a las células cancerosas emergentes tanto en expresión génica como en alteraciones cromosómicas. Las células progenitoras muestran la mayor similitud, incluidos patrones coincidentes de cambios en el número de copias, lo que sugiere que al menos algunos cánceres surgen directamente de este grupo. Dentro de las progenitoras, identifican un subconjunto marcado por dos genes, KIAA0101 y PRAP1, que están fuertemente enriquecidos en tejido canceroso y son apenas detectables en otros lugares. Estas células doblemente positivas se agrupan dentro de regiones malignas en mapas espaciales y se destacan mediante tinciones fluorescentes, lo que respalda la idea de que son precursoras inmediatas de tumores tempranos. Proteínas regulatorias adicionales, como SIRT6 y XRCC4, se activan a medida que estas progenitoras transitan hacia células cancerosas y pueden ayudar a sostener la tolerancia al daño del ADN, la inflamación y la supervivencia durante este cambio peligroso.
Qué significa esto para la prevención y la detección precoz
Para un observador no experto, este trabajo convierte una imagen difusa—“la irritación estomacal puede conducir al cáncer”—en un mapa detallado de quién hace qué, cuándo y dónde dentro de las glándulas del antro gástrico. Muestra que un pequeño grupo de células progenitoras y de células mucosas de glándula actúa como un motor central que puede ser redirigido desde la reparación normal hacia la construcción de tejido de tipo intestinal y, eventualmente, al cáncer temprano. Al señalar marcadores moleculares específicos de progenitores de alto riesgo (como KIAA0101 y PRAP1) y conmutadores de control clave (HNF4A, ESRRA, SIRT6), el estudio sugiere nuevas pruebas que podrían identificar cambios peligrosos en biopsias rutinarias y nuevos objetivos terapéuticos diseñados para interrumpir el proceso antes de que se forme un tumor visible.
Cita: Yin, H., Zhang, H., Zheng, S. et al. Dissecting the differentiation origins of intestinal metaplasia and early intestinal-type gastric cancer in gastric antrum by single-cell RNA profiling. npj Precis. Onc. 10, 167 (2026). https://doi.org/10.1038/s41698-026-01355-8
Palabras clave: cáncer gástrico, metaplasia intestinal, secuenciación de ARN unicelular, linaje celular, lesiones precancerosas