Clear Sky Science · ru
Анализ происхождения дифференцировки кишечной метаплазии и раннего кишечного рака желудка в антральном отделе с помощью одноклеточного РНК‑секвенирования
Почему изменения клеток слизистой желудка имеют значение
Рак желудка — один из самых смертоносных видов рака в мире, отчасти потому, что часто обнаруживается на поздних стадиях. Однако до появления опухоли клетки, выстилающие нижнюю часть желудка (антрум), проходят ряд тонких изменений, развивающихся годами. В этом исследовании поставлен простой, но ключевой вопрос: какие именно клетки на этом пути первыми начинают вести себя как раковые и как обычные желудочные клетки перепрограммируются в кишечноподобные, а затем — в раковые? Наблюдая за отдельными клетками по одной, исследователи отображают это скрытое превращение и указывают новые подходы для более раннего обнаружения и возможного предотвращения рака. 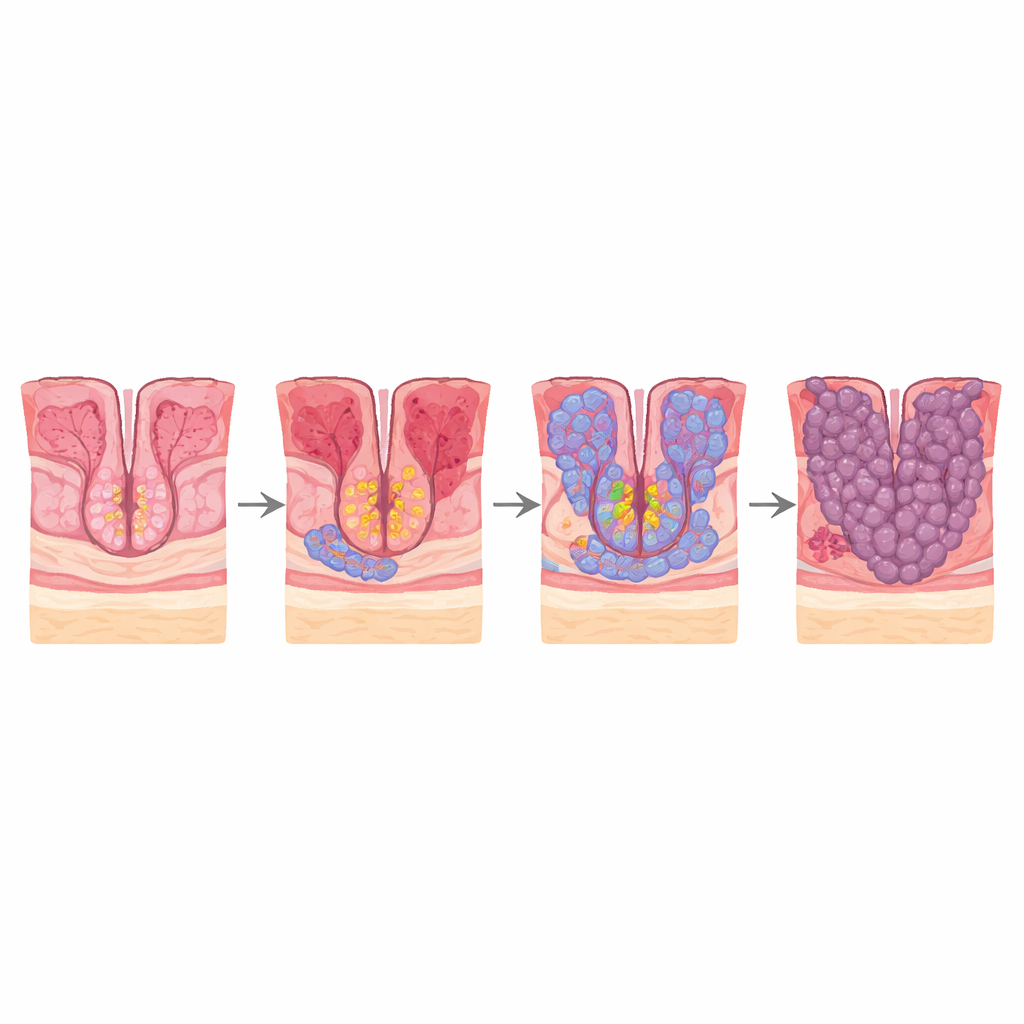
Прослеживая путь от раздражения к раннему раку
Большинство кишечных форм рака желудка возникают по хорошо описанной последовательности: хронический гастрит, утрата нормальных желез (атрофия), замещение желудочных клеток клетками, похожими на кишечные (кишечная метаплазия), и, наконец, ранний рак. Авторы повторно проанализировали данные одноклеточного РНК‑секвенирования биопсий, охватывавших весь этот путь — неатрофический гастрит, атрофический гастрит, кишечную метаплазию и ранний рак желудка. Эта технология фиксирует, какие гены активны в тысячах отдельных клеток, позволяя классифицировать каждую клетку и восстанавливать ее вероятное «родословное древо». Они объединили эти данные с пространственным транскриптомомом, который возвращает информацию о местоположении каждой клетки в ткани, и с окрашиванием образцов пациентов для подтверждения ключевых закономерностей.
Ключевые игроки в здоровом, но воспаленном желудке
На ранней стадии неатрофического гастрита в выстилке антрума доминируют три основных эпителиальных типа клеток: поверхностные бокаловидные (pit mucous) клетки, железистые слизистые (gland mucous) клетки, находящиеся глубже в железах, и более небольшой пул прогениторных клеток между ними. Анализ активности генов и «оценок» развития показывает, что эти прогениторы находятся в корне системы, давая начало как поверхностным, так и железистым слизистым клеткам через промежуточное, менее дифференцированное состояние. Конкретные регуляторные белки, особенно белок TAGLN2, включаются по мере превращения прогениторов в поверхностные слизистые клетки и помогают управлять нормальным процессом обновления во время воспаления.
Когда восстановление превращается в кишечноподобную ткань
В прогрессировании болезни к хроническому атрофическому гастриту и затем кишечной метаплазии баланс клеточных линий сдвигается. Поверхностные слизистые клетки сокращаются, в то время как железистые слизистые клетки и новые кишечноподобные типы клеток расширяются. При кишечной метаплазии исследователи обнаружили, что и прогениторные клетки, и железистые слизистые клетки могут приобретать признаки кишечноподобных стволовых клеток и затем созревать в абсорбтивные энтероциты — ключевые клетки кишечника. Они прослеживают два параллельных пути, которые сходятся в промежуточном кишечноподобном стволовом состоянии, прежде чем завершиться в полностью развитых энтероцитах. Другая ветвь секреторных прогениторов порождает бокаловидные клетки, слизевыделяющие клетки, характерные для кишечника. Набор метаболических регуляторов, особенно HNF4A и ESRRA, постепенно активируется вдоль этих путей и, по-видимому, направляет преобразование желудочной ткани в кишечную. Пространственные карты человеческой ткани показывают плавный градиент маркеров вдоль желез, подтверждая, что эти переходы происходят непрерывно и послойно. 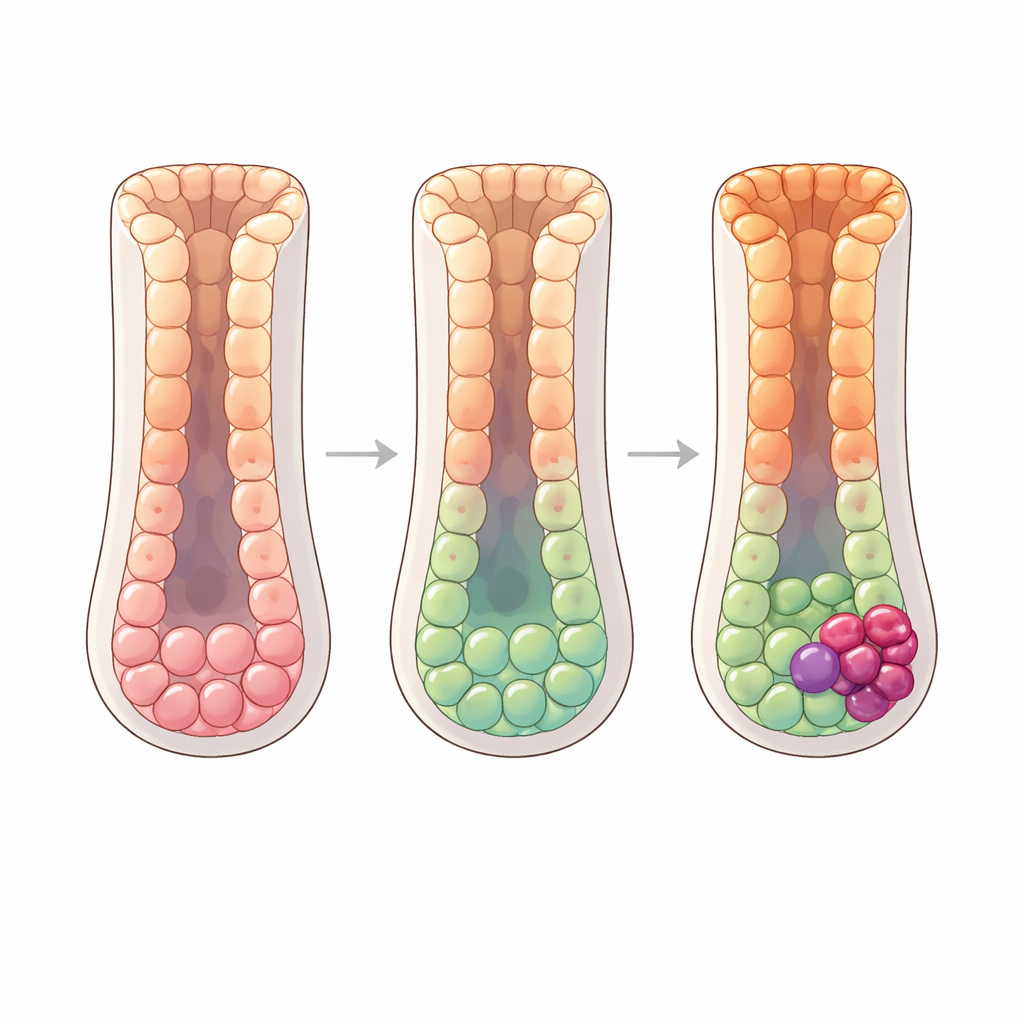
Определение вероятных исходных клеток ранних опухолей
В образцах раннего рака желудка команда выясняла, какие нормальные клетки наиболее сходны с возникающими раковыми клетками по экспрессии генов и по хромосомным изменениям. Пул прогениторных клеток показал наибольшее сходство, включая соответствие паттернов изменений числа копий хромосом, что говорит о том, что по крайней мере часть опухолей возникает непосредственно из этого пула. Среди прогениторов они выделили подгруппу, отмеченную двумя генами — KIAA0101 и PRAP1, — которая сильно обогащена в раковой ткани и почти не обнаруживается в других участках. Эти двуположительные клетки образуют кластеры в зонах поражения на пространственных картах и подсвечиваются при флуоресцентном окрашивании, что поддерживает идею о том, что они являются непосредственными предшественниками ранних опухолей. Дополнительные регуляторные белки, такие как SIRT6 и XRCC4, активируются по мере перехода этих прогениторов в раковые клетки и могут способствовать терпимости к повреждению ДНК, воспалению и выживанию в ходе этого опасного преобразования.
Что это означает для профилактики и ранней диагностики
Для неспециалиста эта работа превращает расплывчатую идею — «раздражение желудка может привести к раку» — в подробную дорожную карту того, кто что делает, когда и где внутри желез антрума. Показано, что небольшой пул прогениторов и железистых слизистых клеток действует как центральный двигатель, который может быть перенаправлен от нормального восстановления к формированию кишечноподобной ткани и, в конечном счете, к раннему раку. Идентификация конкретных молекулярных маркеров высоко‑рисковых прогениторов (таких как KIAA0101 и PRAP1) и ключевых регуляторных переключателей (HNF4A, ESRRA, SIRT6) предлагает новые тесты, способные выявлять опасные изменения в рутинных биопсиях, а также новые мишени для терапии, направленной на прерывание этого процесса до образования видимой опухоли.
Цитирование: Yin, H., Zhang, H., Zheng, S. et al. Dissecting the differentiation origins of intestinal metaplasia and early intestinal-type gastric cancer in gastric antrum by single-cell RNA profiling. npj Precis. Onc. 10, 167 (2026). https://doi.org/10.1038/s41698-026-01355-8
Ключевые слова: рак желудка, кишечная метаплазия, одноклеточное РНК‑секвенирование, клеточная линия, предраковые поражения